
①制汽轮机叶片 ②制有机玻璃 ③制永久性模具 ④制造柴油机 ⑵氮化硅晶体属于 晶体(填晶体类型)。
⑶下列物质融化时,所克服的微粒间作用力与氮化硅熔化时所克服的微粒间作用相同的是 。 ①单质I2和金刚石 ②晶体硅和二氧化硅 ③冰和干冰 ④金刚石和碳化硅
⑷已知氮化硅晶体结构中,原子间都以单键相连,且N原子和N原子、Si原子和Si原子不直接相连,同时每个原子都满足8电子稳定结构。请写出氮化硅的化学式: ,1 mol 氮化硅晶体中含 mol N—Si键。
⑸现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅。反应的化学方程式为: 。
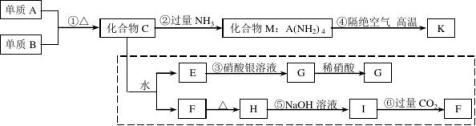
材料科学是近年来化学研究的热点之一。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性,它是以中学化学中的常见物质为原料来生产的,下图虚线框外为其生产过程;虚线框内的其他转化是为探究C的组成而设,G、H均为难溶于水的白色固体;图中C、M、K均含A元素,C物质遇水强烈水解,能生成一种白色胶状物质F和E的酸雾,其余物质均为中学化学常见物质。请回答下列问题:
A.以二氧化硅为主要原料制造光导纤维 B.碳炉边放盆水,可防止煤气中毒 C.在墙壁刚粉刷过石灰浆的室内生一炭火盆,墙壁会冒汗 D.用干冰进行人工降雨 2、下列说法正确的是 A.SiO2能和水发生化合反应生成硅酸 B.SiO2是酸性氧化物,它不溶于任何酸 C.SiO2的俗名叫水玻璃,不溶于水 D.SiO2又叫水晶,能溶于NaOH溶液中
3、①盐酸、②浓硫酸、③氧气、④氢氟酸、⑤氢氧化钾溶液中,能与地壳中含量第一和第二的两元素形成的化合物起化学反应的是 A.①② B.④⑤ C.②④ D.③④
4、将过量的二氧化碳通入下列溶液中,最终会出现浑浊的是 A.氯化钙溶液 B.澄清的石灰水 C.水玻璃 D.硝酸钡溶液
5、熔融烧碱应选用的器皿是 A.铁制坩埚 B.普通玻璃坩埚 C.石英坩埚 D.陶瓷坩埚 6、下列关于碳和硅的叙述中,不正确的是 A.+4价氧化物都与氢氧化钠溶液反应 B.单质在加热时都能与氧气反应
C.氧化物都能溶于水生成相应的酸 D.碳和硅两种元素都有能导电的单质 7、和空气接触可发生非氧化还原反应的物质组合是 ① Na ②Na2SiO3溶液 ③Na2O2 ④烧碱溶液 ⑤石灰水 ⑥Fe(OH)2 A.①③④ B.②④⑤ C.②③⑥ D.①④⑤
8、某无色混合气体可能含有CO2、H2、CO和H2O(气)中的一种或几种,依次进行以下处理(假设每次处理均反应完全):①通过盛有硅胶的干燥管时,气体体积不变;②通过炽热的氧化铜时,固体变为红色;③通过白色CuSO4粉末时,粉末变蓝色;④通过澄清石灰水时,溶液变浑浊。则原混合气体的成分不可能是 A H2和CO B CO2、H2和CO C H2O和CO2 D H2和CO2
⑴指出K可能所属的晶体类型____________;⑵写出化学式:单质B__________,化合物F___________; ⑶写出图中下列反应的离子方程式:⑤____________________________________________________, ⑥____________________________________________________;
⑷写出反应④的化学反应方程式:_________________________________________。
第 1 页 邮编:830054
二、非选择题(每空3分,共计60分)
9、下表中括号内的物质是杂质,试将除杂试剂和分离方法填入表中:
新疆师范大学附属中学2013届高三化学备课组
第二篇:高一化学必修一第三章金属及其化合物方程式总结
第三章 金属及其化合物
反应方程式总结
本章以Na、Al、Fe为例介绍金属及其化合物的性质和用途,以“单质—>氧化物—>氢氧化物—>盐类”的顺序介绍其相应性质,物质之间的化学反应多切杂,但是杂中有序,希望同学能熟练、灵活运用。对本章主要反应做出以下总结:【写出相应的化学方程式】
Na、Na2O、Na2O2的颜色,Na2CO3、NaHCO3的颜色状态、溶解性、俗称;Al、Al2O3、Al(OH)3的物理性质,重点掌握Al及其化合物的两性【既与酸反应又与强碱反应】;掌握Fe、FeO、Fe2O3的颜色,俗称,及Fe2+与Fe3+之间的转换关系。
1、 Na在空气中氧化
2、 Na在空气中加热
现象:
3、 Na与水反应
现象
4、 Na与硫酸反应
5、 Na与饱和氢氧化钙溶液反应方程式及现象
6、 Na与硫酸铜溶液反应方程式及现象
7、 Na与饱和硫酸铵反应方程式及现象
8、 Na与硫酸铁反应
9、 Na2O与水反应
10、 Na2O与CO2反应
11、 Na2O2与水反应
12、 Na2O2与CO2反应
13、 NaOH与适量CO2反应
14、 NaOH与过量CO2反应
15、 向饱和Na2CO3溶液中通入CO2
16、 向Na2CO3溶液中逐滴加入HCl溶液现象及反应方程式
17、 向Na2CO3溶液中加入CaCl2溶液
18、 向Na2CO3溶液中加入Ba(OH)2溶液
19、 向NaHCO3溶液中逐滴加入HCl溶液现象及反应方程式
20、 向NaHCO3溶液中逐滴加入CaCl2溶液,是否有现象?能否发生反应?
21、 向NaHCO3溶液中加入足量Ba(OH)2溶液
22、 向NaHCO3溶液中加入少量Ba(OH)2溶液
23、 向NaHCO3溶液中加入NaOH溶液
24、 加热NaHCO3固体,并将气体导入澄清石灰水,现象及相关反应方程式
25、 Al在空气中氧化
26、 Al与HCl溶液反应
27、 Al与NaOH溶液反应
28、 Al2O3与HCl溶液反应
29、 Al2O3与NaOH溶液反应
30、 Al(OH)3的实验室制法
31、 Al(OH)3与HCl溶液反应
32、 Al(OH)3与NaOH溶液反应
33、 高温加热Al(OH)3
34、 向AlCl3溶液中逐滴加入NaOH溶液,现象及相应方程式
35、 向AlCl3溶液中加入过量的NaOH溶液
36、 已知偏铝酸(HAlO2)为积弱的酸,酸性比H2CO3还弱,在溶液中,
偏铝酸极易结合水分子形成H3AlO3形式的化合物即Al(OH)3向NaAlO2溶液中通入CO2现象及方程式
37、 向NaAlO2溶液中逐滴加入HCl溶液的现象及方程式
38、 Fe在氧气中燃烧
39、 铁粉与水蒸气高温下反应
40、 Fe与稀盐酸反应
41、 FeO与稀盐酸反应
42、 Fe2O3与稀盐酸反应
43、 向FeCl2溶液中加入NaOH溶液的现象及方程式
44、 向FeCl3溶液中加入NaOH溶液的现象及方程式
45、 高温加热Fe(OH)3
46、 向FeCl3溶液中加入足量铁粉
47、 向FeCl3溶液中加入铜粉
48、 向FeCl2溶液通入氯气(或加入氯水)
49、 实验室如何鉴别Fe2+和Fe3+
50、 如何检验溶液中是否含有Fe2+
