��ϰר���� �� ���ǽ�������
����ϰĿ�
1. �˽������Ȼ��Ĵ�����ʽ�����ʡ�
2. ֪������������������ʺͻ�ѧ���ʡ�
3. ֪�������ε����ʺ���;��
4���˽�����ι�ҵ��
��֪ʶ���ɡ�
һ���������
1������������ʣ�
2����Ļ�ѧ���ʣ�
�� �����£�ֻ�������������ᣨHF�����ռӦ
�� ���������£��ܺ�һЩ�ǽ������ʷ�Ӧ
Si + O2 ��
Si + Cl2 ��
Si + C ��
3������Ʊ���
���������⡿
��1������Ȼ���������ڵؿǵĸ��ֿ������ʯ�е���ʽ�� ��
A������� B���������� C������ D��������
��2�����ڹ��˵������ȷ���� (
A��������Ƿǽ���Ԫ�أ����ĵ����ǻҺ�ɫ���н�������Ĺ���
B�������ĵ����Խ��ڽ����;�Ե��֮�䣬�����õİ뵼��
C����Ļ�ѧ���ʲ����ã������²����κ����ʷ�Ӧ
D�����ȵ�һ���¶�ʱ��������̼�������ȷǽ�����Ӧ
�����������������
1����������
2����ѧ���ʣ���������Ļ�ѧ���ʲ����ò���ˮ��ӦҲ������vHF����w��Ӧ�� �������������������
SiO2 + H2O ��
SiO2 + CaO ��
SiO2 + NaOH ��
[˼��] ��α���ǿ����Һ��
�� ���η�Ӧ
SiO2 + Na2CO3 ��
SiO2 + CaCO3 ��
�� ��������
�� ���ԣ�
[˼��] ��α���������ȡ�������ʲô������
90 ) ��
���������⡿
��3������˵����ȷ����
A��������������ˮ������
B�����ά������������dz�ǿ�����ù���ͨѶ����ͬʱ���ʹ�����Ϣ
C����Ϊ����ʱ����������̼���Ʒ�Ӧ�ų�CO2�����Թ�������Ա�̼��ǿ
D������������������������������κ��ᡣ
��4���������ʲ���������跴Ӧ���� ��
A���ռ� B������� C������ D��ʯ��ʯ ��
�������ᡢ������
1��ԭ����v �w����v �w������ˮ�������Ա�̼������ע�⣻����
��ˮ�Ͷ�������ֱ�ӷ�Ӧ�ƹ��ᣩԭ�����ɫճ��״���ʣ��ܲ��ȶ����ڿ�������
ʧȥ ���� ��Ӧʽ��
�����ǰķ�ĩ״�����ʣ�������Ⱥ��� ���� ��
2��������
��1����������
��2����ѧ���ʣ�
��3�����棺
���������⡿
��5���������ڴ�ĥ�����IJ����Լ�ƿ�е��Լ��� �� ��
A��KOH��Һ B��ŨH2SO4 C��ˮ���� D�������
�ģ������ι�ҵ
1������
��1��ԭ�ϣ� �� ��
��2��ԭ���� ��
��ͨ��������Ҫ�ɷ֣� CaSiO3 ��Na2SiO3��SiO2
ʯӢ��������SiO2 �ֻ�����������ͨ�����ɷ�һ��
��ɫ����������ͨ�����м�һЩ����������
�� CuO����ɫ��Co2O3����ɫ��MnO2����ɫ��Fe2����ɫ
2��ˮ�ࣺԭ�ϣ�3���մ�
��ͳ�մ����� ��Ϊ��Ҫԭ���ճɵ���Ʒ���������ɶ�ף�
����ˮ�ԣ�������֯���ܣ���������ˮ�����ſ�ѧ�����ķ�չ��һЩ��������ṹ��
�ܵ��������ǽ�������������Ƴ������磺 �� �� �ȡ�
���������⡿
��6�����Ʋ�������ˮ�����ֹ�ҵ�����У�����Ҫ��ԭ���� �� ��
A����ʯ�� B��ʯ��ʯ C��ʯӢ D������
��7������ͨ������Ҫ�ɷ�һ������ ( )
A���ֻ����� B������ֽ C���л����� D��ˮ������
91
��������ϰ��
1�������йع輰�仯����������У�������� �� ��
A�����ʹ������õİ뵼����� B���賣��ʱ���Ժ�ǿ�Ӧ
C�������ǻӷ����� D����������㷺��������Ȼ��
2����һ��ʱ�ڣ�һЩ��֪�����ڶ�ͨѶ�����������еĹ������Ǯ������Ǽ�û������Ǯȴ�ƻ���ͨѶ��ʩ��Υ���˹��ҷ��ɡ�����ͨѶ����о�IJ����� �� ��
A��ͭ B���� C���� D����������
3�����������������ǽ����������Ե��� �� �� ���ܳ��ܸ��¡�ǿ�ȸ� �ھ��е�ѧ���� �۾��й�ѧ���� �ܾ����������� �ݿ����Ժ�
A���� B���٢� C���٢ڢۢ� D���٢ڢۢ�
4 ��������մ�Ҳ��һ���������ǽ������ϣ����������Ƴ��������������������������� �� ��
A.���µ����� B.��ѧ���� C.��ѧ���� D.���﹦��
5��������������һ������������SiO2��Ӧ���� ( ) ��ŨH2SO4����H2O����Ũ�����������KOH��Һ���������ƣ���̼����
A���٢ڢ� B���ڢ� C���ܢݢޢ� D���ۢܢݢ�
6�����з�Ӧ����һ���õ����� �� ��
A��SiO2�D��Na2SiO3 B��SiO2�D��H2SiO3
C��Na2SiO3�D��SiO2 D��H2SiO3�D��SiO2
7�����й�ҵ�����в����������������̼���� �� ��
A����̼�Ͷ��������ƴֹ� B���Ʋ��� C����ˮ�� D��������ʯ��
8���ڻ��ռ�Ӧѡ�õ������� �� ��
A�������� B�� �������� C��ʯӢ���� D��������
9����������Һ��ͨ��CO2���壬�����ܲ����������� �� ��
A���Ȼ��ƺ����ᱵ�Ļ��Һ B��ϡ��ˮ����
C�����ǻ�����������Һ D��̼���Ʊ�����Һ
10��Ӧ�ô������IJ����Լ�ƿ�������Һ��
A������ B����������Һ C��ˮ���� D��Ũ����
11������ˮ��Ͳ������������ܽ�������ι�ҵ��һ���ص��� �� �������������ǹ����Σ��ڷ�Ӧ�����Ǹ��£��ۺ��й��������ԭ�ϣ��ܷ�Ӧԭ����һϵ�и��ӵ�����-��ѧ�仯
A���٢� B���٢ڢ� C���٢ڢۢ� D���٢ۢܪ�
12�����������У���Ҫ�ɷֲ��Ƕ���������� ( )
A�����ɰ B����� C��ˮ�� D��ʯӢ
13��Ҫ��ȥSiO2�л��е�����CaO���ʣ������˵��Լ��� ( )
A��������Һ B������ C������ D����������Һ
92 �� ��
14���������ʵ���Ҫ�ɷֲ����ڹ����ε��� �� ��
A��ˮ�� B���մ� C��ˮ���� D����ͨ����
15�����и���������ˮ���ܴ���������� �� ��
������A��K+��H��SiO32��S2 B��Na+��K+��H+��SiO32-
���� C��Na+��Cl-��OH��HCO3 D��Na+��H+��NO3-��SO42-
16������ʯ��ʯ���������衢���������ְ�ɫ��ĩ��Ҫ��һ���Լ����𣬿�ѡ�ã� ��
A������������Һ B������ C����������Һ D���Ȼ�����Һ
17�����������У��Ȳ��������ᷴӦ���ֲ����ռ���Һ��Ӧ���� �� ��
A��ˮ���� B���������� C��һ����̼ D��������
18�����������ʵı�����Һ��ͨ��CO2����������Ӧ���� �� ��
A��Na[Al(OH)4] B��NaHSO4 C��Na2SiO3 D��Ca(ClO)2
19������������ɿɱ�ʾΪAl2Si2Ox(OH)y������x��y����ֵ�ֱ�Ϊ �� ��
A��7��2 B��5��4 C��6��3 D��3��6
20����������ɫ����Һ��Ca(HCO3)2��Һ��Na2SiO3��Һ�ͳ���ʯ��ˮ����������Һ�зֱ�ͨ��CO2���塣�Ը���ʵ�������жϣ�
��1�����ɰ�ɫ�������˳����������������������������Һ����ԭ��ҺΪ ��
��2�����ɰ�ɫ�������˳����������������������������Һ����ԭ��ҺΪ ��
(1)����ʯ��ˮ; ��2��Na2SiO3��Һ
21����A��B��C��D��E���ֶ�����Ԫ�ص����ʣ������ܷ������±仯����1��C���Ⱥ�ʧˮ����D����2��A��Һ�������Һ��Ӧ���ɰ�ɫ����E����3��D���ռӦ����A��ˮ��
��4��B�ڿ�����ȼ������D����5��D�ڸ�������̼��Ʒ�Ӧ����E��һ�����壻��6��A��Һ�����ᷴӦ�����ɰ�ɫ��״��������7��D�ڸ�������̼��Ӧ���ɵ���B�����Ʋ�A��
B��C��D��E��Ϊ�����д����1������7�������仯�Ļ�ѧ����ʽ��
��1��_____________________________________________________________________��
��2��_____________________________________________________________________��
(3)_______________________________________________________________________��
��4��_____________________________________________________________________��
��5��_____________________________________________________________________��
(6)_______________________________________________________________________��
(7)_______________________________________________________________________�� 93
�ڶ�ƪ������л������������֪ʶ���ܽἰϰ��
���������������
һ������
1�����������ṹ
��1���������������������ڳ����У�����������˹��ú��Ŀӵ��У�����Ȼ�����ؿ��У���
��2������ʽ��CH4������ʽ��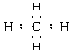 �ṹʽ��
�ṹʽ��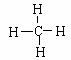 ��
��
��3������ռ�ṹ�������������� �ṹ��̼ԭ��λ���ߣߣߣߣ������㶼���ߣߣߣߣ���
2���������������
�������ߣ�ɫ�ߣ�ζ�ߣ��壬�ȿ����ߣ����ߣ�����ˮ��������CCl4��
3������Ļ�ѧ����
��1���ȶ��ԣ�һ������£����ʺ��ȶ�����ǿ�ᡢǿ���ǿ�������Ȳ���Ӧ��
��2����ȼ�ԣ�CH4+2O2 CO2+2H2O
CO2+2H2O
��3��ȡ����Ӧ���л���������ijЩԭ�ӻ�ԭ���ű�����ԭ�ӻ�ԭ����������ķ�Ӧ��ȡ����Ӧ�������������ڹ��������·�Ӧ������ɫ���ߣߣߣ���ƿ�ڳ����ߣߣߣ���˵�������˲�����ˮ�����ʡ�ƿ�����ߣߣ���ʹʪʯ����ֽ���ߣ����ƶ����Ȼ������ɡ��ĸ���Ӧ�ķ���ʽ�ߣߣߣߣߣߣߣߣߣߣ����ߣߣߣߣߣߣߣߣߣߣߣߣߣ����ߣߣߣߣߣߣߣߣߣߣߣ����ߣߣߣߣߣߣߣߣߣߣߣ���
��������
��1��������̼ԭ�Ӽ��Ե�����ϳ���״��̼ԭ��ʣ��ۼ�ȫ������ԭ�ӽ�ϵ�����Ϊ����(Ҳ�б�������)
��2��������ͨʽ��
��3����������ͨ�ԣ���״̬��C1-C4����������Ϊ��̬��C5-C11Һ̬��C��>11Ϊ��̬���۷е㣺Cԭ����Խ�࣬�۷е�Խ�ߡ�Cԭ������ͬʱ��֧��Խ�࣬�۷е�Խ�͡���ˮ���ԣ�������ˮ���������л��ܼ���
��4��������������̼ԭ������10�����ڣ������á���ɡ����ס��ҡ����������졢�ѡ����������ɡ������̼ԭ�����������ϡ��顱�֣�̼ԭ������10�����ϣ��ú������ֱ�ʾ����ʮ����)��ϵͳ���������������裺�� ����Cԭ�Ӹ�������ࣻ�� ����֧������̼���������֧�������һ�˱�ţ���֧��λ��֮����С����д���ƣ� �� �� ��
����ͬϵ���ͬ���칹��
1��ͬϵ�P���ж�
��1��ͬϵ��Ķ��壺�ṹ���ƣ��ڷ�����������һ�������ɸ���CH2��ԭ���ŵ��л����Ϊͬϵ�
��2���ж����ݣ��ٷ�����ɷ���ͬһ �����˴������ɸ�ϵ�CH2��������̼������̼�����ṹ ���뻷�Ĵ�С�أ��������������ŵ�������� �����л���������� ��
��3��ͬϵ��ͨʽ�Ĺ��ɺ�Ӧ�ã��ܽ�һϵ�о������ƽṹ��ͬϵ���ͨʽ��Ӧ������ѧ�������������ҳ���ͬ���ʵķ���ʽ��ȷ��ϵ��ٸ�����ʼ̼������ȷ��ͨʽ��Ȼ������ͨʽ����ѧ����֪ʶ������ͬϵ����̼���������
2��ͬ���칹�����д�������ж�
�����������ͬ�ķ���ʽ�������в�ͬ�ṹ��������ͬ���칹��������������춡�顣����ͬ������Ļ����ﻥ��Ϊͬ���칹�塣
��1��ͬ���칹������ࣺ��̼���칹��ָ̼ԭ��֮�����ӳɲ�ͬ����״��״�ṹ����ɵ��칹������λ���칹��ָ�����Ż�ȡ������̼���ϵ�λ�ò�ͬ����ɵ��칹����������칹��ָ�л�������еĹ����Ų�ͬ���л������ͬ����ɵ��칹��Ҳ�й������칹����
��2��ͬ���칹�����д���������� �����л���ķ�������ж�����ܵ�����칹��һ����ͨʽ�жϣ�����д �����л��������칹д�������칹�Ŀ��ܵ�̼���칹��һ����á������������ɸ���Ϊ��дֱ����һ�ߴ���ȡ���������м䣻һ���ţ������ˣ���̼ʱ������ɢ������ ��һ������д�����������ŵ�����ͬ���칹�壬Ȼ���ڸ���̼���������ƶ������ŵ�λ�ã����������������ϵĹ�����ʱ������һ�������ţ������ϵڶ��������ţ��������ơ����� ������̼�ļ�����ԭ����̼ԭ��ʣ��ļۼ�����ԭ��ȥ���ͣ��Ϳɵ�����ͬ���칹��Ľṹ��ʽ��
��3��ͬ���칹����ж����ݣ��ٷ���ʽ���� ����Է���������ͬ���ṹ��ͬ�Ļ����ﲻһ����ͬ���칹�壬��C8H18��C7H14O���ڽṹ ��̼���Ǽܲ�ͬ�����������̼���ϵ�λ�ò�ͬ������������ͬ��
���
һ��1���������壬������������ģ���ԭ��2���ޡ��ޡ�����С������
3����ȥ����״СҺ�Σ�������������죬�ƶ����Ȼ������ɣ�CH4+Cl2 CH3Cl+HCl(CH3Clһ�ȼ��飬������ˮ������)��CH3Cl+Cl2
CH3Cl+HCl(CH3Clһ�ȼ��飬������ˮ������)��CH3Cl+Cl2 CH2Cl2+HCl(CH2Cl2���ȼ��飬������ˮ)��CH2Cl2+Cl2
CH2Cl2+HCl(CH2Cl2���ȼ��飬������ˮ)��CH2Cl2+Cl2 CHCl3+HCl(CHCl3���ȼ��飬�����ȷ£�������ˮ���л��ܼ�)��CHCl3+Cl2
CHCl3+HCl(CHCl3���ȼ��飬�����ȷ£�������ˮ���л��ܼ�)��CHCl3+Cl2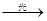 CCl4+HCl(CCl4���ȼ��飬�ֽ����Ȼ�̼��������ˮ���л��ܼ�)
CCl4+HCl(CCl4���ȼ��飬�ֽ����Ȼ�̼��������ˮ���л��ܼ�)
����CnH2n+2(n��1) ��������������룬֧��λ�Ρ�֧����Ŀ��֧������ij�顣
����ͨʽ�����ƣ���ͬ����ͬ�����̼������λ�����ͣ���ͬ����ͬ
ͬ����ϰ��
һ��ѡ���⣨�������15С�⣬ÿС��ֻ��һ����ȷ�𰸣�
1�������йؼ����˵���д������ (C )
A����ú���еļ���������ֲ����徭����Ͷ�����
B����Ȼ������Ҫ�ɷ��Ǽ���
C��������û����ɫ��û����ζ�����壬��������ˮ
D����������������ȡ����Ӧ�����ɵIJ������ȼ�����һ��Ч�ʽϸߵ�����
2�����й��ڼ������ʵ�˵���У�������� �� D��
A��������һ�ַǼ��Է���
B��������Ӿ�����������ṹ
C��������Ӿ��м��Լ�
D�����������H��C��H�ļ���Ϊ90��
3������������һ�������¿���CH4������ѧ��Ӧ���� ��C ��
A����ˮ B����ˮ C������ D������KMnO4��Һ
4���������ʵ����ļ����������Ϻ��������������³�ַ�Ӧ�����ò��������ʵ��������� �� D��
A��CH3Cl B��CH2Cl2 C��CCl4 D��HCl
5�����������������г��ȼ�պ� �������ȿ�ʹ��ˮ����ͭ�������ֿ�ʹ����ʯ��ˮ����ǵ��� ��B ��
A��SO2 B��CH4 C��H2 D��CO
6�������л��ﳣ���³�Һ̬���� ��C ��
A��CH3(CH2)2CH3 B��CH3(CH2)15CH3
C��CHCl3 D��CH3Cl
7���������̼���� ��C ��
A��ֱ���� B������������ C������� D����֧����ֱ����
8�������������л����ʽ�������п��ܻ�Ϊͬϵ���һ���� �� A��
A��16��30��58��72 B��16��28��40��52
C��16��32��48��54 D��16��30��42��56
9����ͬϵ��������ͬϵ�ﶼ�� ��D ��
A������ͬ�ķ�����
B���в�ͬ��ͨʽ
C������ͬ����������
D�������ƵĻ�ѧ����
10���ڳ��³�ѹ�£�ȡ����4����̬����1mol���ֱ���������������ȼ�գ������������������ǣ�D ��
A��CH4 B��C2H6 C��C3H8 D��C4H10
11���������ʵķ����У�������������ṹ���ǣ�A ��
A��CCl4 B��CHCl3 C��CH2Cl2 D��CH3Cl
12���������У��������Ӿ�����ͬ������������ͬ�ĵ��������ǣ�B ��
A��HCl B��NH3 C��NH4�� D��OH��
13�����ն����з�Ӧ����û��Ӱ����ǣ�C ��
A�������������ķ�Ӧ
B�����������ķ�Ӧ
C�������������ķ�Ӧ
D��������ķֽⷴӦ
14�����������в����������������ʵ��ǣ�C ��
A��ȼ�ղ���ֻ��CO2��H2O
B����±�ص��ʷ���ȡ����Ӧ
C��������ˮ
D��ͨ������ǿ�ᡢǿ�ǿ��������Ӧ
15������״���µ�11.2L�����22.4L������Ϻ��ȼ���ָ���ԭ״��ʱ������������Ϊ��A ��
A��11.2L B��22.4L C��33.6L D��44.8L
��������⣨���5С�⣩
16������ĵ���ʽΪ________���ṹʽΪ________��1 g���麬___1/16NA____��������ӣ�4 g ������____4.5________ gˮ��������ȣ���___17.5________gһ����̼ԭ������ȡ�
17�����������������һϵ�з�Ӧ����__ȡ��______��Ӧ�����ɵ��л����г������ܼ�����___CCl4________����������������____CCl4_________���ȷµĻ�ѧʽ��__CHCl3_________�����մ��෴Ӧ����д����������ڹ�������������������Ӧ�Ļ�ѧ����ʽ��
____________________________________________________________��
18��ijԪ��ԭ�ӵ������������Ǵ�������������������Ԫ���� ̼����Ԫ����Ԫ�����ڱ���λ���ڶ� �����ڢ�A �壻������Ԫ����ɵ���Ļ�����Ļ�ѧʽΪ CH4 �������ֻ���������Ԫ�ص���������Ϊ 25% ��
19��C8Hm������������mֵ���� 18 ��Cn H22����������nֵ���� 10 ����Է�������Ϊ212�������ķ���ʽΪ C15H32 ��
20�������м������ʣ���ʯī�ͽ��ʯ ��C2H6��C5H12 ��C2H4��C2H6 ��CH3CH2CH2CH3�� CH3CH(CH3)2 ��3517Cl��3717Cl�����������д���пհף�����ͬ���칹����� 4 ��ͬ����������� 1 ������ͬϵ����� 2 ������ͬλ�ص��� 5 ��
���������⣨���2С�⣩
21������ʱ20 mLij��̬���������������ϣ���ȫȼ�պ�IJ���ͨ��Ũ���ᣬ�ٻָ������£��������������50 mL ��ʣ��������ͨ������������Һ������ּ�����40 mL �������̬���ķ���ʽ�� C2H6
22��ȡ��״���¼�����������Ļ������840mL����ȼ����ȼ�պ�������ù����ļ�ʯ�����գ���ʯ������0.600g�����㣺��ʯ�����պ���ʣ������������״���£���336mL
