第 三 章 金 属 及 其 化 合 物 一 、 钠 1 、 钠 与 非 金 属 反 应 2Na+S=Na2S 钠在空气中燃烧(黄色的火焰) 2Na+O2 Na2O2 钠块在空气中变暗 4Na+O2=2Na2O Na2O 在空气中加热(变黄) 2Na2O+O2 2Na2O2 2、钠与水 反应(浮、熔、游、消、变、 ) 2Na + 2H2O = 2NaOH + H2 ↑ 2Na + 2H2O = 2Na + + 2OH - + H2 ↑ 3 、 钠 与 酸 反 应 2Na+2HCl=2NaCl+H2↑ 4.钠与碱反应:实质是钠与水的反应 5、钠与盐反应 Na 与盐溶液一 般不发生置换反应,但与熔融的盐可发生置换 4Na+TiCl4(熔融) Ti+4NaCl 6、Na 放入 盐溶液时,先与水反应,它包括两种情况: (1)如果盐溶液的溶质不与 NaOH 反应:如氯化钠 溶液 (2)如果盐溶液中的溶质与 NaOH 反应:生成的碱与盐发生复分解反应, 例如: 将 Na 放入 CuSO4 溶液中 2Na+2H2O=2NaOH+H2↑ 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 7 、 工 业 制 钠 : 电 解 熔 融 的 NaCl , 2NaCl( 熔 融 ) 2Na + Cl2↑ 8 、 氧 化 钠 与 水 反 应 Na2O + H2O = 2NaOH 9 、 氧 化 钠 与 CO2 反 应 Na2O + CO2 = Na2CO3 10 、 氧 化 钠 与 酸 反 应 Na2O + 2HCl = 2NaCl + H2O 11 、 过 氧 化 钠 与 水 反 应 2Na2O2 + 2H2O = 4NaOH + O2↑ 2Na2O2 + 2H2O = 4Na + + 4OH - + O2↑ 12 、 过 氧 化 钠 与 CO2 反 应 2Na2O2 + 2CO2 = 2Na2CO3 + O2 13 、 过 氧 化 钠 与 酸 反 应 2Na2O2+4HCl=4NaCl+2H2O+O2↑ 14、苏打(纯碱)与盐酸反应 ①盐酸中滴加纯 碱溶液 Na2CO3+2HCl=2NaCl+H2O+CO2↑ CO32 - + 2H + = H2O + CO2↑ ② 纯 碱 溶 液 中 滴 加 盐 酸 , 至 过 量 Na2CO3 + HCl = NaHCO3 + NaCl CO32 - + H + = HCO3 - NaHCO3 + HCl = NaCl + H2O + CO2↑ HCO3 - + H + = H2O + CO2↑ 15 、 小 苏 打 受 热 分 解 2NaHCO3 Na2CO3+H2O+CO2 ↑ 16、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热 NaHCO3 + NaOH Na2CO3 + H2O 溶 液 中 : HCO3 - + OH - = H2O + CO32 - 17 、 侯 氏 制 碱 法 反 应 式 : NaCl + NH3 + CO2 + H2O = NaHCO3 + NH4Cl 二、铝相关方程式 1、铝箔在氧气中剧烈燃 烧 4Al + 3O2 2Al2O3 2 、 铝 片 与 稀 盐 酸 反 应 2Al+6HCl=2AlCl3+3H2↑ 2Al +6H+=2Al3++3H2↑ 3、实验室制取 Al(OH)3 铝盐溶液加氨水的离子方程式: Al3+ + 3NH3?H2O= Al(OH)3↓+3NH4+ 4 、 铝 与 氢 氧 化 钠 溶 液 反 应 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑ 2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑ 5 、 铝 与 三 氧 化 二 铁 高 温 下 反 应 ( 铝 热 反 应 ) 2Al+Fe2O3 2Fe+Al2O3 6、Al2O3 与盐酸反应的离子方程式: Al2O3 + 6H+ =2Al3+ + 3H2O 7、Al2O3 与氢氧化钠溶液反应的离子方程式: Al2O3 +2OH=2AlO2- + H2O 8、Al(OH)3 与盐酸反应的离子方程式: Al(OH)3 +3H+ =
Al3++ 3H2O 9、 Al(OH)3 与氢氧化钠溶液反应的离子方程式: Al(OH)3+OH- = AlO2+2 H2O 10、氢氧化铝加热分解生成氧化铝和水: 2Al(OH)3 Al2O3 + 3H2O 11、氧化铝制取铝: 2Al2O3 4Al + 3O2↑ 12、氯化 铝溶液中加入过量的氢氧化钠溶液: Al3+ +4OH- = AlO2- + 2H2O 13、 氢氧化铝 加热分解生成氧化铝和水: 2Al(OH)3 Al2O3 + 3H2O 14、NaAlO2 溶液中 加入过量盐酸溶液的离子方程式: AlO2- + 4H+ = Al3++ 2H2O 15、氯化铝溶液中加 入 NaAlO2 溶液的离子方程式: Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓ 16、NaAlO2 溶 液中通入足量 CO2 的离子方程式: AlO2- +CO2+ 2H2O= Al(OH)3↓+ HCO3- 17、 氯化铝净水原理: AlCl3+3H2O====Al(OH)3(胶体)+ 3HCl 三 、 其 他 金 属 化 学 方 程 式 1 、 镁 在 空 气 中 燃 烧 : 2Mg+O2 2MgO 2、镁在卤素单质、硫等反应 Mg+ Cl2 MgCl2 Mg+ S MgS 3Mg+N2 Mg3N2 3、与 H2O 反应(Mg、A1 和冷水都不反应,但在加热条件下与水反应生成氢 氧化物和氢气) Mg+2H2O Mg(OH)2+H2↑ 2A1+6H2O 2A1(OH)3+3H2↑ 4、与酸反应置换出 H2 Mg、A1 与浓、稀盐酸、稀硫酸、磷酸等酸反应置换 出 H2,其中铝在冷浓 H2SO4,冷浓硝酸中发生钝化现象。所以可用铝制容器贮存冷的浓硫酸 或浓硝酸。 5、与某些氧化物反应 镁与二氧化碳反应: 2Mg+CO2 2MgO+C 6、高温下铁与水反应 3Fe+4H2O(g) Fe3O4+4H2 7、氧化铁溶于盐酸中 Fe2O3+6HCl=2FeCl3+ 3H2O Fe2O3+6H+=2Fe3++3H2O 8. 氯化 铁中滴入氢氧化钠溶液(红褐色沉淀) FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl Fe3++3OH -=Fe(OH)3↓ 9、 氯化亚铁溶液中通入氯气 2FeCl2+Cl2 =2FeCl3 2Fe2++Cl2=2Fe3++2Cl- 10、 氯化铁溶液中加入铁粉 2FeCl3 + Fe = 3FeCl2 2Fe3++Fe=3Fe2+ 11、用 KSCN 检验的存在离子方程式 Fe3++3SCN-= Fe (SCN)3 12、 铜与浓硫酸反应: Cu+2H2SO4 (浓) CuSO4 + 2H2O+SO2 ↑ 13、碳与浓硫酸反应: C+2H2SO4(浓) 2H2O +CO2↑+2SO2↑ 14、铁与盐酸、稀硫酸的反应: Fe + 2H+ == Fe2+ + H2O(反 应后溶液呈浅绿色) 15、铁与过量稀硝酸的反应: Fe + 4H+ + NO3- == Fe3+ + NO↑+ 5H2O ( 反 应 后 溶 液 呈 棕 黄 色 ) Fe + 4HNO3 ( 稀 ) = Fe(NO3)3 + NO↑ + 2H2O 铁 粉 过 量 : 3Fe + 8HNO3 ( 稀 ) = 3Fe(NO3)2 + 2NO↑ + 4H2O 16 、 铜 与 浓 硫 酸 的 反 应 Cu +2H2SO4(浓) CuSO4 + SO2↑+ 2H2O 17、 铜与浓硝酸的反应 Cu + 4HNO3 ( 浓 ) = Cu(NO3)2 + 2NO2↑+ 2H2O 18 、 铜 与 浓 硝 酸 的 反 应 3Cu + 8HNO3 ( 稀 ) = 3Cu(NO3)2 + 2NO↑+ 4H2O Cu + 2FeCl3 = 2FeCl2 + CuCl2 Cu + 2AgNO3 = 2Ag + Cu(NO3)2
第二篇:高中数学三角函数知识点总结(原创版)1
 高中数学三角函数知识点总结
高中数学三角函数知识点总结
(文一四六专用)
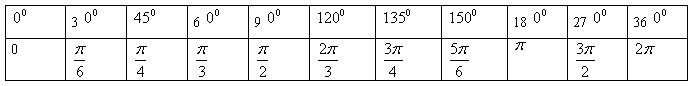
1.特殊角的三角函数值:

2.角度制与弧度制的互化: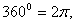
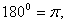
1rad=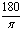 °≈57.30°=57°18ˊ. 1°=
°≈57.30°=57°18ˊ. 1°=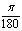 ≈0.01745(rad)
≈0.01745(rad)
3.弧长及扇形面积公式
弧长公式: 扇形面积公式:S=
扇形面积公式:S=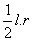
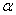 ----是圆心角且为弧度制。 r-----是扇形半径
----是圆心角且为弧度制。 r-----是扇形半径
4.任意角的三角函数
设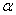 是一个任意角,它的终边上一点p(x,y), r=
是一个任意角,它的终边上一点p(x,y), r=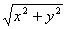
(1)正弦sin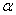 =
=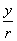 余弦cos
余弦cos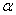 =
= 正切tan
正切tan =
=
(2)各象限的符号:


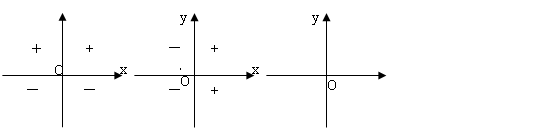
sin cos
cos tan
tan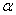
5.同角三角函数的基本关系:
(1)平方关系:sin2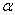 + cos2
+ cos2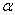 =1。(2)商数关系:
=1。(2)商数关系: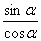 =tan
=tan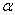
(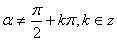 )
)
6.诱导公式:记忆口诀: 奇变偶不变,符号看象限。即k为奇数时,变形式,举例如下:
奇变偶不变,符号看象限。即k为奇数时,变形式,举例如下:
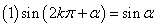 ,
,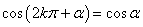 ,
, .
.
 ,
,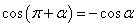 ,
, .
.
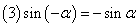 ,
, ,
, .
.
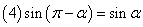 ,
, ,
,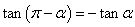 .
.
口诀:函数名称不变,符号看象限.
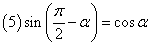 ,
, .
.
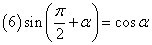 ,
,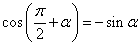 .
.
7正弦函数、余弦函数和正切函数的图象与性质



 8、三角函数公式:
8、三角函数公式:
降幂公式: 升幂公式 :
1+cos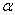 =
=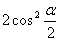 cos2
cos2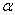

1-cos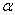 =
=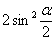 sin2
sin2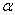

9.正弦定理 :(在△ABC中,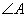 对应
对应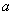 边,
边,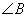 对应
对应 边,
边, 对应
对应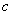 边,
边,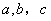 分别三边长度)
分别三边长度)
 .(R为圆外接圆半径)
.(R为圆外接圆半径)
余弦定理:
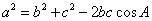 ;
;
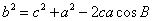 ;
;
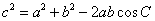 .
.
三角形第二面积公式: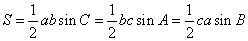 .
.
