实验二 SDS-聚丙烯酰胺凝胶电泳法
(SDS-PAGE)测定蛋白质的分子量
1 原理
1.1聚丙烯酰胺凝胶的性能及制备原理
1.1.1性能
聚丙烯酰胺凝胶的机械性能好,有弹性,透明,相对地化学稳定,对pH和温度变化比较稳定,在很多溶剂中不溶,是非离子型的,没有吸附和电渗作用。通过改变浓度和交联度,可以控制孔径在广泛的范围内变动,并且制备凝胶的重复性好。由于纯度高和不溶性,因此还适于少量样品的制备,不致污染样品。
1.1.2 制备原理
聚丙烯酰胺凝胶是用丙烯酰胺(Acr)和交联剂甲叉双丙烯酰胺(Bis)在催化剂的作用下聚合而成。聚丙烯酰胺凝胶聚合的催化系统有化学聚合和光聚合两种。本实验是用化学聚合。化学聚合的催化剂通常多采用过硫酸铵(AP)或过硫酸钾,此外还需要一种脂肪族叔胺作加速剂,最有效的加速剂是N,N,N’,N’-四甲基乙二胺(TEMED)。在叔胺的催化下,由过硫酸铵形成氧的自由基,后者又使单体形成自由基,从而引发聚合反应。叔胺要处于自由碱基状态下才有效,所以在低pH时,常会延长聚合时间;分子氧阻止链的延长,妨碍聚合作用;一些金属也能抑制聚合;冷却可以使聚合速度变慢。通常控制这些因素使聚合在1小时内完成,以便使凝胶的性质稳定。
1.1.3 凝胶浓度和交联度与孔径的关系
凝胶浓度根据被分离的物质的分子量大小确定。当分析一个未知样品时,常先用7.5%的标准凝胶或用4~10%的凝胶梯度来试测,而后选出适宜的凝胶浓度。凝胶的机械性能、弹性是否适中很重要,胶太软易断裂,;太硬则脆,也易折断。
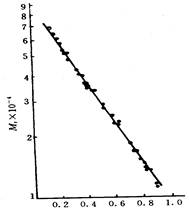
1.2 SDS-凝胶电泳法测定蛋白质分子量的原理
蛋白质分子在聚丙烯酰胺凝胶中电泳时,它的迁移率取决于所带净电荷及分子的大小和形状等因素。如果在聚丙烯酰胺凝胶系统中加入SDS和巯基乙醇,则蛋白质分子的迁移率主要取决于它的分子量,而与所带电荷和形状无关。
…… …… 余下全文