受理号:

医 疗 器 械 注 册 申 请 表
产品名称:

规格型号:

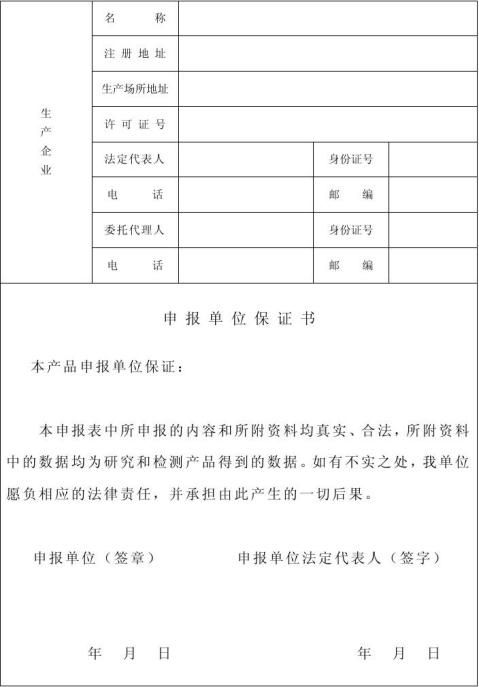
生产厂家:

成都市食品药品监督管理局
填 表 说 明
1.按照《医疗器械注册管理办法》及相关文件的规定报送资料,并在所附资料项后面的方框内划“√”。报送的资料应按本申请表规定顺序排列,并活页装订。同时每项申报材料应标明名称和顺序号。
2.本申请表应打印。填写内容应完整、清楚、整洁,不得涂改。
3.申报产品名称、规格型号应与所提交的注册产品标准、检测报告等申报材料中所用名称、规格型号一致。
4.生产者是指以自己的名义把产品推向市场,并对该产品的安全性、有效性负最终责任的单位;承产单位指受生产者委托承担产品加工制造的单位。生产场所是指产品实际加工制造的场所。
5.如申报材料中有需要特别加以说明的问题,请在本表“其它需要说明的问题”栏中说明
6.请在“注册申请应附资料及顺序”栏对应项目左侧方框内划“√”。如根据有关规定,某项材料不需提交,请在该项目左侧的方框内划“#”,并在本表“其它需要说明的问题”栏中写明理由。
7.本申请表从成都市药品监督管理局网站(WWW.CDFDA.GOV.CN)免费下载。报送注册材料时,需同时提交保存有申请表的软盘。
此栏由注册受理人员填写

以下栏目由申请者填写(填表前,请详细阅读填表说明)
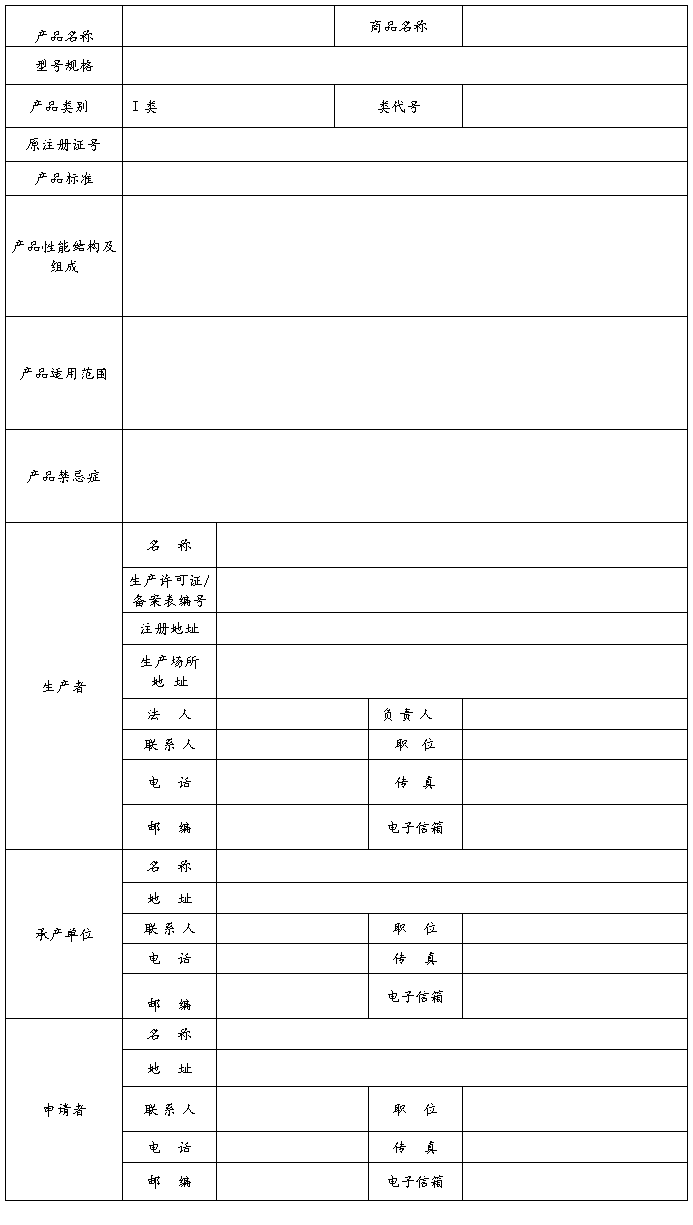
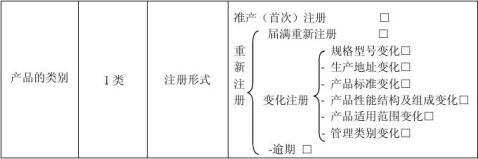
注册申请应附材料及顺序
注:请在对应项目左侧方框内划√。如根据有关规定,某项材料不需提交,请在该项目左侧的方框内划#,并在本表“其它需要说明的问题”栏中写明理由。

第二篇:医疗器械注册申请表
受理号:____________
医疗器械注册申请表
产 品 名 称: 规 格 型 号: 申请企业(盖章): 法人代表(签字): 申报日期:
此栏由注册受理人员填写
鞍山市食品药品监督管理局
填 表 说 明
1. 按照《医疗器械注册管理办法》及相关文件报送资料;报送注册材料时,需同时提交申请表的电子文档。
2. 申请表应打印,填写内容应完整、清楚、整洁,不得涂改。
3. “生产企业名称”、“生产地址”、“生产场所地址”应与《辽宁省第一类医疗器械生产企业登记表》相同。
4. 申报产品名称、规格型号应与所提交的注册产品标准、检测报告等申报材料中所用名称、规格型号一致。
5. 如申报材料中有需要特别加以说明的问题,请在本表“其他需要说明的问题”栏中说明。
6. 请在“注册申请应附资料及顺序”栏对应项目的方框内用“√”做标记。如根据有关规定,某项材料不需提交,请在方框内用“#”做标记,并在本表“其他需要说明的问题”栏中写明理由。
7. 报送资料一律采用4号字A4打印纸,资料应按本项的顺序排列,装订
成册,并在每项的第一页作一标签,按本项的规定注明该资料的编号。
8. 申请表的封面应有企业法人代表签字并加盖企业公章。