蛋 白 质 (一)名词解释
1. 两性离子(dipolarion) 2. 必需氨基酸(essential amino acid)
3. 等电点(isoelectric point,pI) 4. 稀有氨基酸(rare amino acid)
5. 非蛋白质氨基酸(nonprotein amino acid) 6. 构型(configuration)
7. 蛋白质的一级结构(protein primary structure) 8. 构象(conformation)
9. 蛋白质的二级结构(protein secondary structure) 10.结构域(domain)
11.蛋白质的三级结构(protein tertiary structure) 12.氢键(hydrogen bond)
13.蛋白质的四级结构(protein quaternary structure) 14.离子键(ionic bond)
15.超二级结构(super-secondary structure) 16.疏水键(hydrophobic bond)
17.范德华力( van der Waals force) 18.盐析(salting out)
19.盐溶(salting in) 20.蛋白质的变性(denaturation)
21.蛋白质的复性(renaturation) 22.蛋白质的沉淀作用(precipitation)
23.凝胶电泳(gel electrophoresis) 24.层析(chromatography)
(二) 填空题
1.蛋白质多肽链中的肽键是通过一个氨基酸的_____基和另一氨基酸的_____基连接而 形成的。
2.大多数蛋白质中氮的含量较恒定,平均为___%,如测得1 克样品含氮量为10mg,则 蛋白质含量为____%。
3.在20 种氨基酸中,酸性氨基酸有_________和________2 种,具有羟基的氨基酸是 ________和_________,能形成二硫键的氨基酸是__________.
4.蛋白质中的_________、___________和__________3 种氨基酸具有紫外吸收特性,因 而使蛋白质在280nm 处有最大吸收值。
5.精氨酸的pI 值为10.76,将其溶于pH7 的缓冲液中,并置于电场中,则精氨酸应向电 场的_______方向移动。
6.组成蛋白质的20 种氨基酸中,含有咪唑环的氨基酸是________,含硫的氨基酸有 _________和___________。
7.蛋白质的二级结构最基本的有两种类型,它们是_____________和______________。
8.α-螺旋结构是由同一肽链的_______和 ________间的___键维持的,螺距为______, 每圈螺旋含_______个氨基酸残基,每个氨基酸残基沿轴上升高度为_________。天
然蛋白质分子中的α-螺旋大都属于___手螺旋。
9.在蛋白质的α-螺旋结构中,在环状氨基酸________存在处局部螺旋结构中断。
10.球状蛋白质中有_____侧链的氨基酸残基常位于分子表面而与水结合,而有_______ 侧链的氨基酸位于分子的内部。
11.氨基酸与茚三酮发生氧化脱羧脱氨反应生成______色化合物,而________与茚三酮 反应生成黄色化合物。
12.维持蛋白质的一级结构的化学键有_______和_______;维持二级结构靠________键; 维持三级结构和四级结构靠_________键,其中包括________、________、________ 和_________.
13.稳定蛋白质胶体的因素是__________________和______________________。
14.GSH 的中文名称是____________,它的活性基团是__________,它的生化功能是 ____________________。
15.加入低浓度的中性盐可使蛋白质溶解度________,这种现象称为________,而加入 高浓度的中性盐,当达到一定的盐饱和度时,可使蛋白质的溶解度______并
__________,这种现象称为_______,蛋白质的这种性质常用于_____________。
16.用电泳方法分离蛋白质的原理,是在一定的pH 条件下,不同蛋白质的________、 _________和___________不同,因而在电场中移动的_______和_______不同,从而
使蛋白质得到分离。
17.氨基酸处于等电状态时,主要是以________形式存在,此时它的溶解度最小。
18.鉴定蛋白质多肽链氨基末端常用的方法有__________和_______________。
19.测定蛋白质分子量的方法有_________、____________和__________________。
20.今有甲、乙、丙三种蛋白质,它们的等电点分别为8.0、4.5 和10.0,当在pH8.0 缓冲 液中,它们在电场中电泳的情况为:甲_______,乙_______,丙________。
21.当氨基酸溶液的pH=pI 时,氨基酸以_____离子形式存在,当pH>pI 时,氨基酸以 _______离子形式存在。
+22.谷氨酸的pK1(α-COOH)=2.19, pK2 (α-NH3) = 9.67, pKR(R 基)= 4.25,谷氨酸的
等电点为__________。
23.天然蛋白质中的α螺旋结构,其主链上所有的羰基氧与亚氨基氢都参与了链内 _____键的形成,因此构象相当稳定。
24.将分子量分别为a(90 000)、b(45 000)、c(110 000)的三种蛋白质混合溶液进 行凝胶过滤层析,它们被洗脱下来的先后顺序是_____________。
25.肌红蛋白的含铁量为0.34%,其最小分子量是______.血红蛋白的含铁量也是0.34%, 但每分子含有4 个铁原子,血红蛋白的分子量是________.
26.一个α-螺旋片段含有180 个氨基酸残基,该片段中有_____圈螺旋?该α-螺旋片 段的轴长为_____.
(三) 选择题
1.在生理pH 条件下,下列哪种氨基酸带正电荷?
A.丙氨酸 B.酪氨酸 C.赖氨酸 D.蛋氨酸 E.异亮氨酸
2.下列氨基酸中哪一种是非必需氨基酸?
A.亮氨酸 B.酪氨酸 C.赖氨酸 D.蛋氨酸 E.苏氨酸
3.蛋白质的组成成分中,在280nm 处有最大吸收值的最主要成分是:
A.酪氨酸的酚环 B.半胱氨酸的硫原子 C.肽键 D.苯丙氨酸
4.下列4 种氨基酸中哪个有碱性侧链?
A.脯氨酸 B.苯丙氨酸 C.异亮氨酸 D.赖氨酸
5.下列哪种氨基酸属于亚氨基酸?
A.丝氨酸 B.脯氨酸 C.亮氨酸 D.组氨酸
6.下列哪一项不是蛋白质α-螺旋结构的特点?
A.天然蛋白质多为右手螺旋
B.肽链平面充分伸展
C.每隔3.6 个氨基酸螺旋上升一圈。
D.每个氨基酸残基上升高度为0.15nm.
7.下列哪一项不是蛋白质的性质之一?
A.处于等电状态时溶解度最小 B.加入少量中性盐溶解度增加
C.变性蛋白质的溶解度增加 D.有紫外吸收特性
8.下列氨基酸中哪一种不具有旋光性?
A.Leu B.Ala C.Gly D.Ser E.Val
9.在下列检测蛋白质的方法中,哪一种取决于完整的肽链?
A.凯氏定氮法 B.双缩尿反应 C.紫外吸收法 D.茚三酮法
10.下列哪种酶作用于由碱性氨基酸的羧基形成的肽键?
A.糜蛋白酶 B.羧肽酶 C.氨肽酶 D.胰蛋白酶
11.下列有关蛋白质的叙述哪项是正确的?
A.蛋白质分子的净电荷为零时的pH 值是它的等电点
B.大多数蛋白质在含有中性盐的溶液中会沉淀析出
C.由于蛋白质在等电点时溶解度最大,所以沉淀蛋白质时应远离等电点
D.以上各项均不正确
12.下列关于蛋白质结构的叙述,哪一项是错误的?
A.氨基酸的疏水侧链很少埋在分子的中心部位
B.电荷的氨基酸侧链常在分子的外侧,面向水相
C.白质的一级结构在决定高级结构方面是重要因素之一
D.白质的空间结构主要靠次级键维持
13.列哪些因素妨碍蛋白质形成α-螺旋结构?
A.脯氨酸的存在 B.氨基酸残基的大的支链
C.碱性氨基酸的相邻存在 D.酸性氨基酸的相邻存在
E.以上各项都是
14.于β-折叠片的叙述,下列哪项是错误的?
A.β-折叠片的肽链处于曲折的伸展状态
B.β-折叠片的结构是借助于链内氢键稳定的
C.有的β-折叠片结构都是通过几段肽链平行排列而形成的
D.基酸之间的轴距为0.35nm
15.持蛋白质二级结构稳定的主要作用力是:
A.盐键 B.疏水键 C.氢键 D.二硫键
16.维持蛋白质三级结构稳定的因素是:
A.肽键 B.二硫键 C.离子键 D.氢键 E.次级键
17.凝胶过滤法分离蛋白质时,从层析柱上先被洗脱下来的是:
A.分子量大的 B.分子量小的 C.电荷多的 D.带电荷少的
18. 下列哪项与蛋白质的变性无关?
A. 肽键断裂 B.氢键被破坏 C.离子键被破坏 D.疏水键被破坏
19.蛋白质空间构象的特征主要取决于下列哪一项?
A.多肽链中氨基酸的排列顺序 B.次级键 C.链内及链间的二硫键 D.温度及pH
20.下列哪个性质是氨基酸和蛋白质所共有的?
A.胶体性质 B.两性性质 C.沉淀反应 D.变性性质
E.双缩脲反应
21.氨基酸在等电点时具有的特点是:
A.不带正电荷 B.不带负电荷
C.A 和B D.溶解度最大
E.在电场中不泳动
22.蛋白质的一级结构是指:
A.蛋白质氨基酸的种类和数目 B.蛋白质中氨基酸的排列顺序
C.蛋白质分子中多肽链的折叠和盘绕 D.包括A,B 和C
(四) 是非判断题
( ) 1.氨基酸与茚三酮反应都产生蓝紫色化合物。
( ) 2.因为羧基碳和亚氨基氮之间的部分双键性质,所以肽键不能自由旋转。
( ) 3.所有的蛋白质都有酶活性。
( ) 4.α-碳和羧基碳之间的键不能自由旋转。
( ) 5.多数氨基酸有D-和L-两种不同构型,而构型的改变涉及共价键的破裂。
( ) 6.所有氨基酸都具有旋光性。
( ) 7.构成蛋白质的20 种氨基酸都是必需氨基酸。
( ) 8.蛋白质多肽链中氨基酸的排列顺序在很大程度上决定了它的构象。
( ) 9.一氨基一羧基氨基酸的pI 为中性,因为-COOH 和-NH2 的解离度相同。
( ) 10.蛋白质的变性是蛋白质立体结构的破坏,因此涉及肽键的断裂。
( ) 11.蛋白质是生物大分子,但并不都具有四级结构。
( ) 12.血红蛋白和肌红蛋白都是氧的载体,前者是一个典型的变构蛋白,在与氧结合 过程中呈现变构效应,而后者却不是。
( ) 13..用FDNB 法和Edman 降解法测定蛋白质多肽链N-端氨基酸的原理是相同的。
( ) 14.并非所有构成蛋白质的20 种氨基酸的α-碳原子上都有一个自由羧基和一个自 由氨基。
( ) 15.蛋白质是两性电解质,它的酸碱性质主要取决于肽链上可解离的R 基团。
( ) 16.在具有四级结构的蛋白质分子中,每个具有三级结构的多肽链是一个亚基。
( ) 17.所有的肽和蛋白质都能和硫酸铜的碱性溶液发生双缩尿反应。
( ) 18.一个蛋白质分子中有两个半胱氨酸存在时,它们之间可以形成两个二硫键。
( ) 19.盐析法可使蛋白质沉淀,但不引起变性,所以盐析法常用于蛋白质的分离制备。
( ) 20.蛋白质的空间结构就是它的三级结构。
( ) 21.维持蛋白质三级结构最重要的作用力是氢键。
( )22.具有四级结构的蛋白质,它的每个亚基单独存在时仍能保存蛋白质原有的生物 活性。
( )23.变性蛋白质的溶解度降低,是由于中和了蛋白质分子表面的电荷及破 坏了外层 的水膜所引起的。
( )24.蛋白质二级结构的稳定性是靠链内氢键维持的,肽链上每个肽键都参与氢键的形成。
(五)问答题
1.什么是蛋白质的一级结构?为什么说蛋白质的一级结构决定其空间结构?
2.什么是蛋白质的空间结构?蛋白质的空间结构与其生物功能有何关系?
3.蛋白质的α螺旋结构有何特点?
4.蛋白质的β折叠结构有何特点?
5.举例说明蛋白质的结构与其功能之间的关系。
6.什么是蛋白质的变性作用和复性作用?蛋白质变性后哪些性质会发生改变?
7.简述蛋白质变性作用的机制。
8.蛋白质有哪些重要功能
9.下列试剂和酶常用于蛋白质化学的研究中:CNBr、异硫氰酸苯酯、丹黄酰氯、脲、 6mol/L HCl、β-巯基乙醇、水合茚三酮、过甲酸、胰蛋白酶、胰凝乳蛋白酶。其中哪 一个最适合完成以下各项任务?
(1)测定小肽的氨基酸序列。
(2)鉴定肽的氨基末端残基。
(3)不含二硫键的蛋白质的可逆变性;如有二硫键存在时还需加什么试剂?
(4)在芳香族氨基酸残基羧基侧水解肽键。
(4)在蛋氨酸残基羧基侧水解肽键。
(5)在赖氨酸和精氨酸残基羧基侧水解肽键。
10.根据蛋白质一级氨基酸序列可以预测蛋白质的空间结构。假设有下列氨基酸序列: Ile-Ala-His-Thr-Tyr-Gly-Pro-Glu-Ala-Ala-Met-Cys-Lys-Try-Glu-Ala-Gln-Pro-Asp-Gly-Met-Glu-Cys-Ala-Phe-His-Arg
(1)预测在该序列的哪一部位可能会出弯或β-转角。
(2)何处可能形成链内二硫键?
(3)假设该序列只是大的球蛋白的一部分,下面氨基酸残基中哪些可能分布在蛋白 的外表面,哪些分布在内部?
天冬氨酸;异亮氨酸;苏氨酸;缬氨酸;谷氨酰胺;赖氨酸
第二篇:蛋白质化学练习题及参考答案
-第一章 蛋白质化学 测试题--
一、单项选择题
1.测得某一蛋白质样品的氮含量为0.40g,此样品约含蛋白质多少?
A.2.00g B.2.50g C.6.40g D.3.00g E.6.25g
2.下列含有两个羧基的氨基酸是:
A.精氨酸 B.赖氨酸 C.甘氨酸 D.色氨酸 E.谷氨酸
3.维持蛋白质二级结构的主要化学键是:
A.盐键 B.疏水键 C.肽键 D.氢键 E.二硫键
4.关于蛋白质分子三级结构的描述,其中错误的是:
A.天然蛋白质分子均有的这种结构 B.具有三级结构的多肽链都具有生物学活性 C.三级结构的稳定性主要是次级键维系 D.亲水基团聚集在三级结构的表面 E.决定盘曲折叠的因素是氨基酸残基
5.具有四级结构的蛋白质特征是:
A.分子中必定含有辅基 B.在两条或两条以上具有三级结构多肽链的基础上,肽链进一步折叠,盘曲形成 C.每条多肽链都具有独立的生物学活性 D.依赖肽键维系四级结构的稳定性 E.由两条或两条以上具在三级结构的多肽链组成
6.蛋白质所形成的胶体颗粒,在下列哪种条件下不稳定:
A.溶液pH值大于pI B.溶液pH值小于pI C.溶液pH值等于pI D.溶液pH值等于
7.4 E.在水溶液中
7.蛋白质变性是由于:
A.氨基酸排列顺序的改变 B.氨基酸组成的改变 C.肽键的断裂 D.蛋白质空间构象的破坏E.蛋白质的水解
8.变性蛋白质的主要特点是:
A.粘度下降 B.溶解度增加 C.不易被蛋白酶水解 D.生物学活性丧失 E.容易被盐析出现沉淀
9.若用重金属沉淀pI为8的蛋白质时,该溶液的pH值应为:
A.8 B.>8 C.<8 D.≤8 E.≥8
10.蛋白质分子组成中不含有下列哪种氨基酸?
A.半胱氨酸 B.蛋氨酸 C.胱氨酸 D.丝氨酸 E.瓜氨酸
二、多项选择题(在备选答案中有二个或二个以上是正确的,错选或未选全的均不给分)
1.含硫氨基酸包括: A.蛋氨酸 B.苏氨酸 C.组氨酸 D.半胖氨酸
2.下列哪些是碱性氨基酸: A.组氨酸 B.蛋氨酸 C.精氨酸 D.赖氨酸
3.芳香族氨基酸是: A.苯丙氨酸 B.酪氨酸 C.色氨酸 D.脯氨酸
4.关于α-螺旋正确的是:
A.螺旋中每3.6个氨基酸残基为一周 B.为右手螺旋结构
C.两螺旋之间借二硫键维持其稳定 D.氨基酸侧链R基团分布在螺旋外侧
5.蛋白质的二级结构包括:
A.α-螺旋 B.β-片层 C.β-转角 D.无规卷曲
6.下列关于β-片层结构的论述哪些是正确的:
A.是一种伸展的肽链结构 B.肽键平面折叠成锯齿状 C.也可由两条以上多肽链顺向或逆向平行排列而成 D.两链间形成离子键以使结构稳定
7.维持蛋白质三级结构的主要键是:
A.肽键 B.疏水键 C.离子键 D.范德华引力
8.下列哪种蛋白质在pH5的溶液中带正电荷?
A.pI为4.5的蛋白质 B.pI为7.4的蛋白质 C.pI为7的蛋白质D.pI为6.5的蛋白质
9.使蛋白质沉淀但不变性的方法有:
A.中性盐沉淀蛋白 B.鞣酸沉淀蛋白 C.低温乙醇沉淀蛋白 D.重金属盐沉淀蛋白
10.变性蛋白质的特性有:
A.溶解度显著下降 B.生物学活性丧失 C.易被蛋白酶水解 D.凝固或沉淀
三、填空题
1.组成蛋白质的主要元素有_________,________,_________,_____ , ____。
2.不同蛋白质的含________量颇为相近,平均含量为________%。
3.蛋白质具有两性电离性质,大多数在酸性溶液中带______电荷,在碱性溶液中带_______电荷。当蛋白质处在某一pH值溶液中时,它所带的正负电荷数相待,此时的蛋白质成为 _________,该溶液的pH值称为蛋白质的__________。
4.蛋白质的基本组成单位是_________,有_________种。
5.在蛋白质分子中,一个氨基酸的α碳原子上的________与另一个氨基酸α碳原子上的________脱去一分子水形成的键叫________,它是蛋白质分子中的基本结构键。
6.蛋白质颗粒表面的_________和_________是蛋白质亲水胶体稳定的两个因素。
7.蛋白质变性主要是因为破坏了维持和稳定其空间构象的各种_________键,使天然蛋白质原有的________与________性质改变。
8.按照组成分分类,蛋白质分子组成中仅含氨基酸的称_______,分子组成中除了蛋白质部分还有非蛋白质部分的称_________,其中非蛋白质部分称_________。
9、维持蛋白质三级结构的主要键是_________,_________,_________,_________。
四、名词解释
1、蛋白质的一级结构、蛋白质的二级结构、蛋白质的三级结构、蛋白质的四级结构
2、蛋白质的等电点
3、肽单元(肽键平面)
五、简答题
1、举例说明蛋白质的一级结构与功能的关系,空间结构与功能的关系。
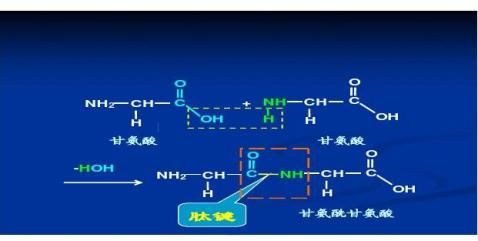
2、写出二肽的形成过程。
参考答案
一、单项选择题
1.B 2.E 3.D 4.B 5.E 6.C 7.D 8.D 9.B 10.E
二、多项选择题
1.AD 2.ACD 3.ABD 4.ABD 5.ABCD
6.ABC 7.BCD 8.BCD 9.AC 10.ABC
三、填空题
1.碳 氢 氧 氮 硫2.氮 16 3.正 负 两性离子(兼性离子) 等电点4.氨基酸 20
5.氨基 羧基 肽键6.水化膜 电荷层(或同性电荷的排除作用)7.次级键 生物学活性 理化性质
8.单纯蛋白质 结合蛋白质 辅基 9.疏水作用 盐键(或离子键) 氢键 范德华力
四、名词解释()
五、简答题
1、举例说明蛋白质的一级结构与功能的关系,空间结构与功能的关系。
一级结构和功能密切相关。一级结构相似其功能也相似,一级结构不同其功能也不同。一级结构发生改变则蛋白质功能也发生改变。如:
(1)核糖核酸酶一级结构与功能的关系,二硫键破坏后,生物学活性丧失。
(2)胰岛素一级结构与功能的关系 若将A链N端的第1个氨基酸残基切去,其活性只剩2%~10%,再将第2~4位氨基酸残基切去,其活性完全丧失。若将A、B两链间的二硫键还原,A、B两链即分离,胰岛素的功能完全消失。若将B链第28~30位氨基酸残基切去,其活性仍能维持100%。
(3)血红蛋白一级结构与功能的关系 镰刀形红细胞性贫血患者的血红蛋白其α--链与正常人的血红蛋白完全相同,所不同的是β—链N端第六位正常人为谷氨酸而镰刀形红细胞性贫血患者的为缬氨酸,仅此一个氨基酸的改变,就造成红细胞变形成为镰刀状,带氧能力低,极易破碎,产生贫血。
空间结构与功能也密切相关。空间结构发生改变,其功能活性也随之改变。如:
(1).血红蛋白空间结构与功能的关系 Hb未结合O2时,4个亚基结构紧密,此时Hb对氧亲和力低;随着O2 的结合,空间结构发生变化,使结构相对松弛,此时Hb对氧亲合力高,是Hb结合O2 的形式。
(2)、朊病毒蛋白空间结构与功能的关系 例:疯牛病中的蛋白质构象改变,疯牛病是由朊病毒蛋白引起的一组人和动物神经退行性病变。正常PrP富含α-螺旋,称为PrPc。在某种未知蛋白质作用下转变成为β-折叠的PrPsc,从而致病。
2、写出二肽的形成过程。如2个甘氨酸形成二肽的过程: