酵母核糖核酸的提取及测定
植物098 原硕 0901080808
摘要:用浓盐法提取酵母RNA,经过多步分离提纯,在现有实验条件下,得到样本RNA含量=67.5%,RNA提取率=1.2%
关键字:酵母,浓盐法,RNA含量,提取及测定
一、 研究背景及目的:
RNA作为细胞中参与基因表达和蛋白质合成的重要物质,在平时学习中多有涉及,本实验通过从酵母中提取RNA,掌握提制RNA的方法并掌握其测定手段,巩固离心机和紫外分光光度计的使用。
二、 研究依据及原理:
酵母作为工业上大量生产核酸的最为理想的微生物,因为酵母核酸中主要是RNA(2.67~10.0%),DNA很少(0.03~0.516%),菌体容易收集,RNA也易于分离。此外,抽提后的菌体蛋白质,也具有很高的利用价值。
RNA提取过程是先使RNA从细胞中释放,并使它和蛋白质分离,然后将菌体除去,再根据核酸在等电点溶解度最小的性质,将pH调到2.0~2.5使RNA沉淀,进行离心收集。
提取RNA的方法很多,在工业生产上常用的是稀碱性和浓盐法。
本实验采取浓盐法(10%NaCl)
核酸不论是DNA还是RNA,都是由核苷酸组成的多聚核苷酸化合物,而核苷酸是由糖,碱基和磷酸构成。
要测定生物体内核酸的含量或者测定提取出来的核酸含量,只需要测定组成核苷酸的一种成分,如磷,糖或碱基,便可计算出核糖的含量,因为核算分子中这三个组份是以等分子比例存在的,即每一个嘌呤或嘧啶分子都与一分子戊糖及一分子磷酸相连接的,所以只要测出其中任何一组分的含量即可求出核糖的含量。
本实验采用紫外吸收法测定核糖核酸含量,因为核酸的组成成分嘌呤及嘧啶碱基具有强烈的紫外吸收,最大吸收在260mm处,利用此特性可以对核酸进行定量测定。
三、 实验材料与方法:
1、 材料:干酵母(安琪牌)
灰蓝色pH试纸和黄色pH试纸
2、 试剂:
(1)10%NaCl
(2)6NHCl
(3)95%乙醇(分析纯)
(4)5~6%的氨水
(5)RNA沉淀剂
取0.5克钼酸铵,加水193ml,加7ml 70%过氯酸,总体积200ml。(70%过氯酸即高氯酸,原液浓度即是70%)。
3、 仪器:
(1) 量筒:50ml;具塞试管:15ml×2
(2) 三角瓶:100ml;容量瓶:25ml×1,50ml×2
(3) 烧杯:50ml×3
(4) 表面皿:6cm×1
(5) 滴管,玻棒,移液器,塑料碗
(6) 烘箱
(7) 离心机
(8) 托盘天平,分析天平
(9) 匀浆器
(10) 紫外分光光度计(Rayleigh,UV-9600)
4、 实验方法:
1) 提取:称取7g酵母,研钵中研磨成粉末,倒入三角瓶中,然后量取50ml 10%NaCl溶液,倒入三角瓶,是酵母粉充分彻底悬浮,之后小心放入沸水浴中,浸提半小时。
2) 分离:将上述提取液取出,于冰浴中彻底冷却,转入离心管,以3500r/min离心30min。使提取液及菌体残渣等分离。
3) 沉淀RNA:将离心得到的上清液,小心倾倒于50ml小烧杯中,并置于冰浴中冷却,待溶液冷却至10℃以下后,于冰浴中在搅拌下(注意不要过分剧烈)小心用6MHCl调节pH至2.0~2.5(用灰蓝色pH试纸),调好后继续于冰水中放置10min。
4) 洗涤纯化:将上述悬浊液小心转入离心管,以3000r/min离心10min,得到RNA沉淀。小心倾去上清液,直接与离心管中用95%乙醇洗涤RNA沉淀两次,每次用15ml乙醇,充分搅拌洗涤,然后以3500r/min离心6min。
5) 干燥:用牛角勺仔细将洗涤后的RNA沉淀从离心管内挖出涂于事先将边缘折起成框的称量纸上(预先用分析天平称重并记录数据),涂布均匀后,小心置于80℃烘箱内5min左右,使沉淀充分干燥。将干燥后的RNA制品连同称量纸一起准确称重,而后小心将RNA制品的大部分转移至匀浆器中,将称量纸和残余RNA制品再次称重,记录下所有数据。
6) 含量测定(紫外分光光度法):采用比消光系数法,比消光系数本实验中给定A260=0.022。
测定步骤:
将第5步中得到的溶液,转入小烧杯中,用5%氨水小心调pH至7.0(用黄色pH试纸),最后转入25ml容量瓶,用蒸馏水定容。
取两支试管,按下表操作:
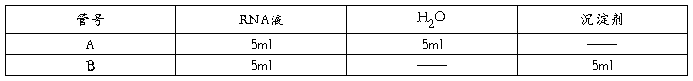
摇匀,冰浴20min,转入离心管3500r/min离心10min,小心取上清液,各取0.5ml至50ml容量瓶,蒸馏水定容,其中一个做标准空白液,在紫外分光光度计上测定OD260值。
四、 实验结果及计算:
1) 原始数据:
称取酵母量(样品重)W=7g
空白称量纸重 W1=0.6048g
总制品+纸重 W2=0.7282g
残余制品+纸重 W3=0.6198g
比消光系数 A260=0.022
测定消光值 OD260=0.322
透光度T=47.6%
2) 推演数据:
总制品重:G1=0.1234g
定量样品重:G2=0.1084g
3) 结果计算:
(1) RNA含量(%)=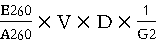 ×100%=67.5%
×100%=67.5%
V:被测样品体积
D:样品测定时的稀释倍数
(2) RNA提取率(%)=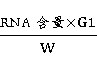 ×100%=1.2%
×100%=1.2%
五、 结果分析:
本实验使用浓盐法和紫外分光光度法提取和测定了酵母的核糖核酸含量。
实验中,有如下几处可能产生误差,1、研磨时的充分程度,研磨的充分程度的不同,将直接影响最后所能提取到的RNA含量的多少。2、本实验过程中,多次涉及到样品转移、离心、洗涤过程中,将不可避免的造成样品的损失,直接造成最终RNA提取率的下降。3、实验操作过程中,实验人员并未佩戴手套,人体附带的RNase一类的酶可能会造成一定量的RNA分解。4、烘干后的RNA样品很轻,在称量、转移过程中很容易造成损失。
综上所述,本实验中一定未能提取出酵母的全部RNA,实验过程中必然造成了样品一定程度上的损失,参考酵母RNA含量(2.67~10.0%),以及在A260/A280=1.983时,90g湿酵母(相当于20g干酵母)可提取1gRNA(选自:李志东 邱峰 张洪林,《影响浓盐法提取啤酒酵母RNA的工艺参数研究》,《化工技术与开发》20##年第36卷第2期,12页36卷),考虑到本实验的实验条件及上面提到的误差因素,本实验结果在RNA含量和RNA提取率上都基本让人满意。
六、 参考文献:
1、 李良秋 黄晓兰,《高效液相色谱法测定酵母RNA中四种生物碱基的含量》,第二届全国发酵工程学术讨论会第二届全国发酵工程学术讨论会论文集,1998年
2、 徐希柱,《啤酒酵母中RNA、β-(1,3)-D-葡聚糖和蛋白质的提取及应用研究》,《山东农业大学》 20##年
3、 田宝勇 赵星洁,《啤酒酵母RNA降解产物5′-核苷酸的高效液相色谱分析》,《酿酒科技》,20##年第3期
4、 李珊 吴振强,《盐法提取啤酒废酵母RNA的研究》,《酿酒科技》20##年第7期
5、 朱俊东 黄国荣 糜漫天 郎海滨,《啤酒酵母中提取核糖核酸的研究》, 《食品科学》160 2006, Vol. 27, No. 02
6、 廖鲜艳 李永仙 等,《啤酒酵母胞内RNA提取的研究》,《酿酒》20##年第29卷第2期
7、 李志东 邱峰 张洪林,《影响浓盐法提取啤酒酵母RNA的工艺参数研究》,《化工技术与开发》20##年第36卷第2期
8、 曹成喜 等,《生物化学仪器分析基础》,2008,化学工业出版社
9、 孙培龙 吴石金,《生物化学技术实验指导》,2008,化学工业出版社
10、 张龙翔 张庭芳 李玲媛,《生化试验方法和技术》,1997,高等教育出版社
七、 思考题:
1、 RNA中的嘌呤碱基和嘧啶碱基在不同pH条件下异构情况不同,对紫外光的吸收值不同,摩尔消光系数会随之改变。所以应固定pH值;pH不固定会影响测定结果。因为pH不同的条件下,OD值也会随之改变,而实验中所给的比消光系数是在一定pH值下给定的。所以pH值不固定会影响测定结果。
2、 1)加钼酸铵—过氯酸沉淀剂是为了沉淀RNA,然后用得到的上清液做空白对照,以减少定量样品重的蛋白质、糖类等物质对RNA含量测定的干扰;2)由朗博—比尔定律A=εbc,当吸光度在0.2~0.8时,测量误差最小,本实验中ε、b都已固定,只能改变浓度c,是A在上述范围内,所以要稀释。
3、 1)总体策略:保持物质活性,结构完整,纯化到所需浓度,能够大量提纯(量产);2)分离纯化生命大分子时要注意:保持所提取物质活性;抑制或避免接触所能分解被提纯物质的酶,以免物质被酶分解;反应条件应温和,避免能破坏生命大分子的因素。
八、 实验小结:
酵母作为工业上大量生产核酸的最为理想的微生物,因为酵母核酸中主要是RNA,DNA很少,菌体容易收集,RNA也易于分离。因而本实验使用浓盐法和紫外分光光度法提取和测定了酵母的核糖核酸含量。
实验过程中,通过浓盐法提取出样品酵母中的RNA,经过多次分离提纯,最后用紫外分光光度发,通过吸光率,测定了样品中的RNA含量。计算出RNA提取率。
实验中从在几处误差,使得实验数据在现有条件下不可避免偏低,但参考酵母RNA标准范围(2.67~10.0%),以及在A260/A280=1.983时,90g湿酵母(相当于20g干酵母)可提取1gRNA(选自:李志东 邱峰 张洪林,《影响浓盐法提取啤酒酵母RNA的工艺参数研究》,《化工技术与开发》20##年第36卷第2期,12页36卷),实验结果基本让人满意。
通过实验,我们更充分的理解了浓盐法提取RNA的原理,加深了对RNA相关性质的理解,对其含量有了一定的感性认识。
第二篇:实验三 酵母核糖核酸的提取及测定(预习报告)
生物化学实验预习报告
实验三 酵母核糖核酸的提取及测定
一、研究背景
RNA(核糖核酸)普遍存在于动物、植物、微生物及某些病毒和噬菌体内,是遗传信息的载体,由数量不等的核糖核苷酸通过磷酸二酯键连接而成。由于RNA在细胞内能够行使各种各样的生物功能,属酸性高分子化合物,参与蛋白质生物合成,调控基因表达,作为核酶催化生化反应活性,对维持生物体的正常发育有着重要作用。此外,由于RNA还具有较强的保湿性、抗氧化性、强烈的紫外光吸收性、天然助长性以及抗皱防衰、防病治癌等特殊功能,[1]人们在研究基础理论的同时逐渐开始对RNA制剂的开发及应用进行探索。RNA制剂是以RNA及其衍生物为材料,经加工制成的产品,主要包括从富含RNA的生物体中的提取物、自溶物或者降解产物加工制成的各种商品。目前,人们已经开始逐渐接受含RNA制剂的各种产品,需求量日益攀升,RNA制剂已广泛应用于医药、食品、农业、日化、环境保护等方面,具有广阔的商业前景,形成了一大新兴产业。但不管是理论研究还是实际应用,都面临一个问题:RNA往往与细胞内的其他化合物混在一起,离体之后稳定性差、含量低,采用廉价、合适的手段分离纯化得到RNA显得至关重要。当然,人们已经摸索出来了多种多样的方法,这些方法各有特点,但其基本的思路和程序大致相似,基本战略也是有规律可循的。另外,近年来RNA试剂盒的出现使方便、快速提取纯度高、完整性好的RNA分子也实现了可能。
二、研究目标
1.了解RNA制剂开发应用的前景和基本思路;
2.掌握RNA分离纯化的设计思想及主要的操作细节;
3.学习酵母RNA提取和测定的操作方法。
三、研究策略
1.选材
即选取富含RNA的生物材料,微生物由于其原料易获得性被广泛应用于工业上大量生产RNA的原料。
2.提取
提取RNA的方法有很多种,如浓盐法、稀碱法、混合盐法、苯酚法、表面活性剂法等[2],但在工业生产上应用最多的还是稀碱法和浓盐法。两种方法的原理不同,浓盐法是原理是在加热条件下,高浓度NaCl改变细胞膜的通透性,使RNA释放出来;稀碱法是利用碱使微生物的细胞壁溶解,释放RNA。两种方法各有特点,浓盐法的破壁率低,但提取的RNA纯度比稀碱法要高;稀碱法的破壁效果好,消耗时间短,能耗低,但提取RNA纯度较低,适于工业化生产。在实际中应根据具体情况及要求选择合适的方法。
3.提纯
提纯过程中常需要去除的杂质是蛋白质。通常采用等电沉淀法使RNA沉淀出来,使其与杂质分离,但有资料显示该法不能有效分离RNA和蛋白质,且RNA损失率较高。另外,也可使用盐析法、等电沉淀法析出蛋白质或蛋白酶降解法除去蛋白质。
4.含量测定
测定RNA的含量可通过测定核糖核苷酸的糖、碱基或者磷酸来实现。目前有三种方法,定磷法、戊糖测定法和紫外吸收法。定磷比色法准确、微量、快速,是测定RNA含量的最好方法;戊糖测定法通过糖的颜色反应测定RNA,简单、快速,当样品中有粘多糖和蛋白质存在时会有干扰;紫外吸收法简单、快速、微量,但易受到蛋白质及含有共轭双键物质的干扰。
四、研究方案及可行性分析
本实验以食品用干酵母粉为材料,采用浓盐法提取核糖核酸并用紫外分光光度法测定制品中RNA的含量。方案合理,实验材料及器具实验室均可提供,时间上也允许,故本方案具有可行性。
五、具体实验设计
1.实验仪器及试剂
仪器:UV9600紫外分光光度计、JP-100架盘药物天平、恒温水浴锅、TDL-40B低速离心机;
器具:微量可调手动移液器、普通大试管、25ml容量瓶、50ml容量瓶、研钵;
试剂:10%NaCl溶液、6M HCl、95%乙醇、2%的氨水、RNA沉淀剂、蒸馏水;
材料:食品用干酵母粉。
2.实验步骤
(1)酵母核糖核酸的提取(7h)
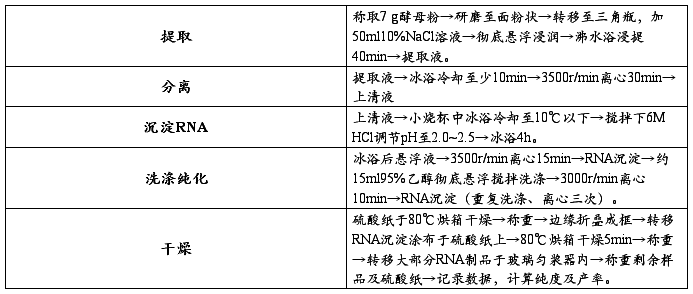
(2)核糖核酸含量的测定(紫外分光光度法)(1h)
1匀浆液制备(15min)
玻璃匀浆器内加入5ml蒸馏水→匀浆至均一的胶体溶液→转入小烧杯(10ml左右蒸馏水分次清洗并入)→混匀,2%氨水调pH7.0→转入25ml容量瓶,定容,混匀
2含量测定(40min)
取两支试管,按下表操作
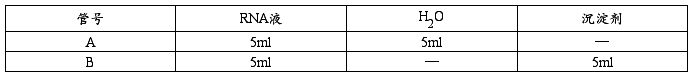
A、B管混匀→冰浴20min→3500r/min离心10min→取上清液于两支试管→各0.5ml至两个50ml容量瓶,定容,混匀→测定样品OD260值。
(3)原始数据记录处

(4)结果计算公式
1制品纯度(%)= ×定量样品稀释倍数×
×定量样品稀释倍数× ×100%
×100%
2产率:RNA提取率(%)=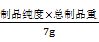 ×100%
×100%
3.实验所需时间预计
本实验共需时间约8h。
4.某些试剂与操作的作用
(1)10%NaCl溶液 破除酵母菌细胞壁,释放RNA。查阅资料显示NaCl浓度为8%~10%时RNA溶液的纯度及提取率较高。
(2)沸水浴浸提 对破除酵母菌细胞壁起促进作用。破壁时的温度对RNA提取率有很大的影响,温度越高,越有利于细胞壁的破坏,胞内物质(包括蛋白质和核酸)释放的也越多。考虑到生产应用的方便性及可操作性,温度不超过100 ℃。
(3)6M HCl调节pH至2.0~2.5 在核酸的等电点下使其尽可能多的沉淀,达到与杂质分离的目的。
(4)2%氨水调pH7.0 中性pH条件下使RNA尽可能多的溶解,从而使RNA含量测定更准确。
(5)测定OD260值之前将上清液稀释100倍 高浓度有可能超出朗伯-比尔范围,使测定结果偏差较大,稀释后测定反而更准确。
5.误差分析
(1)整个实验中搅拌过程一定要缓慢,否则会使RNA机械破碎,影响含量测定。
(2)调节等电点时应严格控制pH。因为pH过低会使核酸发生酸性水解,过高则核酸沉淀不完全,且会使杂质(DNA或蛋白质等)沉淀较多。
(3)紫外法测定RNA含量时,第一次定容要格外小心,切勿超过总体积(容量瓶量程小,只有25ml)。
六、质疑及相关思考
1.查阅资料了解到酵母的浓度以及水浴浸提时间都会对RNA的提取率有一定的影响,大部分人得出的最适酵母浓度为10%左右(与本实验相差不大),而浸提时间则从2~5h不等(与本实验40min差距较大),[3]本实验浸提时间的设置是出于什么考虑?
2.等电沉淀法析出RNA时蛋白质及DNA等杂质有多少没有被除去(一起留在了沉淀里)?我们知道,RNA的等电点为2.0~2.5,DNA等电点为4~4.5,蛋白质等电点就变化很大了,我们在保证RNA析出量最多的前提下,肯定会有部分的DNA及蛋白质杂质析出,从而对RNA含量测定造成干扰。既然如此,这些杂质对RNA含量测定的影响有多大?是否可以忽略?
3.本实验测定的是变性之后的RNA含量。我们知道,核酸变性后氢键和碱基堆积力受到破坏,使紫外吸收值升高,该现象称为增色效应。既然如此,我们在260nm波长下测定的就不是酵母菌细胞RNA分子的含量。
4.经酸性乙醇沉淀的RNA,离心之后,沉积在离心杯的底部。由于沉淀较多,用95%乙醇洗涤时肯定会不充分,很多杂蛋白不易除去,形成很多粘团,使得下面的干燥也不易操作。如果充分洗涤杂蛋白必须搅拌,这样会使RNA 被机械破碎,影响含量测定。有实验显示用苯酚-氯仿抽提法具有较好的效果,[4]由于酚-氯仿在水溶液中抽提蛋白,作用充分,又不用剧烈振荡,避免了RNA被机械切割,蛋白质又能充分去除,分离得到的RNA样品纯度较高。
5.关于紫外法测定RNA含量时的空白组设置。测定RNA含量时设置了A、B两个管,分别加入蒸馏水及等量的沉淀剂,B管的作用是沉淀RNA,作为对照。应该以蒸馏水作为空白组,分别测定A、B两个管的OD260值,B管测定值表示除RNA以外物质的吸光度值,A管测定值表示RNA及其他物质的总吸光度值,以二者之差作为RNA的吸光度值。
七、思考题
1.作为商品开发,我们更多的是应该考虑市场需求的共性还是个性?为什么?相应的,如何完成相关欲开发产品的定位?
更多考虑的是市场需求的共性。共性商品面向大众,存在广阔的市场需求,具有商业前景,一旦该产品成功投入市场就可以从中挖掘出巨大的经济效益;相反,个性产品只适用于小部分人群,需求量少。若要完成相关与开发产品的定位,就需要进行市场调查,分以下几个方面:(1)调查该产品的市场需求量和供应量,分析确定该产品目前有没有空余市场,以合理设计该产品的产量;(2)调查该产品的具体应用领域甚至该领域的哪一个部分,定位该产品的科技含量;(3)调查目前市场上类似的产品及其生产流程、成本、市场价格,要么降低成本,要么研究类似产品中所不具备的特性,分析开发新产品。
2.基于生物制品的产业开发,探讨实验室的科学研究和大工业生产之间的关系和异同处?
实验室研究往往是工业化生产的前体或者说基础。生物制品的产业开发,首先是在实验室对某种的物质或代谢途径等进行大量的研究之后,对其理化性质、生物学功能等有了非常清楚的认识,然后试着去寻求该物质的应用价值,在实验室进行小规模生产,最后再考虑大工业生产。
相同点:都需要从原料开始去探索相关的生产流程,以得到最终的产品。不同点:实验室研究设备的容量很小,很难对大型工业设备中必然出现的许多工程因素(如传热、传质、流动与混合等)作充分考察;此外,在连续运转的工业化生产上,还要保证设备的稳定和工艺的重现性;最后,工业化生产还要考虑成本、市场需求等客观存在的实际问题,因为工业化生产追求的还是经济效益。
八、参考文献
[1] 应国清,石陆娥,唐振兴.核苷酸类物质的应用研究进展[J].广州食品工业科技,2004,20(02):126~128.
[2] 乔宾福.实用微生物技术[M].上海:上海科学技术文献出版社,1994.
[3] 王战勇,孔俊豪.浓盐法和稀碱法提取啤酒废酵母核糖核酸的比较[J].化学与生物工程,2007,24(02):60~62.
[4] 王琪琳.酵母核糖核酸的分离实验改进及其综合利用[J].生物学通报,2002,37(01):53.
