电导的测定及其应用
一、实验目的及要求
1.了解溶液的电导,电导率和摩尔电导的概念。
2.测量电解质溶液的摩尔电导,并计算弱电解质溶液的电离常数。
二、实验原理
电解质溶液是靠正、负离子的迁移来传递电流。而弱电解质溶液中,只有已电离部分才能承担传递电量的任务。在无限稀释的溶液中可认为弱电解质已全部电离。此时溶液的摩尔电导率为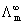 ,而且可用离子极限摩尔电导率相加而得。
,而且可用离子极限摩尔电导率相加而得。
一定浓度下的摩尔电导率Λm与无限稀释的溶液中的摩尔电导率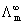 是有差别的。这由两个因素造成,一是电解质溶液的不完全离解,二是离子间存在着相互作用力。所以Λm通常称为表观摩尔电导率。
是有差别的。这由两个因素造成,一是电解质溶液的不完全离解,二是离子间存在着相互作用力。所以Λm通常称为表观摩尔电导率。
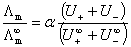 (1)
(1)
若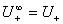 ,
,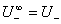 则
则
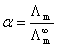 (2)
(2)
式中α为电离度。
AB型弱电解质在溶液中电离达到平衡时,电离平衡常数K,浓度C,电离度α有以下关系:
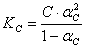 (3)
(3)
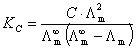 (4)
(4)
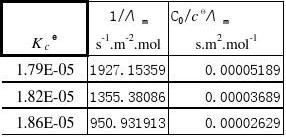
根据离子独立定律, 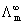 可以从离子的无限稀释的摩尔电导率计算出来。Λm则可以从电导率的测定求得,然后求算出KC 。
可以从离子的无限稀释的摩尔电导率计算出来。Λm则可以从电导率的测定求得,然后求算出KC 。
三、仪器与试剂
DDS-11A型电导率仪1台,恒温槽l套,0.1000mol/L醋酸溶液。
四、实验步骤
1.调整恒温槽温度为25℃±0.3℃。
2.用洗净、烘干的叉形管1支,加入10mL的0.1000mol/L醋酸溶液, 恒温后,测定其电导率。
3.用另一支移液管取l0mL电导水注入电导池,混合均匀,等温度恒定后,测其电导率,如此操作,共稀释4次。
4.倒去醋酸,洗净电导池,最后用电导水淋洗。注入10mL电导水,测其电导率。
5.实验结束后,切断电源,倒去电导池中溶液,洗净电导池,注入蒸馏水,并将铂黑电极浸没在蒸馏水中。
五、数据处理
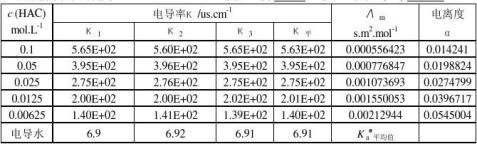
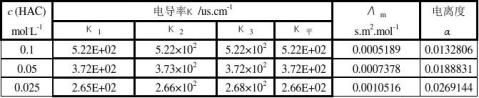
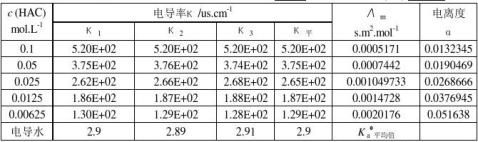
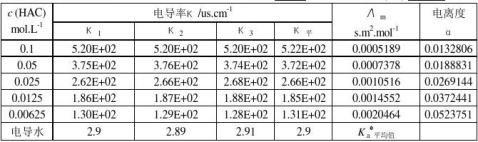
1.已知298.2K时,无限稀释离子摩尔电导率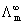 (H+)=349.82×10-4S·m2/mol ,
(H+)=349.82×10-4S·m2/mol ,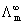 (Ac-)=40.9×10-4S·m2/mol 。计算醋酸的
(Ac-)=40.9×10-4S·m2/mol 。计算醋酸的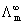 。
。
2.计算各浓度醋酸的电离度α和离解常数KC 。
六、实验注意事项
1.本实验配制溶液时,均需用电导水。
2.温度对电导有较大影响,所以整个实验必须在同一温度下进行。每次用电导水稀释溶液时,需温度相同。因此可以预先把电导水装入锥形瓶,置于恒温槽中恒温。
七、思考题
1.本实验为何要测水的电导率?
2.实验中为何用镀铂黑电极?使用时注意事项有哪些?
八、讨论
1.温度升高一度电导平均增加1.9%即
Gt=G25℃[1+1.3×10-2(t-25)] (5)
2.普通蒸馏水中常溶有CO2和氨等杂质,故存在一定电导.因此实验所测的电导值是欲测电解质和水的电导的总和。因此作电导实验时需纯度较高的水,称为电导水。其制备方法,通常是在蒸馏水中加入少许高锰酸钾,用石英或硬质玻璃蒸馏器再蒸馏一次。
3.铂电极镀铂黑的目的在于减少极化现象,且增加电极表面积,使测定电导时有较高灵敏度。铂黑电极不用时,应保存在蒸馏水中,不可使之干燥。
第二篇:实验一 电导的测定及其应用数据处理
实验一 电导的测定及其应用
-1
-12.4911.63171E-05
-1


94 m-1


94 m-1
94 m-1
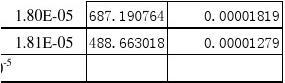
=1.82×均值)
