物理化学实验报告
专业班级 YINGHUA 姓名 SANDY 实验日期 2011年9月13日
同组姓名 XIAO 指导老师 LUO
实验名称 HAC电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
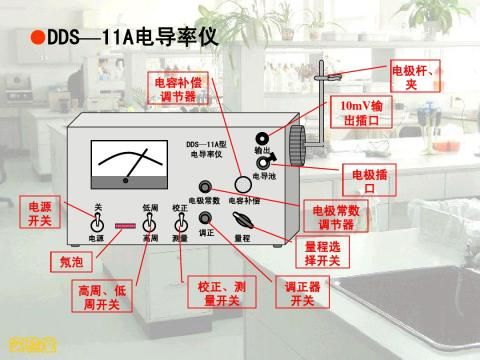
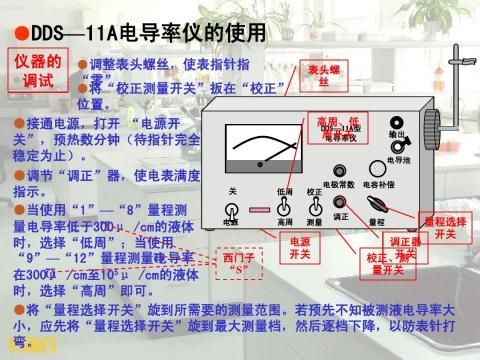
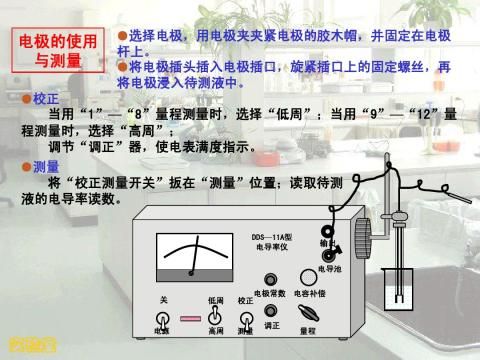
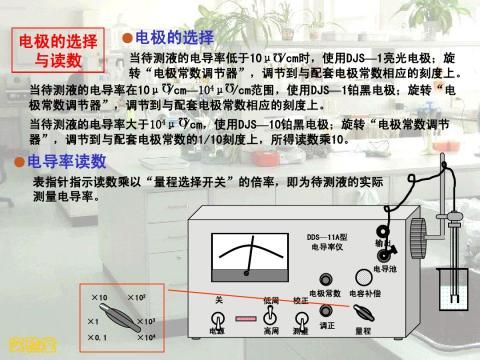
3、掌握恒温水槽及电导率仪的使用方法。
二、实验原理
1、电解质溶液的电导率、摩尔电导率
①电导率
对于电解质溶液,常用电导G表示其导电能力的大小。电导G是电阻R的倒数,
电导的单位是西门子,常用S表示。
G =κA /l
κ为该溶液的电导率 l/A = Kcell,称为电导池常数。
其意义是电极面积为及1m2、电极间距为lm的立方体导体的电导,单位为S·m-1。
Kcell可通过测定已知电导率的电解质溶液的电导而求得。然后把欲测溶液放入该电导池测出
其电导值G,再得出κ
②摩尔电导率Λm
Λm=κ/ C
C为溶液浓度,单位mol.m-3
2、当溶液的浓度逐渐降低时,由于溶液中离子间的相互作用力减弱,所以摩尔电导
率逐渐增大。柯尔劳施根据实验得出强电解质稀溶液的摩尔电导率Λm与浓度有如下
关系:
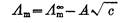
Λ∞m为无限稀释时的极限摩尔电导率 ,A视为常数可见,以Λm对 作图得一直线,其截距即为Λ∞m。
作图得一直线,其截距即为Λ∞m。
3、弱电解质溶液中,只有已电离部分才能承担传递电量的任务。在无限稀释的溶液中可认为弱电解质已全部电离。此时溶液的摩尔电导率为Λ∞m,可用离子极限摩尔电导率相加求得。
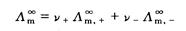
在弱电解质稀溶液中。离子的浓度很低,离子间的相互作用可以忽视,因此在浓度C时的解离度α等于他的摩尔电导率Λm与其极限摩尔电导率之比,即:
α=Λm/Λ∞m
对于HAc,在溶液中电离达到平衡时,电离平衡常数Kc与原始浓度C和解离度α有以下关系:
HAc====H+ + Ac-
t=0 C 0 0
t=t平衡 C(1-α) Cα Cα
K⊙=cα/c⊙(1-α)
在一点温度下K⊙是常数,因此可以通过测定Hac在不同浓度时的α代入上式求出K。
α=Λm/Λ∞m代入上式中得出:
K⊙=cΛm2/ [c⊙Λ∞m(Λ∞m-Λm)]
或者 cΛm=(Λ∞m)2 K⊙ c⊙(1/Λm )- Λ∞m K⊙c⊙
以cΛm对1/Λm作图,其直线斜率为(Λ∞m)2 K⊙ c⊙,因此可算出K⊙。
三、实验仪器、试剂
仪器:梅特勒326电导率仪1台、量杯(50ml)2只、移液管(25ml)3只、洗瓶1只、洗耳球1只
试剂:10.00(mol/m-3)KCl溶液、100.0(mol/m-3)HAc溶液、电导水
四、实验步骤
1、打开电导率仪开关,预热5min。
2、HAc溶液和电导水的电导率测定
①用移液管准确移入100.0(mol/m-3)HAc溶液25.00ml。置于洁净,干燥的量杯中。测其电导率3次,去平均值。
②再用移液管准确移入25.00ml已恒温的电导水,置于上述量杯中。搅拌均匀后,测其电
导率3次,取其平均值。
③用移液管准确移出25.00ml上述量杯中的溶液,弃去。再用移液管准确移入25.00ml电导水
置于上述量杯中。搅拌均匀后,测其电导率3次,取其平均值。
④再用移液管准确移入25.00ml电导水,置于上述量杯中。搅拌均匀后,测其电导率3次,
取其平均值。
⑤倾去电导池中的HAc溶液,用电导水洗净量杯和电极。然后注入电导水,测定电导水的电
导率3次,去平均值。
⑥倾去电导池中的电导水,量杯放回烘箱,电极用滤纸吸干。
五、数据记录与处理
室温: 25 ℃ 大气压: 100Kpa 实验温度 25 ℃
已知数据:25℃下10.00(mol/m-3)KCl溶液电导率=0.4113S.m-1; 25℃下无限稀释的Hac水溶液的摩尔电导率=3.9071*10-2S.m2.mol-1
1.测定HAc溶液的电导率
电导水的电导率k( H2O)/( S.m-1): 9.30*10-4 S.m-1

2、数据处理
1.HAc溶液的各组数据填入下表内:
HAc原始浓度:0.093 mol.dm-3

κ=κ′-κH2O
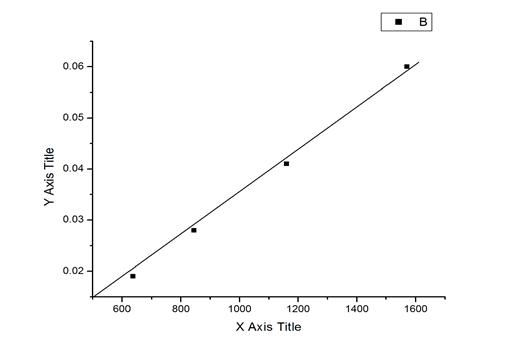
以CΛm对1/Λm作图得:
由图得出该直线的斜率k=(0.02847-0.01922) /(1.16*103-8.44*102)=2.93*10-5截距c=0.0148
因此由cΛm=(Λ∞m)2 K⊙c⊙(1/Λm ) - Λ∞m K⊙c⊙方程得出
K⊙=k/(Λ∞m)2 c⊙=2.93*10-5/[(3.907*10-2)2*1000]=1.92*10-5
误差为(2.30*10-5-1.92*10-5)/2.30*10-5=0.1652
 六、结果讨论
六、结果讨论
一、误差产生原因可能是配制溶液时浓度不是很准确,有点误差,还有就是操作过程中的误差。
主要误差原因:
1、溶液配制时的问题:溶液时由大浓度向小浓度一瓶一瓶稀释过来的。一旦某一瓶配制出现偏差,则将影响到后面的几瓶,因此在溶液配制的时候要及其小心,我认为这也是影响实验准确性的一个很重要的因素。
2、浓度较小时,信号不明显,即某个电阻改变一个大阻值,其示波器的变化不大,可能会导致大的偏差。
二、结果与讨论
1、电解质溶液导电主要与电解质的性质,溶剂的性质,测量环境的温度有关,所以测电导时要恒温。而电导池常数是一个不随温度变化的物理量,因此可以直接在不同的温度下使用。
2、电解质的摩尔电导率随浓度增加而降低,原因是:对强电解质而言,溶液浓度降低,摩尔电导率增大,这是因为随着溶液浓度的降低,离子间引力变小,粒子运动速度增加,故摩尔电导率增大。对弱电解质而言,溶液浓度降低时,摩尔电导率也增加。在溶液极稀时,随着溶液浓度的降低,摩尔电导率急剧增加
第二篇:实验课题二 电导率仪与溶液电导率的测定