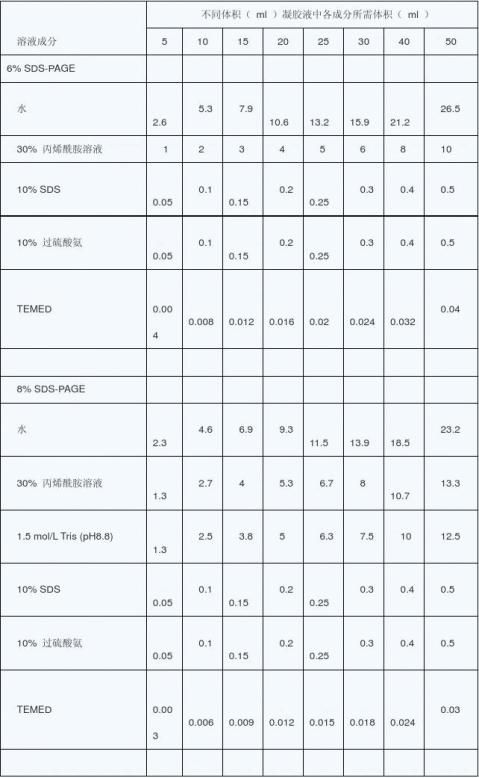
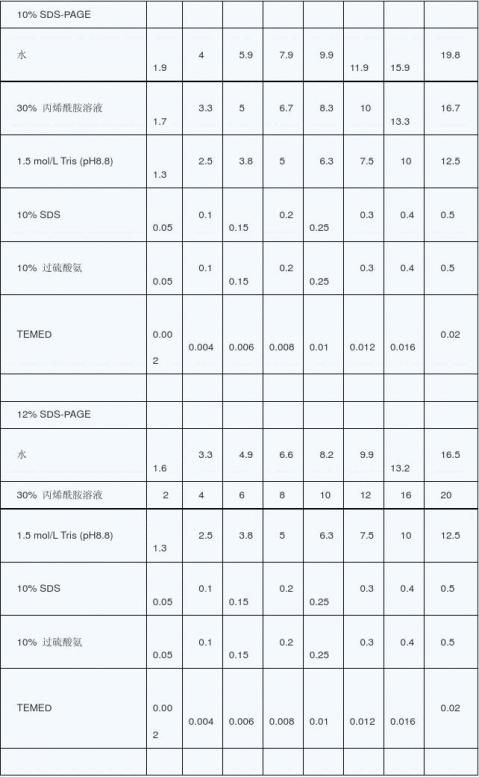
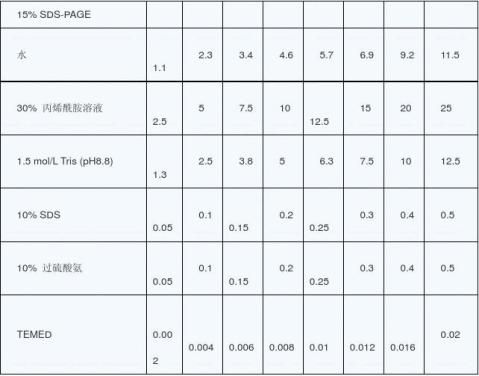
1. 聚丙烯酰胺凝胶电泳
聚丙烯酰胺凝胶电泳适宜分离鉴定低分子量的蛋白质,小于1kb的DNA片段和DNA序列。分析装载的样品容量大,可回收,DNA纯度高。在催化剂TEMED(N-N-N,- N,-四甲基乙二胺)和过硫酸胺的作用下,丙烯酰胺聚合成长链,聚丙烯酰胺链在交联剂,N- N,-亚甲双丙烯酰胺的参与下,聚丙烯酰胺链与链之间交叉联结形成凝胶。 1.1 配制30%丙烯酰胺:丙烯酰胺29g
N- N,-亚甲双丙烯酰胺 1g 加水至100ML,40C棕色瓶可保存二月 1.2 配制5×TBE缓冲液:TRIS碱 54克 硼酸 27.5克 EDTA 3.72克 加水至1L 1.3 制备聚丙烯酰胺凝胶所用试剂体积 试剂
制备不同浓度(%)凝胶所用试剂体积(ml) 3.5
30%丙烯酰胺 水 5×TBE 10%过硫酸铵
11.6 67.7 20.0 0.7
5.0 16.6 62.7 20.0 0.7
8.0 26.6 52.7 20.0 0.7
12.0 40.0 39.3 20.0 0.7
20.0 66.6 12.7 20.0 0.7
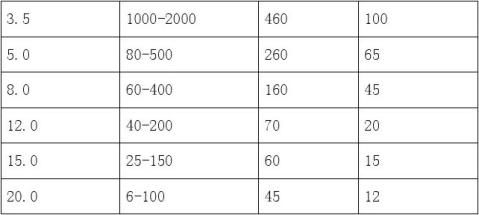
1.4 DNA在聚丙烯酰胺凝胶中有效分离范围
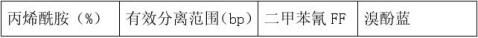
2. 聚丙烯酰胺凝胶电泳具体步骤
2.1从NaOH池中捞出浸泡的玻璃板,取出上面的残胶 2.2 把玻璃板拿到流动水处洗刷干净 2.3 洗干净的玻璃板至于玻璃板架上晾干 2.4 用乙醇擦洗玻璃板
2.5 带凹口的背板涂上硅化剂,面板则涂上粘合剂,防止电泳完毕发生撕胶和脱胶的可能(涂摸要均匀)
2.6 面板在下,背板在上。两侧用塑料板密封,并用夹子夹好。底部调节使之水平
2.7 将加入催化剂后的凝胶沿凹口均匀倒下,插入适当的封条。勿使封条下留下气泡。用夹子夹紧封条部位
2.8 室温聚合30分钟,小心取出凹口处封条,用水冲洗加样孔(否则封条所残留的丙烯酰胺在加样孔聚合产生不规则表面,引起DNA带变形)
2.9 将凝胶固定在电泳槽里。带凹口背板朝里,面向缓冲液槽 2.10 用0. 5×TBE灌满电泳槽的缓冲液槽,接上电极,打开电源。
调试工作环境为电压2000-2200V,电流150-200mA,单板电泳功率为80W。预热30分钟左右。
2.11 点样之前需切断电源,用枪将点样孔的气泡及胶吹出,然后插入点样梳,注意不要插得太深,否则点样胶面会变形,影响美观及点样。
2.12枪吸加样品,PCR产物先加loading buffer 10ul ,再变性5分钟左右,接着在冰水中冷却5分钟以上方可点样,点样完毕,电泳开始。
2.13 电泳至所需位置后,切断电源,拔出导线,回收缓冲液,卸下玻璃板。在工作台上,将背板撬起,放回原处。将面板进行银染
3. 电泳后的银染检测
3.1 原理:影像产生是由于核酸在胶上所占部位与周围的氧化——还原势不同而产生。银染液中的银离子(Ag+)可与核酸形成稳定的复合物,然后用还原剂如甲醛使Ag+还原成银颗粒,这样核酸电泳带就染成了黑褐色。
3.2 银染
银染液的配制:称2.5至3.0g AgNO3加1200---1400ml水
银染:将电泳完的面板首先在银染漂洗盆了漂洗赶紧,使胶面上没有异物。玻璃板反面没有污染物。
将加入银染液的银染盆放在摇床上后,将面板放入银染1小时左右。
3.3 显影
显影液的配制:NaOH---20g, Na2CO3----0.6g,甲醛4.5ml,加水1200ml
显影:将面板从银染盆里取出,在银染漂洗盆里漂洗,震荡5-6次,取出后使其表面尽量无水,再放入已加入显影液的显影盆里(显影,显影液的配制及甲醛的加入都需要在通风橱的摇床上进行)显影过程大约10到15分钟,以DNA条带清晰可见为准。
将显现完毕的板子在显影漂洗盆里漂洗后,方可读带。
本实验室凝胶电泳相关常用试剂配方:
1. 我实验室常用的聚丙烯酰胺凝胶是6%变性聚丙烯酰胺凝胶(简称变性胶,PAGE),就是在普通聚丙烯酰胺凝胶中加入变性剂。我们使用的变性剂是尿素。
6%PAGE具体配制方法为:
尿素210g,10×TBE 25ml ,丙烯酰胺28.5 g ,亚甲双丙烯酰胺 1.5g,加水定容至500ml,过滤后使用。
考虑到方便使用的问题,一般一次配制2L(尿素840g,10×TBE100ml,丙烯酰胺114g,亚甲双丙烯酰胺6g)。
2. 10×TBE(Tris-硼酸-EDTA)的配制
EDTA 7.44g,硼酸55g,Tris 108g,加水定容至1000ml
3. 10%过硫酸氨(AP)
10g过硫酸氨,纯水定容至100ml
4. 硅化剂配方
二甲基二氯硅烷:无水乙醇=13ml:500ml
5. 反硅化剂(粘合剂)配制
无水乙醇 500ml(一瓶),44ddH2O,3.3冰醋酸,550ul Bind silnce
(3,-Trimethoxysilyl propyl)
配置完遮光4。C保存
6 loading buffer 配制
0.1g 二甲苯氰,0.1g 溴酚蓝,1ml 0.5molEDTA ,100mL甲酰胺
*************作为检测DNA序列差异的有效手段,变性凝胶电泳在我室广泛使用,但是也有其使用范围。在我室还有一种常用的非变性凝胶电泳技术,简称SSCP(Single Strand Conformation Polymorphism,单链构象多态性)。
原理:在SSCP测定中,双链DNA(dsDNA)被变性成为单链DNA(ssDNA),每一条单链DNA都基于它们的内部序列而呈现出一种独有的折叠构象,即使同样长度的DNA单链因其碱基顺序不同、甚至单个碱基的不同会形成不同的构象。这些单链DNA在非变性条件下,用非变性聚丙烯酰胺凝胶电泳分离,单链DNA的迁移率和带型,都取决于其折叠构象和电泳时的温度。
SSCP与变性凝胶电泳基本一致,不同之处有以下几点:
a. SSCP使用非变性凝胶进行电泳,即在凝胶配制中不加入变性
剂。我室常用8%非变性胶(丙烯酰胺 80g,N- N,-亚甲双丙烯酰胺 2.76 g,10×TBE 50ml,加水定容到1L)
b. 工作环境,由于SSCP受温度影响,所以在电泳过程中应防止温
度的升高,所以电泳环境为电压400V,电流50mA,单板电泳功率为9W,不用预热。缓冲液最好用新配制的。
c. 由于电泳功率较低,所以电泳时间较长,通常需要10小时以上,
因此一般电泳需要过夜。室温在25。C以下。
有错误之处请大家批评指正!
第二篇:聚丙烯酰胺凝胶电泳凝胶的配方