己二酸的制备
一、实验目的
学习用环己醇制备己二酸的原理和方法;掌握浓缩、过滤、重结晶等操作技能。
二、实验原理
己二酸是合成尼龙-66的主要原料之一,它可以用硝酸或高锰酸钾氧化环己醇制得。
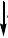
OH
3+8HNO3+8NO+7H2OCOOH2
8NO2
三、药品仪器
药品:50%HNO3,NH4VO3,环己醇,NaOH吸收液。 仪器:球形冷凝管、温度计、分液漏斗、100ml三颈烧瓶、
布氏漏斗、抽滤瓶等。
四、实验步骤
在装有回流冷凝管、温度计、和滴液漏斗的100 mL三颈烧瓶中,放置18 mL (0.18 mol) 50% HNO3,及少许偏钒酸铵(约0.03g),并在冷凝管上接一气体吸收装置,用稀NaOH吸收反应过程中产生的二氧化氮气体。
滴液漏斗中加入6 mL(约0.06 mol)环己醇。
三颈烧瓶用水浴预热到50 oC左右,移去水浴,先滴入5~6
滴环己醇,至反应开始放出二氧化氮气体,然后慢慢加入其余部分的环己醇,调节滴加速度,使瓶内温度维持在50~60oC之间。温度过高时,用冷水浴冷却,温度过低时,则用热水浴加热,滴加完毕约需15min。
加完后继续搅拌,并用80~90 oC的热水浴加热10min,至几乎无棕红色气体放出为止。然后将此热溶液倒入100ml的烧杯中,冷却后析出己二酸,抽滤,用15ml冷水洗涤两次,干燥,粗产物约6克。
粗制的己二酸可以在水中重结晶。纯己二酸为白色棱状晶体,产量约5.1 g,mp为153 oC。
五、实验注意点
1. 环己醇和硝酸切不可用同一量筒量取。
2. 偏钒酸铵不可多加,否则产品发黄。
3. 本实验为强烈放热反应,所以滴加环己醇的速度不宜过快,以免反应过剧,引起爆炸。一般可在环己醇中加1ml水,一是减少环己醇因粘稠带来的损失,二是避免反应过剧。
4. 实验产生的二氧化氮气体有毒,所以装置要求严密不漏气,并要作好尾气吸收。
第二篇:实验十六 己二酸的制备
实验十六 己二酸的制备
一、实验目的
1、学习环己醇氧化制备己二酸的原理和方法;
2、掌握重结晶、搅拌等基本操作。
二、实验原理
己二酸是合成尼龙-66的主要原料之一,可以用硝酸氧化环己醇制得。
反应方程式如下:
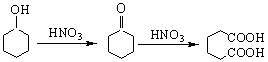
三、实验药品及其物理常数
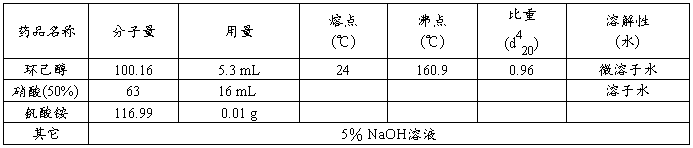
四、主要仪器和材料
水浴锅 三口烧瓶(100 mL、19#×3) 恒压滴液漏斗 空心塞(14#) 球形冷凝管(19#) 螺帽接头(19#,2只) 温度计(100℃) 布氏漏斗 吸滤瓶 烧杯 冰 滤纸 水泵等.
五、实验装置
滴加、回流、尾气吸收装置
六、操作步骤
【操作要点及注意事项】
⑴搭装置:仪器的选用,搭配顺序,各仪器高度位置的控制要合理。
⑵检验气密性:实验产生的二氧化氮气体有毒,所以装置要求严密不漏气。注意尾气吸收装置中三角漏斗的高度。
⑶加料:环己醇和硝酸切不可用同一量筒量取。钒酸铵不可多加,否则产品发黄。
⑷滴加:本实验为强烈放热反应,所以滴加环己醇的速度不宜过快,以免反应过剧,引起爆炸。一般可在环己醇中加1mL水,一是减少环己醇因粘稠带来的损失,二是避免反应过剧。
⑸加热:可选择水浴加热,滴加完后继续用80-90 ℃水浴加热约15 min, 同时要摇动反应瓶,至几乎无棕色二氧化氮气体放出为止。
七、实验结果
1、产品性状: ; 2、理论产量: ;
3、实际产量: ; 4、产率: .
八、实验讨论
1、在该反应中为何要检查装置气密性?
2、为什么反应必须严格控制环己醇的滴加速度?
3、为什么有些实验在加入最后一个反应物前应预先加热?
九、实验体会
谈谈实验的成败、得失。
