现代有机合成实验实验报告
实验名称:二苯甲醇的制备
一、实验目的
(1)学习制备二苯甲醇的实验原理和方法;
(2)巩固重结晶的操作方法;
(3)进一步练习半微量实验。
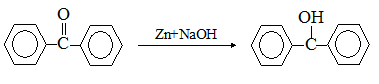
二、实验原理
二苯甲酮可以通过多种还原剂还原得到二苯甲醇。在碱性醇溶液中用锌粉还原,是制备二苯甲醇常用的方法,适用于中等规模的实验室制备,对于小量合成,硼氢化钠是更理想的试剂。本实验采用锌粉还原。
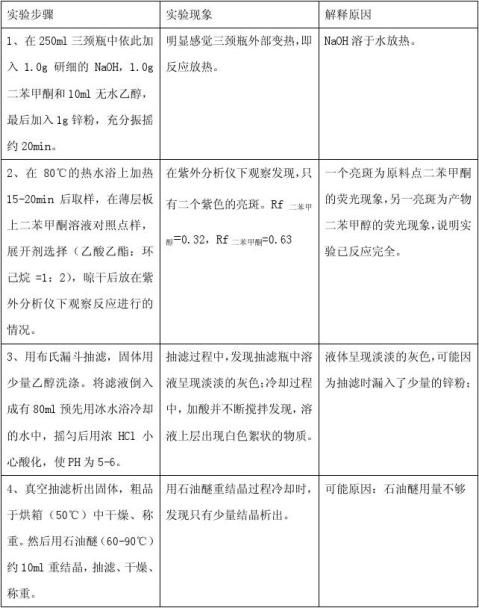
三、实验步骤
(1)仪器:搅拌器(标准口)、铁架台、球形冷凝管(标准口)、油浴锅、100℃温度计、250ml三颈瓶、100ml量筒、减压抽滤装置、天平、干燥器、烧杯、玻璃棒、表面皿、滤纸。
(2)试剂:二苯甲酮 1.0g ; NaOH 1.0g ; 无水乙醇 10ml; 石油醚 10ml;乙酸乙酯:环己烷 =1:2(10ml); 硅胶G 适量
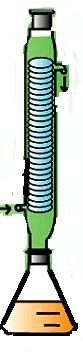
二苯甲醇反应装置
四、数据处理
经重结晶,抽滤、干燥后,称得针状结晶的二苯甲醇为0.53g,产率为53%。 五、实验结论
1、二苯甲酮和氢氧化钠必须研碎,否则反应很难进行。
2、锌粉最好后加,便于振摇。
3、热水浴最好是5min,10min太长了,易发生颜色变化(变黄,严重者发红),温度可以控制在70-75℃。
4、整个反应过程要求不断振摇,是实验成败关键。
5、反应液颜色为灰黑色为正常。若溶液发红,可能反应不成功。
6、酸化时,溶液的酸性不宜太强,否则难于析出固体。PH=5-6。
7、由于用(60-90℃)石油醚重结晶,故产品仪器均需干燥,否则很难溶解产物。
8、产物若为桔红色即不太好,应为白色或浅黄色。
六、实验讨论
1、此实验中溶剂的选择是95%的乙醇,可否选择甲醇呢,为什么?
答:该实验中溶剂可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇,对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。
2、浓盐酸在这个实验中所起到的作用主要有哪些?
答:中和过量的氢养化钠,滴加时速度不宜过快,有大量气泡放出,严禁明火。
七、参考文献
[1]王清廉,沈凤嘉. 有机化学实验[M]. 高等教育出版社,1978.
[2]李需良. 微型半微型有机化学实验[M]. 高等教育出版社, 2003.
[3]曾绍琼. 有机化学实验[M]. 高等教育出版社, 1986.
第二篇:二苯甲醇的制备
二苯甲醇的制备
一、实验目的
1.学习酮的还原反应;
2.了解NaBH4还原的原理。
一、实验内容
用NaBH4还原二苯甲酮制备二苯甲醇。
二、实验原理
反应式: OH
NaBH4
MeOH
三、实验方法与步骤
1、加料并反应:在50ml圆底烧瓶中溶解1.5克二苯酮于20ml甲醇中,小心加入0.4克硼氢化钠,混匀后在室温放置20min,并时加摇动。
2、后处理,分离出粗产品:在水浴上蒸去大部分甲醇,冷却后将残液倒入40ml水中,并搅拌使充分混合水解硼酸酯的络合物。每次用10ml乙醚分三涮洗烧瓶和萃取水层,合并醚萃取液,用无水硫酸镁干燥。过滤除去硫酸镁,水浴上蒸去乙醚,再用水泵减压抽去残余的乙醚。
3、产品提纯:残渣用15ml石油醚(60-90℃)重结晶,得约1克二苯甲醇的针状结晶,熔点68-69℃。纯二苯甲醇的熔点为69℃。
四、实验要求
1. 实验内容要求:产品产量应在0.5克以上,外观为白色针状晶体;熔点不低于65℃,熔程不超过3℃;
2. 实验报告要求:应具备实验目的、原理、实验内容、操作过程、实验结果及问题讨论;
3. 考核评价要求:(1)操作规范、实验结果良好;(2)有完整的实验预习报告和实验报告(3)仪器的清洗和整理工作妥善。 五、场地、仪器与药品
场地:有机化学实验室。
仪器:M22磨口仪器,电炉,水浴锅,分液漏斗,水泵。 药品:二苯酮、硼氢化钠、甲醇、乙醚和石油醚(60-90℃)。
