实验3 三苯甲醇的制备
一、实验目的
1.学习格氏试剂制备三苯甲醇的原理方法;
2.掌握Grignard试剂的制备进行Grignard反应的操作;
3.进一步练习搅拌、回流、萃取、蒸馏等基本操作。
二、实验原理
主反应:
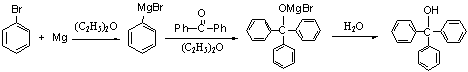
 副反应:
副反应:

三、主要仪器和试剂
仪器:三口烧瓶(100mL) 螺帽接头(19#) 球形冷凝管(19#) 空心塞(19#) 滴液漏斗
试剂:镁条 (1.4 g , 0.055 mol) 无水乙醚(45mL) 沸石 饱和氯化铵 (40mL )无水氯化钙 橡皮管 滤纸 石油醚20mL 石油醚-95%乙醇(2:1,15mL) 碘
表1 反应物与产物的物理常数

四、实验装置
干燥回流-滴加-控温装置
五、实验步骤
1、格氏试剂的制备
2、三苯甲醇的制备
3、三苯甲醇的分离提纯
六、注意事项:
1、加氯化铵溶液之前的步骤中所用仪器和药品必须严格干燥处理。否则将不能反应或不能得到目标化合物。
2、引发反应时,碘的量不可多,若室温下不能引发可适当温热。
3、滴加溴苯溶液时速度要控制好,不可过快以免生成联苯。
4、滴加溴苯溶液时若体系过于粘稠可适当补加一些无水乙醚。
5、滴加完氯化铵溶液后若还有固体未完全溶解可加少许稀盐酸溶解。
6、重结晶过程中加热溶剂时要回流加冷凝管,以减少溶剂损失并防止发生着火的危险。
七、实验结果

八、思考题
1、在对格氏试剂过夜保存时须采取什么措施?在进行格氏反应时是否需要特殊保护?
答:如过夜保存,需用惰性气体保护,与空气隔开。
可以不用特殊保护,因为格氏反应通常是在无水乙醚溶液中进行的,反应时乙醚的蒸气可以把格氏试剂与空气隔绝开。
2、试述碘在本反应中的作用。
答:制备格氏试剂反应不易发生时,加一粒碘,可诱导引发反应。
因为碘负离子既是一个强的亲核试剂,又是一个好的离去基团;在用活性较小的卤代烃制备格氏试剂发生困难时,反应液中加入碘后可提高卤代烃的反应活性,诱导反应发生。
3、在制备苯基溴化镁时,为什么溴苯不宜加入过快
答:如加入过快,会使反应过于激烈,溴苯也是一个极性分子,有缺电中心,能被亲核试剂进攻,产生过多的副产物联苯。
4、在制备三苯甲醇时,加入饱和氯化铵的目的是什么?
答:加入饱和氯化铵的目的是使反应中间产物能在酸性条件下水解,生成的三苯甲醇尽可能多地从饱和水溶液中结晶出来,减少损失。也可用饱和的食盐和少量盐酸溶液替代。
5、本反应可能发生什么副反应?
答:格氏试剂可能与水、氧气、二氧化碳及溴苯反应,生成苯、苯酚、苯甲酸和联苯。
6、 反应结束,可用那些方法除去未反应完的溴苯及副产物?
答:利用三苯甲醇与溴苯及联苯在沸点上的较大差异,且与水不溶等特点,可用水汽蒸馏法除去低沸点副产物;另外,三苯甲醇在石油醚中不溶,而溴苯及联苯确有较好的溶解度,利用它们溶解性能的不同,加入石油醚可提取溴苯及联苯等副产物。从而达到分离的目的。
九、实验体会
谈谈实验的成败、得失。
第二篇:实验十苯甲醇和苯甲酸的制备
实验十 苯甲醇和苯甲酸的制备
一、实验目的
1.学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法。
2.进一步熟悉机械搅拌器的使用。
3.进一步掌握萃取、洗涤、蒸馏、干燥和重结晶等基本操作。
4.全面复习巩固有机化学实验基本操作技能。
二、基本原理
无α-H的醛在浓碱溶液作用下发生歧化反应,一分子醛被氧化成羧酸,另一分子醛则被还原成醇,此反应称坎尼扎罗反应。本实验采用苯甲醛在浓氢氧化钠溶液中发生坎尼扎罗反应,制备苯甲醇和苯甲酸,反应式如下:
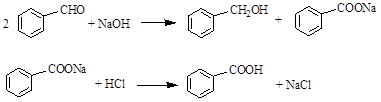
三、主要试剂与仪器
1.试剂 苯甲醛 10 mL (0.10 mol),氢氧化钠 8g (0.2mol),浓盐酸,乙醚,饱和亚硫酸氢钠溶液,10%碳酸钠溶液,无水硫酸镁。
2.仪器 100mL 圆底烧瓶,球形冷凝管,分液漏斗,直形冷凝管,蒸馏头, 温度计套管,温度计(250℃),支管接引管,锥形瓶,空心塞,量筒,烧杯,布氏漏斗,吸滤瓶,表面皿,红外灯,机械搅拌器。
四、主要物料的物理常数
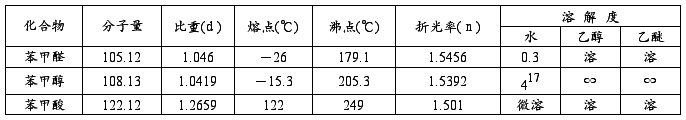
五、实验装置
本实验制备苯甲醇和苯甲酸,采用机械搅拌下的加热回流装置,如图1所示。乙醚的沸点低,要注意安全,蒸馏低沸点液体的装置如图2所示。

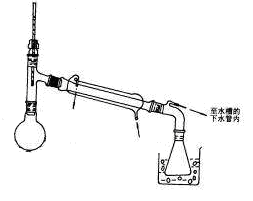
图1 制备苯甲酸和苯甲醇的反应装置图 图2 蒸乙醚的装置图
六、实验步骤
1.在250mL三口烧瓶上安装机械搅拌及回流冷凝管,另一口塞住,如图1。
2.加入8g氢氧化钠和30mL水,搅拌溶解。稍冷,加入10 mL新蒸过的苯甲醛。
3.开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。
4.停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温。
5.反应物冷却至室温后,倒入分液漏斗,用乙醚萃取三次,每次10mL。水层保留待用。
6.合并三次乙醚萃取液,依次用5 mL饱和亚硫酸氢钠洗涤,10mL 10%碳酸钠溶液洗涤,10 mL水洗涤。
7.分出醚层,倒入干燥的锥形瓶,加无水硫酸镁干燥,注意锥形瓶上要加塞。
8.如图2安装好低沸点液体的蒸馏装置,缓缓加热蒸出乙醚(回收)。
9.升高温度蒸馏,当温度升到140℃时改用空气冷凝管,收集198℃~204℃的馏分,即为苯甲醇,量体积,回收,计算产率。
10.将第5步保留的水层慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。
11.冷却,抽滤,得到粗苯甲酸。
12.粗苯甲酸用水作溶剂重结晶,需加活性炭脱色。产品在红外灯下干燥后称重,回收,计算产率。
七、注意事项
1.本实验需要用乙醚,而乙醚极易着火,必须在近旁没有任何种类的明火时才能使用乙醚。蒸乙醚时可在接引管支管上连接一长橡皮管通入水槽的下水管内或引出室外,接受器用冷水浴冷却。
2.结晶提纯苯甲酸可用水作溶剂重,苯甲酸在水中的溶解度为:80℃时,每100 mL水中可溶解苯甲酸2.2g。
八、思考题
1.试比较Cannizzaro反应与羟醛缩合反应在醛的结构上有何不同。
2.本实验中两种产物是根据什么原理分离提纯的?用饱和亚硫酸氢钠及10%碳酸钠溶液洗涤的目的是什么?
3.乙醚萃取后剩余的水溶液,用浓盐酸酸化到中性是否最恰当?为什么?
4.为什么要用新蒸过的苯甲醛?长期放置的苯甲醛含有什么杂质?如不除去,对本实验有何影响?
