一、 实验目的
1. 学习次氯酸钠氧化法制备环己酮的原理和方法;
2. 进一步了解醇和酮之间的联系与区别。
二、 实验原理
用次氯酸钠作氧化剂,将环己醇氧化成环己酮。

四、仪器及用量规格
150ml三颈烧瓶、搅拌器、滴液漏斗、温度计、冷凝管、接收器、分液漏斗、量筒、100ml圆底烧瓶、直形冷凝管、干燥管 、电炉 、形瓶 、接引管 、 75°蒸馏头、玻璃棒
五、 实验装置
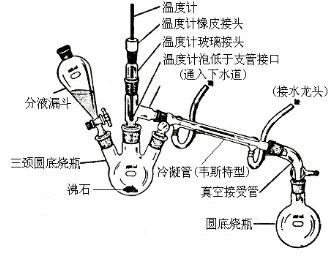
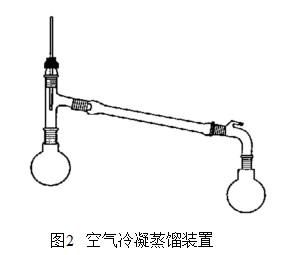
六、步骤及现象
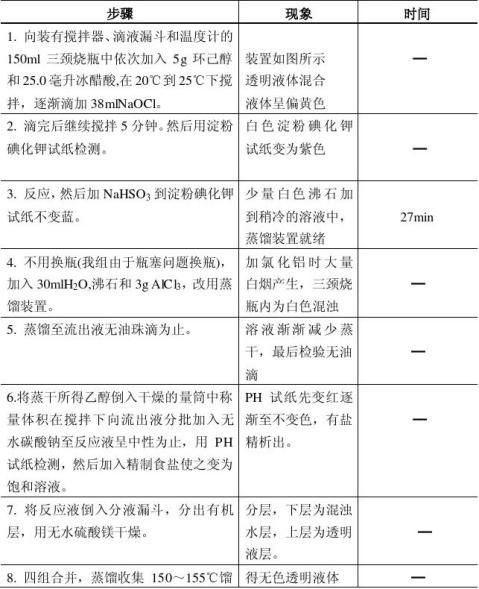

七、数据记录与处理
1.
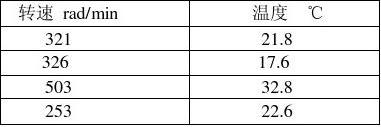


我组由于实验失误所得分液后不纯环己酮体积为2.31 ml
5.实验数据处理
查资料得环己酮的密度为0.9478g/ml
产率=(6.58×0.9478÷98) ÷(5×4÷100) =31.82%
回收率=(6.58÷13.05)×100%=50.42%
八、 结果与讨论
实验教训
⑴这次的试验较为失败,期间出现较大实验失误,在分液时出现分液漏斗瓶塞松开使产物大量损失,总结教训:实验一定要谨慎,不要分心。
⑵总的产率也并不高,不仅仅是由于实验失误问题,也有部分产物在转移过程中损失了:①换瓶时的损失;②在第二次蒸馏时由于没换瓶重新蒸馏所造成的损失;③蒸馏时也许存在不完全所造成的损失。
实验经验
⑴第二次分馏时要注意好换瓶温度,换瓶早了会影响环己酮的纯度; ⑵溶液不能蒸干,防爆沸;
⑶水馏分不宜过多,否则即使盐析,也有环己酮溶于水而损失。
结果与讨论结果与讨论结果与讨论 1.数据分析: 产率相对较低,操作过程不够精细 2.结果讨论: (1) 环己酮的发生过程,用碘化钾检验没有呈蓝紫色,一方面可能是试纸的质量不过关,一方面可能是在反应过程总共出了某些问题导致 环己酮生成量较低,使得结果偏低 (2) 加热蒸馏不充分,液面上还漂浮着黄棕色的油状小液滴时就停止蒸馏,导致
产率较低
(3) 分液静置时间不够长,导致环己酮的损失 3.实际操作对实验结果的影响: (1) 反应温度要控制在20~25℃,此时收率较高,若温度低于20℃则不反应,温度过高则易挥发 (2) 加AlCl3可预防蒸馏时发泡
(3) 加入NaCl是为了降低环己酮的溶解度并有利于环己酮的分层 (4) 分离萃取必须严格按要求进行,否则在此几步中会损失产物影响产率
第二篇:环己酮的制备实验报告
有 机 化 学 实 验 报 告

实 验 名 称: 环己酮的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级: 化工10-6班
姓 名: 严晓晓 学 号 10402010602
指 导 教 师: 邵琼芳 陈 斌
日 期: 2011年11月27日
一、 实验目的
1、 学习次氯酸氧化法制环己酮的原理和方法;
2、 进一步了解醇和酮这件的联系和区别。
二、 实验原理
用次氯酸钠作氧化剂,讲环己醇氧化成环己酮。

三、 主要试剂及仪器
试剂:环己醇(有樟脑气味的无色粘性液体,熔点:25.2℃,沸点: 160.9 ℃ 相对密度:0.9624)、次氯酸钠、冰醋酸、无水碳酸钠、无水硫酸镁、氯化铝、沸石、氯化钠、碘化钾淀粉试纸。
仪器:搅拌器、滴液漏斗、温度计、250 ml三颈烧瓶、酒精灯、锥形瓶、冷凝管、蒸馏烧瓶、接液管、分液漏斗。
四、 试剂用量规格

五、 实验仪器装置
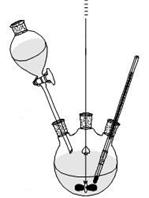
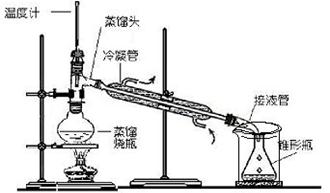
反应装置 蒸馏装置
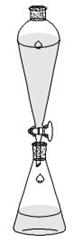
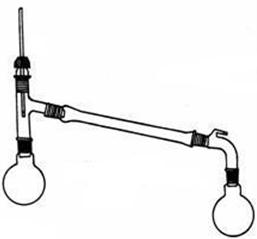
分液装置 空气冷凝蒸馏装置
六、 实验步骤及现象
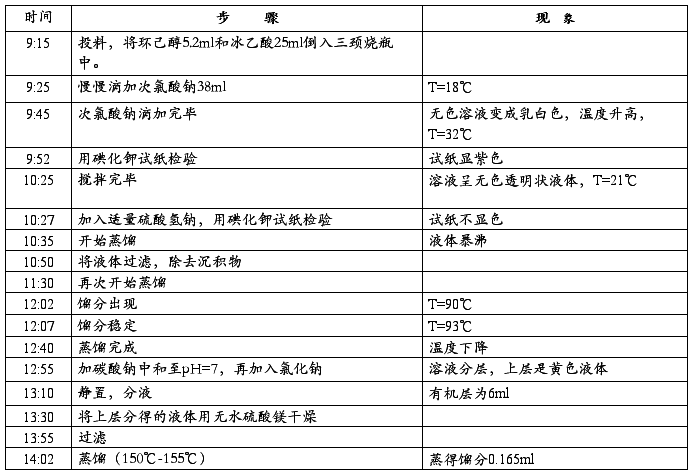
七、 实验数据处理
环己醇的物质的量计算:n=m/M=5g/100g?mol-1=0.05mol
环己酮的物质的量计算:n′=m′/M′=ρV/M′=0.9624g?cm-3*0.165cm3/98 g?mol-1=0.0016mol
理论应该得出的环己酮的物质的量=实际环己醇的物质的量=0.05mol
环己酮产率=实际量/理论量=0.0016/0.05=3.2%
八、 实验讨论
1、 由于在第一次蒸馏时,溶液暴沸,所以将溶液过滤,除去沉积物,使得损失了大量产品;
2、 加热蒸馏不够充分,而且可能有部分蒸汽逸出,导致产品损失;
3、 分液静置的时候时间不够长,导致产品损失;
4、 最后蒸馏的时候时间太短,不够充分,使得环己酮没有完全分离出来。
九、 注意事项
1、 蒸馏时温度不宜升的过快,将导致溶液暴沸;
2、 加入次氯酸不宜过多,否则中和时加入较多的亚硫酸氢钠,从而造成蒸馏时间过长;
3、 盐析时,NaCl不宜加入太多,应该慢慢加入。
