实验一 凝集试验
颗粒性抗原(细菌、螺旋体、红细胞等)与相应抗体结合后,在有适量电解质存在下,抗原颗粒可相互凝集成肉眼可见的凝集块,称为凝集反应(Agglutination reaction)或凝集试验。参与凝集反应的抗原称为凝集原(Agglutinogen),抗体称为凝集素(Agglutinin)。
细菌或其它凝集原都带有相同的负电荷,在悬液中相互排斥而呈现均匀的分散状态。抗原与相应抗体相遇后可以发生特异性结合,形成抗原抗体复合物,降低了抗原分子间的静电排斥力,此时已有凝集的趋向,在电解质(如生理盐水)参与下,由于离子的作用,中和了抗原抗体复合物外面的大部分电荷,使之失去了彼此间的静电排斥力,分子间相互吸引,凝集成大的絮片或颗粒,出现了肉眼可见的凝集反应。根据是否出现凝集反应及其程度,对待测抗原或待测抗体进行定性、定量测定。
凝集反应包括直接凝集反应和间接凝集反应两大类,本实验主要介绍直接凝集反应。
[目的要求]
1. 掌握平板凝集试验和试管凝集试验的操作方法。
2. 掌握凝集试验的结果判定及判定标准。
3. 熟悉平板凝集试验和试管凝集试验所需材料和试剂。
[材料与试剂]
1. 玻板,载玻片,试管(1cm x 8cm),试管架,刻度吸管,滴管,微量可调加样器,滴头(tip头),牙签或火柴棒,记号笔。
2. 灭菌的生理盐水,灭菌的0.5%石炭酸生理盐水。
3. 布氏杆菌病试管凝集抗原,布氏杆菌病平板凝集抗原,布氏杆菌病虎红平板凝集抗原,布氏杆菌病阳性血清,布氏杆菌病阴性血清,被检血清(牛、羊或猪)。
4. 鸡白痢平板凝集抗原,鸡白痢阳性血清,鸡白痢阴性血清,被检鸡血清。
[实验内容及操作方法]
(一)试管凝集试验
以牛布氏杆菌病试管凝集试验为例。
1. 试管准备:每份血清用试管4支,另取3支试管作为对照,作好标记,置试管架上。如被检血清有多份,对照只需做1份。
2. 被检血清稀释:第1管加入2.3 ml 0.5% 石炭酸生理盐水,第2、3、4管加入0.5 ml 0.5% 石炭酸生理盐水;然后用加样器或刻度吸管吸取被检血清0.2 ml ,加入第1管中,反复吹吸5次混匀,吸取1.5 ml 弃之,再吸取0.5 ml 加入第2管中,混匀后吸取0.5 ml 加入第3管,依此类推至第4管,混匀后吸弃0.5 ml (见表1-1)。该被检血清的稀释度分别是1:12.5、1:25、1:50、1:100。
3. 对照管制作:第5管中加0.5% 石炭酸生理盐水0.5 ml ,第6管加1:25稀释的布氏杆菌病阳性血清0.5 ml ,第7管加1:25稀释的布氏杆菌病阴性血清0.5 ml 。
4. 加抗原:将布氏杆菌病试管凝集抗原用0.5% 石炭酸生理盐水作1:20稀释,每支试管加0.5 ml 。
表1-1 布氏杆菌病试管凝集试验术式表(单位:ml)

弃1.5 弃0.5
5. 感作(反应):7支试管加完抗原后,充分混匀,置于37℃温箱中4-10h,取出后置室温18-24h(或37℃温箱12-14h,取出后置室温2-4h;或37℃温箱中22-24 h取出),然后观察并记录结果。
6. 结果判定:判定结果时用“+”表示反应的强度。根据各管中上清液的透明度、抗原被凝集的程度及凝集块的形状,来判定凝集反应的程度。
++++:100%抗原凝集,上清液完全透明,菌体完全被凝集呈伞状沉于管底,振荡时,沉淀物呈片状、块状或颗粒状。
+++:75%抗原凝集,上清液略呈混浊,菌体大部分被凝集沉于管底,振荡时情况如上。(管底凝集物与100%凝集时相同,只是上清液稍浑浊)。
++:50%抗原凝集,上清液浑浊半透明,管底有中等量的凝集物(管底有明显的凝集)。
+:25%抗原凝集,上清液完全浑浊不透明,管底有少量凝集物或凝集的痕迹。
-:抗原完全未凝集,上清液完全浑浊不透明,但由于菌体的自然下沉,在管底中央出现规则的菌体自沉圆点,振荡后立即散开呈均匀混浊。
7. 判定标准:能使50% 抗原凝集的血清最高稀释度称为该血清的凝集价(或称滴度)。
牛、马和骆驼的血清凝集价大于或等于1:100,判为阳性,1:50的凝集价判为疑似反应(可疑);猪、绵羊、山羊和狗的血清凝集价大于或等于1:50,判为阳性,1:25的凝集价判为疑似反应(可疑)。
[注意事项]
1. 实验时必须设抗原、阳性血清及阴性血清对照,以避免假阳性、假阴性的结果。
2. 结果判为可疑时,隔2-3周后采血重做。阳性畜群,重检时仍为可疑,可判为阳性。对同群中既无临床症状又无凝集反应阳性者,马、猪重检仍为可疑,判阴性;牛、羊重检仍为可疑者,可判为阳性,或以补体结合反应核对。
(二)布氏杆菌病平板凝集试验
1. 加血清:取洁净玻板一块,用蜡笔划成方格(4cm2),并注明被检血清号码,以100mL微量可调加样器按下列量加被检血清于方格内,第l格80mL、第2格40mL、第3格20mL、第4格10mL。血清用前需放室温,使其温度达20℃左右。每一份检样需换一个tip头。
大规模检疫时,允许只用两个血清量作试验,牛、马、骆驼用40mL 和20mL ;猪、山羊、绵羊、狗用80mL和40mL。
2. 加抗原:每格加布氏杆菌病平板凝集抗原30mL,滴在血清附近,而不与血清接触。从血清量最少的一格起,用牙签将血清与抗原混匀,一份血清用一根牙签。
抗原用前摇匀,并置室温使其温度达20℃左右。
3. 作用:混和完毕后,将玻板置恒温箱中或采用别的办法适当加温,使温度达到30℃左右,3-5min内记录反应结果。
4. 对照:每次试验须用标准阳性血清和阴性血清以及生理盐水作对照。
5. 结果判定:按下列标准记录反应结果。
++++:出现大的凝集块,液体完全透明,即100% 凝集。
+++:有明显凝集块,液体几乎完全透明,即75% 凝集。
++:有可见凝集块,液体不甚透明,即50% 凝集。
+:液体混浊,有小的颗粒状物,即25% 凝集。
-:液体均匀混浊,无凝集现象。
6. 平板凝集试验与试管凝集试验的关系见表1-2。
表1-2 平板凝集试验与试管凝集试验的关系

7. 判定标准:同试管凝集试验。
8. 注意:对于阳性及可疑的被检血清需用试管凝集试验进行验证。
(三)虎红平板凝集试验
这种试验是快速平板凝集试验。抗原是布氏杆菌加虎红制成。虎红平板凝集试验可与试管凝集试验及补体结合试验效果相比,具有操作简单、快速、特异性强的优点。
1. 被检血清和布氏杆菌病虎红平板凝集抗原各30mL滴于玻璃板的方格内,每份血清各用一支牙签或火柴棒混合均匀。在室温(20℃)4-10min内记录反应结果。同时以阳、阴性血清作对照。
2. 结果判定:在阳性血清及阴性血清试验结果正确的前提下,被检血清出现任何程度的凝集现象均判为阳性,完全不凝集的判为阴性,无可疑反应。
3. 注意:抗原用前充分摇匀,抗原和被检血清用前应放室温30-60min后再进行试验。
(四)鸡白痢平板凝集试验
1. 被检鸡血清和鸡白痢平板凝集抗原各1滴(约30mL)滴于玻板或载玻片上,用牙签或火柴棒充分混合。
2. 结果判定:在室温(20℃)下,观察30-60s,凝集者为阳性,不凝集者为阴性。
[思考题]
1. 凝集反应的原理是什么?
2. 哪些因素影响细菌凝集试验?
3. 凝集试验中为什么要设阳性、阴性血清及抗原对照?
实验二 病毒的血凝及血凝抑制试验
有些病毒具有凝集某种(些)动物红细胞的能力,称为病毒的血凝,利用这种特性设计的试验称血球凝集(HA)试验,以此来推测被检材料中有无病毒存在,是非特异性的,但病毒的凝集红细胞的能力可被相应的特异性抗体所抑制,即血球凝集抑制(HI)试验,具有特异性。通过HA-HI试验,可用已知血清来鉴定未知病毒,也可用已知病毒来检查被检血清中的相应抗体和滴定抗体的含量。
[目的要求]
掌握病毒HA和HI试验的原理和基本操作方法,了解其实用价值。
[材料与试剂]
1. 96孔“U”形或“V”形微量反应板,50mL定量移液器,滴头,微型振荡器。
2. 生理盐水,0.5% 鸡红细胞悬液。
3. 新城疫病毒液(尿囊液或冻干疫苗液),新城疫阳性血清,被检鸡血清。
[实验内容及操作方法]
(一)血球凝集(HA)试验
1. 在96孔微量反应板上进行,自左至右各孔加50mL生理盐水。
2. 于左侧第1孔加50mL病毒液(尿囊液或冻干疫苗液),混合均匀后,吸50mL至第2孔,依次倍比稀释至第11孔,吸弃50mL;第12孔为红细胞对照。
3. 自右至左依次向各孔加入0.5% 鸡红细胞悬液50mL,在振荡器上振荡,室温下静置后观察结果(表4-1)。
表 4-1 病毒血凝试验的操作方法(单位:mL)

4. 结果判定:从静置后10 min开始观察结果,待对照孔红细胞已沉淀即可进行结果观察。红细胞全部凝集,沉于孔底,平铺呈网状,即为100% 凝集(++++),不凝集者(-)红细胞沉于孔底呈点状。
以100% 凝集的病毒最大稀释度为该病毒血凝价,即为一个凝集单位。从表4-1看出,该新城疫病毒液的血凝价为1:128,则l:128为1个血凝单位,1:64、l:32分别为2、4个血凝单位,或将128/4=32,即1:32稀释的病毒液为4个血凝单位。
(二) 血球凝集抑制(HI)试验
1. 根据HA试验结果,确定病毒的血凝价,配制出4个血凝单位的病毒液。
2. 在96孔微量反应板上进行,用固定病毒稀释血清的方法,自第1孔至第11孔各加50mL生理盐水。
3. 第1孔加被检鸡血清50mL,吹吸混合均匀,吸50mL至第2孔,依此倍比稀释至第10孔,吸弃50mL,稀释度分别为:1:2、1:4、1:8 …… ;第12孔加新城疫阳性血清50mL,作为血清对照。
4. 自第1孔至12孔各加50mL 4个血凝单位的新城疫病毒液,其中第11孔为4单位新城疫病毒液对照,振荡混合均匀,置室温中作用10min 。
5. 自第l孔至12孔各加0.5% 鸡红细胞悬液50mL,振荡混合均匀,室温下静置后观察结果(表4-2)。
表4-2 病毒血凝抑制试验的操作方法(单位:mL)
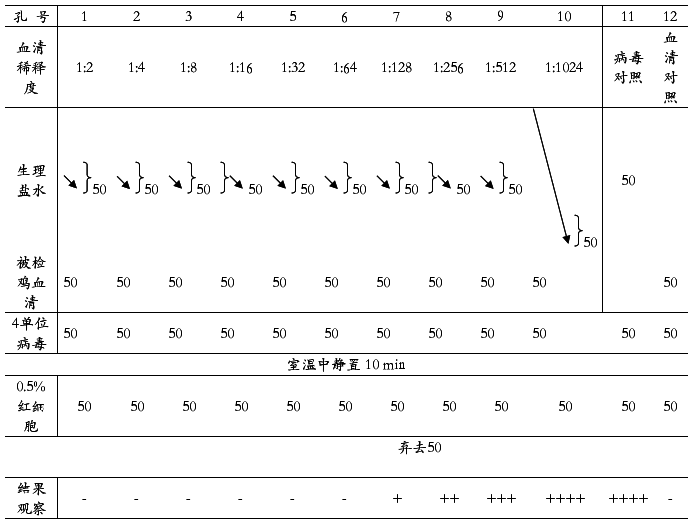
6. 结果判定:待病毒对照孔(第11孔)出现红细胞100%凝集(++++),而血清对照孔(第12孔)为完全不凝集(-)时,即可进行结果观察。
以100%抑制凝集(完全不凝集)的被检血清最大稀释度为该血清的血凝抑制效价,即HI效价。凡被已知新城疫阳性血清抑制血凝者,该病毒为新城疫病毒。
从表4-2看出,该血清的HI效价为1:64,用以2为底的负对数(-log2)表示,即6log2。
附 录
1. 阿氏液(Alsever):即红细胞保养液
枸橼酸钠(5H2O) 0.80g
枸橼酸(H2O) 0.055g
葡萄糖 2.05g
氯化钠 0.42g
双蒸水 加至 100 ml
将以上试剂加热溶解于双蒸水中,调整pH至6.8,115℃灭菌10min,4℃保存备用。
2. 0.5% 鸡红细胞制备方法
先用灭菌注射器吸取3.8% 枸橼酸钠溶液(其量为所需血量的1/5),从鸡翅静脉或心脏采血至需要血量,置灭菌离心管内,加灭菌生理盐水为抗凝血的2倍,以2000r/min离心10min,弃上清液,再加生理盐水悬浮血球,同上法离心沉淀,如此将红细胞洗涤三次,最后根据所需用量,用灭菌生理盐水配成0.5% 鸡红细胞悬液。
3. 96孔微量反应板的清洗
将浸泡有75% 乙醇的棉签放入微量反应板的每个孔内旋转,用自来水冲洗反应板5次,再用蒸馏水冲洗3次以上,置37℃温箱中干燥。
[思考题]
1. HA和HI试验的原理是什么?
2. HI试验是不是特异的抗原抗体反应,为什么?
3. HA和HI试验有何实际应用意义?
第二篇:免疫学实验指导书
免疫学实验指导
刘佳斌编
生命科学学院
生物技术系
2005.3
实验1
动物的注射采血及血清制备
家兔采血有耳静脉采血,耳动脉放血,心脏采血和劲动脉放血法,耳缘静脉采血一般适用于只需少量血液,常用于免疫注射采少量血,测其效价,心脏采血和耳动脉采血法,耳缘静脉采血一般只适用少量采血。常用于免疫注射采少量血,测其效价。心脏采血和耳缘动脉采血可采大量血有能保存动物,从动脉可采大量,动物死去。兔一般采血20ML不影响其存活。
鸡一般用心脏采血法,每只鸡一次取血20ML,不影响其存活,经3—6个月后,可再次采血。注射途径一般有皮下、静脉、皮内和腹腔。
一、目的与内容:
(一)目的
1.学习动物不同部位的采血方法
2.练习对家兔耳静脉的注射方法
3.用离心法制备血清
(二)内容
1、鸡心脏采血
2、家兔采血
3、制备血清
二、材料与用品
(一)材料
兔、鸡
(二)用品
生理盐水、注射器、剪刀、镊子、试管、离心管、离心机
三、操作与观察
(一)鸡心脏采血
1、固定鸡腿、翅膀,拔取心脏部位羽毛,用手将鸡按定。
2、寻找内肋骨到肩胛部皮下静脉,心脏在此静脉分支下面,以食指触摸心跳,消毒,垂直刺入针头,如触及肋骨则稍后退,将针头稍后偏于胸骨,切不可硬往里插,针头向里刺入后,可感到心脏跳动。此时,针头刺入心脏,徐徐抽取血液。采血20ML取下针头,将血液放入离心管。
(二)家兔采血
1、家兔心脏采血
(1)固定兔,剪取左前胸心脏部位的毛,酒精棉球消毒皮肤。
(2)用左手食指、中指、无名指防在右胸处,轻轻向左推,将心脏推至左恻固定,拇指在胸左恻由下向上数至第三至四肋骨探测心脏搏动最剧烈处
(3)将针头从搏动处刺入心脏,若准确徐徐抽取血液,足量后拔除,再改变方向成径直刺入心脏,取血液20ML,放入离心管。
(4)家兔静脉注射,在耳缘静脉注入1ML生理盐水。
2、家兔耳缘静脉采血。
(三)制备血清
四、作业与思考
1、心脏采血关键什么?需要注意哪些问题?
2、抓兔子时为什么不能抓它的双耳?正确的抓取方法是什么?
实验2
抗原与免疫血清的制备
将抗原注射入动物体内,刺激动物的B淋巴细胞转化为浆细胞,产生特异性抗体。待其血清中累积大量抗体时,采其血液分离血清,即抗体的免疫血清。抗原量低到一定程度时,抗体不能产生或用现有方法不能测出,但超过最高限度,又对抗体产生抑制作用。本实验抗原为细菌细胞,采用每毫升含9亿个细菌比较恰当。
一、目的与内容
(一)目的
1、抗原与抗体的制备方法
2、为凝集实验制备材料
(二)内容
1、抗原的制备
2、免疫血清的制备
二、材料与用品
(一)材料
大肠杆菌,家兔
(二)用品
麦氏比浊管,试管,注射器,9号、7号针头,离心机等
0.5%的石炭酸生理盐水
三、操作与观察
(一)抗原的制备
(1) 取5ML0.5%的石炭酸生理盐水,注射大肠杆菌斜面,洗下菌台
(2) 用无菌毛细菌滴管吸取洗下的菌液,注入无菌小试管
(3) 将此含有菌液的小试管放60度水浴箱中1小时,并不时摇动。
(4) 取一与比浊管同质量的小试管,加菌液1ml,再加石炭酸生理盐水4ml(或更多,是原菌液浓度而定),混匀后各比浊管比浊。
麦氏比浊法原理:某一未知菌浓度,菌液在投射光作用下用肉眼与某一比浊管比较,如果二者透光度相同,即可目测该菌大致浓度。
(5)稀释:用0.5%的生理盐水,待菌液稀释9亿/ml,即等浊于第3支。
(二)免疫血清的制备
(1)注射动物:耳缘静脉注射抗原。
(2)14日采血1ml,分离血清,测其效价,合格即大量采血。
(3)心脏采血
(4)分离免疫血清。

四、作业与思考
1.在动物体内制备免疫血清为何要多次注射?
2.制备大肠杆菌抗原时,使用石炭酸生理盐水和加热60℃1h的目的是什么?
实验3
环状沉淀反应
可溶性抗原与相应抗体反应,在有电解质的情况下,会产生细微的沉淀,称为沉淀反应。环状沉淀反应是使抗原抗体在沉淀管内形成交界面,然后在此交界面处出现—环状乳白色沉淀物,出现此环状反应的抗原最高峰,稀释度为沉淀素效价。
一、目的与内容
(一)目的
通过沉淀素的效价测定,学习环状沉淀反应的操作方法及结果观察。
(二)内容
鸡血清与免抗鸡免疫血清发生沉淀反应。
二、材料与用品
(一)材料
鸡血清、兔血清、免抗鸡免疫血清
(二)用品
小试管、1ml吸管量筒、生理盐水
三、操作与观察
1.将鸡血清以1:25稀释,去该液1ml,用倍比稀释法稀释为各种浓度(1#1*、2# 2*……)分别表示自第1管、第2管中吸取1ml以此类推。)

2.将9个干洁小试管插在试管架上,使直立。
3.用吸管吸取1:2的免抗鸡免疫血清,加入小试管底部,每管约两滴。
4.用另一吸管吸取上面稀释的鸡血清(抗原),按下表加入各管。
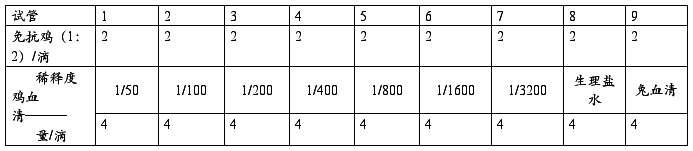
从最高峰稀释度加起,加入时沿壁徐徐加入,使与下层免抗鸡免疫血清之间形成界面,切勿摇动。
5.室温静置15—30分钟,观察试管中的两液面交界处,有无白色沉淀出现。
6.结果记录:由白色沉淀“+”,无沉淀“—”,出现沉淀最大稀释度的试管其稀释度倒数为沉淀素效价。
四、作业与思考
1.结果:

该沉淀素效价为
2.试验时为何稀释抗原,而不稀释抗体?
实验4
玻片凝集反应
细菌细胞成红细胞颗粒抗原与特异性抗体结合后,在有电解质的情况下,会出现肉眼可以看见的凝集块,称为凝集反应。玻片凝集法主要利用抗血清来鉴定未知菌,也可用来显示免疫血清的存在,这是一种定性方法。
一、目的与内容
(一)目的
1.了解血清学反应的基本原则。
2.学习玻片凝集现象。
3.观察凝集现象。
(二)内容
兔抗血清与与大肠杆菌发生凝集反应。
二、材料与用品
(一)材料
大肠杆菌、注射大肠杆菌抗原后的家兔
(二)用品
琼脂斜面、培养物、生理盐水、玻片、接种环、血清
三、操作与观察
1.采集家兔血液10ml,离心,制备抗血清。
2.以1:10用生理盐水稀释抗血清。
3.在玻片一端用小滴管加1 滴1:10抗血清,另一端加1滴生理盐水。
4.挑取少许细菌混入生理盐水中,再搅匀,挑取少许细菌混入血清,搅匀。
5.将玻片略微摆动后,静置室温中,1—3 分钟后观察一端是否有凝集反应出现,另一端为生理盐水对照,仍未均匀混合。
四、作业与思考
1.结果

2. 是否出现凝集反应,如没有分析原因?
3.为何采用生理盐水稀释血清,而不用蒸馏水?
