实验四 转氨基作用(纸层析法)
原理
氨基酸分子上的氨基转移到α-酮酸分子上的反应过程称为转氨基作用(或称氨基移换作用)。转氨基作用是氨酸代谢的重要反应之一,由转氨酶催化。经转氨后,原来的α-—氨基酸变成了相应的α-—酮酸,原来的α-—酮酸则成为新的、相应的α-—氨基酸。
本实验观察谷氨酸与丙酮酸在肌匀浆中的谷氨酸—丙酮酸转氨酶(简称GPT)的催化进行转氨基的过程。然后用纸层析法检查反应体系中丙氨酸的生成。为便于观察转氨基作用,在反应中须加一碘醋酸(或—溴醋酸),以抑制谷氨酸和丙酮酸的其它代谢过程。
试剂
1.0.9% NaCl溶液。
2.PH7.4 0.01mol/L磷酸缓冲液:取0.2mol/LNa2HPO4溶液81ml与0.2mol/LNaH2PO4溶液19ml混匀,稀释至2000ml。
3.1%谷氨酸钾溶液:取谷氨酸1g ,加水20ml,用5%KOH调到中性,然后用pH7.4 0.01mol/L磷酸缓冲液稀释至100ml。
4.1%丙酮酸钠溶液:取丙酮酸1g加pH7.4 0.01mol/L磷酸缓冲溶液溶解成100ml。
5.0.25%一碘酸钠溶液:取一碘醋酸0.25g加水1ml,用5%KOH调到中性,然后加pH7.4,0.01mol/L磷酸缓冲液成100ml。(一碘醋酸可用一溴醋酸代替)。
6.2%HAc
操作
1.肌匀浆的制备(由实验室准备室制备)
取小白兔一只,猛击头部处死后,立即剪颈放血,取肌肉若干经0.9%NaCl溶液洗去血污后,称取肌肉约100g置电动匀浆器中,再加0.01mol/LpH7.4磷酸缓冲液500ml磨成匀浆。
2.转氨基反应:取小试管2支编号,所加试剂以滴为单位。

混匀后同置40℃水浴中保温45分钟(或60分钟)。在保温过程中,时加振摇。取出两管各加入2%醋酸2滴,再同置沸水浴中5分钟,使蛋白质完全凝固,冷却后,离心(200r/min)5分钟,(或静置10分钟),将上清液作氨基酸的纸层析。
附 氨基酸的纸层析
原理
层析法又称色层分离法,原指有色物质在吸附剂上因吸附能力不同而得到分离的方法。后来此方法也应用于无色物质的分离。层析法除了吸附层析以外,还有离子交换层析、分配层析和亲和层析等。纸层析是分配层析中的一种。
分配层析是利用不同的物质在两个互不相溶的溶剂中的分配系数不同而得到分离的。通常用a表示分配系数。
溶质在固定相中的浓度(Cs)
a= —————————————
溶质在流动相中的浓度(CL)
一种物质在某溶剂系统中的分配系数,在一定的温度下是一个常数。
纸层析是以纸作为惰性支持物的分配层析,纸纤维上的羟基具有亲水性,因此以滤纸吸附的水作为固定相,而通常把有机溶剂作为流动相。有机溶剂沿着滤纸自下而上流动的,称为“上行法”;自上而下流动的,称为“下行法”。
将样品点在滤纸上(此点称为原点),进行展开,样品中的种种溶质(如各种氨基酸)即在两相溶剂中不断进行分配。由于它们的分配系数不同,不同的溶质随流动相移动的速率不等,于是就将这些溶质分离出来,形成距原点不等的层析点。
溶质在滤纸上的移动速率用Rf值表示;
原点到层析点中心的距离
Rf=———————————————————
原点到溶剂前沿的距离
只要条件(如温度、展开溶剂的组成、滤纸的质量等)不变,Rf值是常数。故可根据Rf值作定性分析。
层析后,各种溶质在滤纸上的位置可用适当的化学或物理方法处理而使其显示出来。对于氨基酸常用茚三酮使之显色。
试 剂
1.饱和水的酚:取 50 g重蒸馏酚(隔水加热溶化,量取50ml。)与25ml水,在分液漏斗中充分混匀,于暗处放置过夜(7—10小时),分成两层,收集下层清液放入棕色瓶中保存。注意:在重蒸馏和移取酚时,务必防止溅在皮肤上,若溅在皮肤上,立即用70%酒精擦洗,以免腐蚀皮肤。
2.0.1—0.25% 茚三酮丙酮(或乙醇)溶液。
3.0.1 谷氨酸溶液:将转氨基作用实验中的试剂3,用pH7.4 0.01mol/L磷酸缓冲液稀释10倍。
4.0.1丙氨酸溶液:取丙氨酸用pH7.4 0.01mol/L磷酸缓冲液配制。
操作
1.向层析缸中装入饱和水的酚(其深度约1.5cm)。
2.取宽 4.5cm,长18cm滤纸一条,(手指不可接触纸面)在滤纸条一端 2cm处划一水平线(原线),在此线上以间隔相等的距离用铅笔画四个直径约2—4mm的小圆圈,标明号码。
3.用毛细管向各小圈中央点上各种不同的氨基酸溶液,并记录之。例如:第一点为谷氨酸,第二点为丙氨酸,第三点及第四点为转氨基作用实验中的1号及2号试管溶液。点样直径以3mm为宜。

4.待干燥后可重复点样一、二次,再干燥。然后将此纸条插入上述准备好的层析缸中。先将纸条悬挂于玻璃缸内的横玻棒上(或用棉线代替),调节其高度,使纸条的下端浸入酚内约 1 cm ( 勿使氨基酸小点与溶剂直接接触),然后把盖盖紧。(如图20所示)。
图20上行法纸层析
5.经1—1.5小时,当溶剂上升至约10—15 cm高时,取出滤纸,置烘箱烘干或用电吹风吹干,使酚蒸发。
6.将已烘干的滤纸浸入茚三酮酒精溶液,再置干燥箱中烘干(或用电吹风吹干),这时在纸的不同位置上,可见紫红色的斑点出现,用铅笔描绘溶剂前沿和斑点的中心位置。
结果
计算出各氨基酸的Rf值。
附注
1.纸层析法不仅可以用于氨基酸的分离和定性,还可以用于定量测定(把紫色斑点剪下来,用硫酸铜乙醇溶液洗脱下来比色),更可以应用于糖、维生素、抗菌素、有机酸等小分子物质的分离和分析。
2.各种氨基酸在同一实验条件下(即相同的溶剂、温度、滤纸质量)各有其特有的、不变的Rf值,这是我们鉴定氨基酸的重要根据。并且同一氨基酸的Rf值也可随溶剂,滤纸质量或操作情况(如温度等)的不同而改变。例如在溶剂中Rf值相近的二种氨基酸在乙溶剂中可能Rf植相差较多。因此为了彻底分离某一混合氨基酸溶液(例如蛋白水解液),常可用更换溶剂或双向层析的方法。
第二篇:实验六 纸层析法观察转氨基作用 实验报告
实验六 纸层析法观察转氨基作用
【实验名称】:纸层析法观察转氨基作用
09救援一班 第三大组
室温:28°
(一)实验目的:
1、学习氨基酸纸层析的基本原理。
2、掌握氨基酸纸层析的操作原理。
(二)实验原理:
转氨基作用是氨基酸代谢过程中的一个重要反应,在转氨酶的催化下,氨基酸的а-酮酸与α-酮基的互换反应称为转氨基作用。转氨基作用广泛地存在于机体各组织器官中,是体内氨基酸代谢的重要途径。氨基酸反应时均由专一的转氨酶催化,此酶催化氨基酸的α-氨基转移到另一α-酮基酸上。各种转氨酶的活性不同,其中肝脏的丙氨酸氨基转移酶(ALT)催化如下反应:
α—酮戊二酸 + 丙氨酸  谷氨酸 + 丙酮酸
谷氨酸 + 丙酮酸
本实验以丙氨酸和α-酮戊二酸为底物,加肝匀浆保温后,用纸层析法检查谷氨酸的出现,以证明转氨基作用。纸层析属于分配层析。以滤纸为支持物,滤纸纤维与水亲合力强,水被吸附在滤纸的纤维素的纤维之间形成固定相。有机溶剂与水不相溶,把预分离物质加到滤纸的一端,使流动溶剂经此向另一端移动,这样物质随着流动相的移动进行连续、动态的不断分配。由于物质分配系数的差异,而使移动速度就不一样,在固定相中,分配趋势较大的组分,随流动相移动的速度就慢,反之,在流动相分配趋势较大的成分,移动速度快,最终不同的组分彼此分离,物质在纸上移动的速率可以用比值Rf表示:

物质在一定的溶液中的分配系数是一定的,故比值Rf也相对稳定,因此在同一层析体系中可用Rf值来鉴定被分离的物质。
(三)实验材料与仪器:
试剂:
1、0.01mol/L pH 7.4磷酸盐缓冲液。
2、0.2mol/L Na2HPO4溶液81ml与0.2mol/L NaH2PO4溶液19ml混匀,用蒸馏水稀释20倍。
3、0.1mol/L丙氨酸溶液称取丙氨酸0.891克,先溶于少量0.01mol/L pH 7.4磷酸盐缓冲液中,以1.0 N NaOH仔 细调至pH7.4后, 加磷酸盐缓冲液至100ml。
4 、0.1mol/Lα-酮戊二酸称取α-酮戊二酸1.461克,先溶于少量0.01mol/L pH 7.4磷酸盐缓冲液中,以1.0 N NaOH仔细调至pH 7.4 后,加磷酸盐缓冲液至100ml。
5、0.1mol/L 谷氨酸溶液称取谷氨酸0.735克,先溶于少量0.01mol/LpH 7.4磷酸盐缓冲液中,以1.0 N NaOH仔细调至pH 7.4 后, 加磷酸盐缓冲液至50 ml。
6、0.5%茚三酮溶液称取茚三酮0.5克于100 ml丙酮中溶解。
7、层析溶剂:将重蒸过的酚2份和水1份按比例混合后,放入分液漏斗中,震荡,静置24小时后分层,将下部酚层转移到瓶中备用。
仪器:玻璃匀浆器、10ml试管、培养皿、表面皿、沸水浴锅、37℃恒温水浴箱、9cm圆滤纸、烘箱、手术剪刀、分液漏斗。
(四)实验步骤:
1、肝匀浆制备:取新鲜动物肝0.5克,剪碎后放入匀浆器,加入冷0.01mol/LpH 7.4磷酸盐缓冲液1.0 ml,迅速研成匀浆, 用上述缓冲液4.5ml混匀备用。
2、 酶促反应过程
(1)取离心管两支,编号:1(测定管)、2(对照管),各加肝匀浆0. 5ml。把对照管放沸水浴中加热10分钟,取出冷却。
(2)各加0.1mol/L丙氨酸0.5 ml, 0.1mol/Lα-酮戊二酸0.5 ml,0.01mol/L pH 7.4磷酸盐缓冲液1.5 ml,摇匀。
(3)37℃保温,30分钟后取出,保温完毕。
(4)把测定管放沸水浴中煮10分钟,取出后冷却,过滤。
3、层析
(1)取圆形滤纸一张(直径9cm)放洁白纸上,以圆点为中心,约1 cm为半径,用铅笔划一圆线作为基线,在线上四等份处标清四点编号作为点样原点。
(2)点样:用四根毛细玻璃管分别进行点样。把丙氨酸液、谷氨酸液分别点在原点2、4处。把测定液、对照液分别点在原点1、3处。注意斑点不宜过大(应在直径0.5cm以下)。在第一次点样点干后,再在原处同样点第2次。
(3)层析:先在滤纸圆心处打一小孔(铅笔芯粗细),再取滤纸一条卷成捻如灯芯状,上端插入滤纸中心孔中,下端剪成须状。
(4)把滤纸平放在上述培养皿上,使纸芯下浸入层析液中,盖上培养皿盖。可见层析液沿纸芯上升到滤纸中心,渐向四周扩散。当层析液前缘到离滤纸边缘约1cm时,约25分钟,取出滤纸,用镊子小心取下纸芯,放入烘箱中烘干。
(5)显色:将上述滤纸平放在培养皿上,滴0.5%茚三酮的丙酮溶液,使滤纸全部湿润,再放入烘箱干燥,此时可见紫色斑出现,比较色斑的位置,及色泽深浅,计算Rf值,分析是否发生了转氨基反应。
(五)实验结果记录:
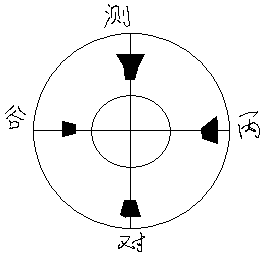 图(1)
图(1)
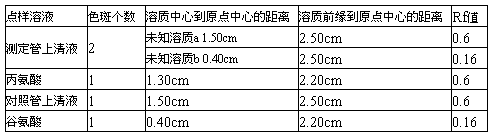
表格(1)
(六)实验讨论:
1、从表格(1)中可以看出,测定管上清液点样出现了两个色斑,根据Rf值的计算也可以看出,测定管中氨基酸发生了转氨基作用,生成的未知物质b为谷氨酸,则未知溶质a为丙氨酸;对照管中因为酶的失活而没有发生转氨基反应,只有丙氨酸,所以色斑只有一个。
2、层析点样时手要洗净,操作中尽可能少量接触滤纸,以免污染。
3、层析液中含有腐蚀性酚,取用时注意安全,防止溅到皮肤及眼睛。
4、点样点不宜过大,直径小于0.5cm.
20##年9月19日
