合水一中2009-2010学年第一学期高二化学期中试题
(文 科)
班级________ 姓名____________ 得分__________
可能采用的相对原子质量:H-1,C-12,N-14,O-16,Na-23,S-32
一、选择题(共25题,每题2分,共计50分。每小题只有一个选项符合题意,不选、多选、错选均不给分。)
1.N2的化学性质很不活泼,其原因是( )
A.N元素的非金属很弱
B.N原子结构很稳定
C.N2分子是由非极性键构成的双原子分子
D.N2分子中有三个共价键,键能很大
2.下列气体中,只能用排水集气法的是( )
A.CO2 B.NO C.NO2 D.H2
3.常温下能用铝制容器盛放的是( )
A.浓盐酸 B.浓硝酸 C.稀硫酸 D.稀硝酸
4.常用来干燥NH3的物质是( )
A. 碱石灰 B.浓H2SO4 C.P2O5 D.CaCl2
5.某一反应物的浓度是2.0mol/L,经过30s后,它的浓度变成了0.8mol/L,在这20s内它的反应速率为( )
A.0.04 B.0.04mol/ (L·s) C.0.8mol/ (L·s) D.0.04mol/L
6.下列气体不会造成空气污染的是( )
A.N2 B.NO2 C.NO D.CO
7.下列物质的水溶液,呈碱性的是( )
A.Na2SO4 B.AlCl3 C.Na2CO3 D.KNO3
8.下列反应中,显示出硝酸强氧化性的是( )
A.氧化铁与浓硝酸反应 B.碳酸钠与硝酸反应
C.碳与浓硝酸反应 D.氢氧化铜与稀硝酸反应
+9.检验某固体样品中是否含有NH4的方法是,先取少量固体于试管中,然后( )
A.加热,用湿润红色石蕊试纸在试管口检验
B.加水溶解,用红色石蕊试纸检测溶液酸碱性
C.加入弱碱溶液,加热,滴入酚酞试剂
D.加入烧碱溶液,加热,用湿润红色石蕊试纸在试管口检验
10.下列离子方程式中,能正确反映CH3COOH与NaOH反应的是( )
A.CH3COOH+OH

-
B.H++OH-===H2O CH3COO-+H2O
1
C.CH3COOH+Na++OH-===CH3COONa+H2O
D.CH3COO-+H++OH-===CH3COO-+H2O
11.下列物质中,既能与氨反应,又能与二氧化碳反应的是( )
A.氢氧化钠 B.氯化氢 C.氧气 D.水
12.能将NH4Cl、(NH4)2SO4、NaCl、Na2SO4四种溶液一一区分的试剂是( )
A.NaOH溶液 B.AgNO3溶液 C. Ba(OH)2溶液 D. BaCl2溶液
13.在24mL0.1mol/LH2SO4溶液中加入12mL0.4mol/LKOH溶液时,所得到的溶液呈( )
A.弱酸性 B.强酸性 C.碱性 D.中性
14.在一定条件下,对于密闭容器中进行的反应:P(g)+

Q(g) R(g)+S(g)
下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
A.P、Q、R、S的浓度相等
B.P、Q、R、S在密闭容器中共存
C.P、Q、R、S的浓度不再变化
D.用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等
15.在一定条件下,发生CO+NO2

CO2+NO的反应,达到化学平衡后,降低温度,混
合物的颜色变浅,下列有关该反应的说法中正确的是( )
A.正反应为吸热反应 B.正反应为放热反应
C.降温后CO的浓度增大 D.降温后各物质的浓度不变
16.制取相同质量的Cu(NO3)2时,消耗硝酸质量最多的是( )
A.铜与浓HNO3反应 B.铜与稀硝酸反应
C.氧化铜与硝酸反应 D.氢氧化铜与硝酸反应
17.在一定条件下,SO2和O2在一密闭容器中进行反应,下列说法中错误的是( )
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.随着反应的进行,正反应速率逐渐减小,最后不变
18.下列电离方程式书写正确的是( )
A.

NaOH Na+ + OH- B.Na2SO4 == Na2+ + SO42-
C.CH3

COOH H+ + CH3COO- D. H2CO3 ==2H+ + CO32-
19.农业及城市生活污水中含磷,家用洗涤剂就是污水中磷的一个重要来源(洗涤剂中含有
磷酸钠).处理污水时要不要除去磷,有以下几种意见,你认为正确的是( )
A.磷是生物的营养元素,不必除去
B.含磷的污水是很好的肥料,不必处理
C.含磷的污水排放至自然水体中能引起藻类增殖,使水变质,必须除去
D.磷对人无毒,除去与否无关紧要
20.下列各反应的化学方程式中,属于水解反应的是( )
2
21.将一定浓度的盐酸倒入碳酸钙粉末里,若作下列改变,其中能使最初的化学反应速
率加快的是 ( )
A.盐酸的浓度不变,而使盐酸的用量增加一倍
B.盐酸的浓度增加一倍,而盐酸的使用量减至原来的二分之一
C.盐酸的浓度和使用量都不变,增加碳酸钙粉末的量
D.使反应在较低的温度下进行
22.氨溶于水中,所得溶液中除水分子外,数量最多的微粒是( )
A.NH3 B.NH3·H2O C.NH4+ D.OH-
23.0.3molCu与足量的稀HNO3完全反应时,被还原的HNO3的物质的量是( )
A.0.8mol B.0.6mol C.0.4mol D.0.2mol
24.在一支25mL的酸式滴定管中盛入0.1mol/L HCl溶液,其液面恰好在5mL刻度处。若把滴定管内溶液全部放入烧杯中,再用0.1mol/L NaOH溶液进行中和,则所需NaOH溶液的体积( )
A.大于20mL B.小于20mL C.等于20mL D.等于5mL
25.砷为第四周期ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是
( )
A.砷在通常状况下是固体 B.可以有-3,+3,+5等多种化合价
C.As2O5对应水化物的酸性比H3PO4弱 D.砷的还原性比磷弱
二、填空题(本大题包括5小题,共26分)
26.(6分)写出下列反应的化学方程式
(1)氨催化氧化 ;
(2)硫酸铵溶液与氢氧化钠溶液共热 ;
(3)铜与浓硝酸反应 。
27.(6分)现有可逆反应A(气)+B(气)3C(气),下图中甲、乙、丙分别表示在不同的条
件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则___曲线是表示有催化剂
时的情况。
(2)若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是____
热反应。
(3)若丙图中两条曲线分别表示不同压强下的情况,则
28.(4分)在高温下,下列反应达到平衡:C(s)+H2

O(g)
3 CO(g)+H2(g)(
正反应为放热反
应)如果升高温度,平衡向 移动;如果增大压强,平衡向 移动。
29.(4分)实验室配制FeCl3溶液时,溶液常常产生浑浊,请你分析产生这种现象的原因是__ (用离子方程式表示);现欲配得澄清的FeCl3溶液,可以采取的方法是 。
30.(6分)在25℃时,纯水中c(H)·c(OH;在酸性溶液中,c(H10mol·L(<,>或=);在碱性溶液中,pH 7 (<,>或=) 。
三、简答题(本大题包括2小题,共12分)
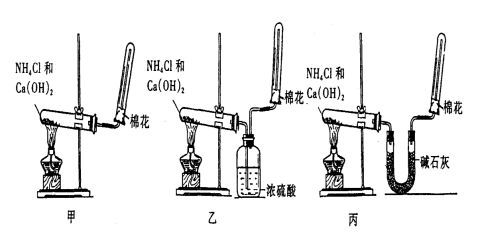
31.(6分)为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验
装置 +-+-7-1
(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) 。(1分)
(2)(2分)
(3)如何检验氨气是否收集满(简述操作方法、现象和结论(3分)
32.(6分)在小烧杯中加入水,再滴入0.1mol/LFeCl3溶液、0.1mol/LKSCN溶液各1滴,将充分混合的溶液平均地分别倒入3支试管中。
向试管1里加入几滴0.1mol/LFeCl3溶液,向试管2里加入几滴0.1mol/LKSCN溶液,分别将上述2支试管与第3支试管相比较,观察溶液颜色的变化。试回答下列问题:
(1)试管1与第3支试管相比较,溶液颜色的变化如何? 。
(2)试管2与第3支试管相比较,溶液颜色的变化如何? 。
(3)根据上述实验现象说明浓度对化学平衡的影响 。
四、计算题(本大题包括2小题,共12分)
33.(6分)在(NH4)2SO4中加入足量的NaOH溶液,加热,充分反应后产生4.48L气体(标
准状况).求(NH4)2SO4的质量。
34.(6分)用1体积的水吸收560体积(标准状况)氨,所得氨水的密度为0.89g?mL-1。计
算①氨水中溶质的质量分数②氨水的物质的量浓度(写出算式,只写答案不给分) (注:只交答题卡)
4
高二化学期中考试答题卡(文)
班级________ 姓名____________得分__________
一、选择题(本题包括25个小题,每小题2分,共50分。每小题只有一个
选项符合题意。)
二、填空题:(本题共26分) 26

.(6分)
⑴

。 ⑵ 。 ⑶ 。 27.(6分)
⑴ ;⑵ ;⑶ 。 28.(4分) , 。
29.(4分)原因,
方法 。 30. (6;。
三、简答题:(本题共12分) 31.(6分)
(1) ;
(2)________ __________;
5
(3) ________________________。
32.(6分)
(1) ;
(2) ;
(3) 。
四、计算题(本题共12分)
33.(6分)
34.(6分)

6
第二篇:高二化学选修第二学期期中考试试卷
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
高二化学(选修)第二学期期中考试试卷
命题人:孙明林 李大宁
注意事项:
1. 第I卷64分,第II卷56分,共120分,考试时间为100分钟。
2. 请将答案统一填写在答题纸上。可能用到的相对原子质量:
H—1 C—12 N—14 O—16
第I卷
一、选择题(每小题只有一个选项符合题意.3分×8题=24分)
1.第一次用无机物制备有机物尿素,开辟人工合成有机物先河的科学家是( )
A.德国的维勒 B.英国的道尔顿
C.德国的李比希 D.俄罗斯的门捷列夫
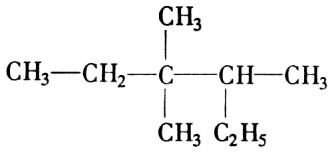
2.有机物 的正确命名为 ( )
A.2—乙基—3,3—二甲基戊烷 B.3,3—二甲基—4—乙基戊烷
C.3,3,4—三甲基已烷 D.2,3,3——三甲基已烷
3.下列有关说法不正确的是
A.具有相同通式的有机物不一定互为同系物
B.分子组成相差一个或若干个CH2原子团的化合物一定互为同系物
C.分子式为C3H8与C6H14的两种有机物一定互为同系物
D.两个相邻同系物的相对分子质量数值一定相差14
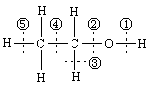
4. 乙醇分子结构中各种化学键如右图所示,关于乙醇在各种反应中断裂键的说明不正确的是
A.和金属钠反应是键①断裂
B.和浓硫酸共热到170℃时断键②和⑤
C.和浓硫酸共热到140℃时断键②,其它键不断
D.和浓氢溴酸混合加热时断键②
5.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为
HC≡C—C≡C-C≡C-C≡C-C≡N.对该物质判断正确的是:
A.晶体的硬度与金刚石相当 B.能使酸性高锰酸钾溶液褪色
3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
C.不能发生加成反应 D.不能使溴水褪色
6.以下实验能获得成功的是
A.用酸性KMnO4溶液鉴别乙烯和乙炔
B.将铁屑、溴水、苯混合制溴苯
C.在苯和硝基苯采用分液的方法分离
D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
7、由溴乙烷制取乙二醇,依次发生反应的类型是
A.消去、加成、水解 B.取代、加成、水解
C.水解、消去、加成 D.消去、水解、取代
8.要检验某溴乙烷中的溴元素,正确的实验方法是
A.加入溴水振荡,观察水层是否有棕红色出现
B.滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无浅
黄色沉淀生成
D.加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成
二、选择题(共8题,每小题有1—2个选项符合题意.4分×10=40分)
9.设阿伏加德罗常数为NA,则下列说法正确的是
A.15g甲基(-CH3)所含有的电子数是NA
B.常温常压下,4g氦气所含有的原子数目为NA
C.标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA
D.常温常压下,1mol丙烷所含有的共价键数目为12NA
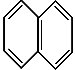
10.
)的同系物。则萘和萘的同系物分子组成通式是:
A.CnH2n-6(n≥11) B.CnH2n-12(n>10)
C.CnH2n-10(n≥10) D.CnH2n-12(n≥10)
11.下列各醇中,能发生消去反应生成(CH3)2C==CH2且能发生催化氧化的是
CH2OH
A.CH3-OH B.CH 3 H
CH3
C. D. 都属于萘(
结构简式:
12.描述CH3—CH==CH—C≡C—CF3分子结构的下列叙述中,正确的是
A.6个碳原子有可能在一条直线上 B.6个碳原子一定都在同一平面上 3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
C.此分子最多有8个原子在同一平面上 D.此分子至少有8个原子在同一平面上
13.下列各组混合物中,不论两种物质以何种比例混合,只要总物质的量一定,经过完全燃烧后,产生的CO2质量不变的是
A.乙炔和苯 B.甲醛(HCHO)与葡萄糖(C6H12O6)
C.乙醇和乙酸 D.丙烯和丙烷
14.两种气态烃的混合物共0.1 mol ,充分燃烧后得3.58 L(标准状况下)CO2和3.6 g水,下列说法正确的是
A.一定有甲烷 B.一定有乙烯 D.可能有乙烷 D.可能有丙炔
15.下列化学式及结构式中,从成键情况看不合理的是
HHA.CH3N B.CH4Si D.CH4S H
16.工业上将苯的蒸气通过赤热的铁能合成一种可作传热载体的化合物。该化合物分子中苯环上的一氯代物有3种。1mol该化合物催化加氢时最多消耗6molH2。这种化合物可能是 C.CH2SO S A. B. C. D.
17.利用某些有机物的同分异构体间的转化可用来贮存热能,如原降冰片二烯(NBD)经太阳照射后转化成四环烷(Q)的的反应:△H=+88.62kJ·mol —1
下列说法不正确的是: ...
A.NBD、Q、甲苯三者互为同系物 B. NBD、Q、甲苯三者是同分异构体
C.92gNBD经太阳照射后完全转化为Q时需吸收88.62kJ热量 D.NBD可开发为贮能材料
18.为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂。已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示。下列叙述中正确的是
A、该物质可以视为酚类
B、在浓硫酸作用下,分子内消去一个水分子,产物有二种同
分异构体
C、能使溴的四氯化碳溶液褪色
3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
D、该物质分子中的所有碳原子均共面
第II卷
三.实验题 (共18分)
19.(4分)下列叙述正确的是________________(选对一个给2分,多选、错选一个扣1分,本题不出现负分)。
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗。
B.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体。
C.浓溴水滴入苯酚溶液中立即产生2,4,6-三溴苯酚的白色沉淀。
D.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,但该现象不能说明苯和溴的取代反应就是放热反应。
E.分离沸点相差30℃以上的混溶液体,应采用的方法是分馏
F.实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃。
G.除去混在苯中的少量苯酚,加入过量溴水,过滤。
20. (14分)为探究实验室制乙烯及乙烯和溴水的加成反应。甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验
目的。
乙同学仔细考察了甲同学的整个实验过程,发现当
温度升到100℃左右时,无色液体开始变色,到160℃
左右时,混合液全呈黑色,在170℃超过后生成气体速
度明显加快,生成的气体有刺激性气味。由此他推出,
产生的气体中应有杂质,可能影响乙烯的检出,必须除
去。据此回答下列问题:
(1)写出甲同学实验中两个反应的化学方程式:
___________________________、__________________________。
(2)乙同学观察到的黑色物质是_____________,刺激性气体是_____________。乙同学认为刺激性气体的存在就不能认为溴水褪色是乙烯的加成反应造成的。原因是(用化学方程表示):_____________________。
(3)丙同学根据甲乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净)
:发现最后气体经点燃3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
是蓝色火焰,确认有一氧化碳。
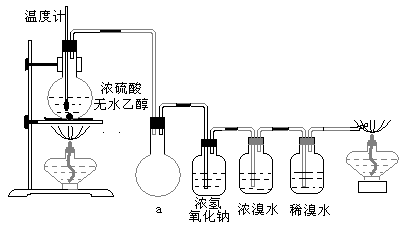
①设计装置a的作用是____________________
②浓溴水的作用是_______________________,稀溴水的作用是____________________。
四、填空题。(共22分)
21.(8分)按要求完成下列问题
(1)甲基的电子式(2)通式为CnH2n+2的最简单同系物的分子式
(3)相对分子质量为72且沸点最低的烷烃的结构简式 _____________________
(4)1,3-丁二烯的键线式
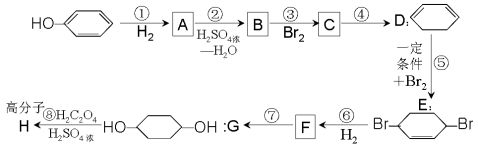
22.(14分)按以下步骤可从
已略去).
请回答下列问题:
(1)B、F的结构简式为:B F 。
(2)反应①~⑦中属于消去反应的是 (填代号)。
(3)根据反应,写出在同样条件下 合成(部分试剂和反应条件
CH2=CH—CH=CH2与等物质的量Br2发生加成反应的化学方程式:
3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
(4)写出第④步的化学方程式(有机物写结构简式,注明反应条件).
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号) 。 (6)核磁共振谱是测定有机物分子结构最有用的工具之一。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)
HO
H可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为: H,其
PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是 。
A. B. C. D.
五、计算题(共16分)
23.一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25。使混合气通过足量溴水,溴水增重8.4g。通过计算回答:
① 混合物的物质的量
② 混合物的组分、体积之比
24.现有A、B两种链状饱和一元醇的混合物0.3 mol,其质量为13.8g。已知①A和B碳
原子数均不大于4,且A<B;②A和B分子中均不含有支链,且都能被催化氧化生成醛。
(1)混合物中A可能的分子式;B可能的分式。
(2)若n(A):n(B)=1:1时,A的名称;B的名称
(3)若n(A):n(B)≠1:1时,
A的结构简式为 B的结构简式为 则n(A):n。
3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
3eud教育网 百万教学资源,完全免费,无须注册,天天更新!
3eud教育网 教学资源集散地。可能是最大的免费教育资源网!
