实验二 硫酸铜的提纯
实验目的
1、了解化学方法提纯粗硫酸铜的原理和方法。
2、练习无机制备的基本操作。
实验原理
粗硫酸铜中含有不溶性杂质和可溶性杂质FeSO4、Fe2(SO4)3等,不溶性杂质可用过滤法除去,杂质FeSO4需要用氧化剂H2O2或Br2氧化为Fe3+,然后调节溶液的pH值4,使Fe3+水解成Fe(OH)3沉淀而除去,其反应如下:
2FeSO4 + H2SO4 + H2O2= Fe2(SO4)3 + 2H2O
Fe3++ 3H2O → Fe(OH)3↓ + 3H+
除去铁离子之后的滤液,蒸发结晶,其它微量可溶性杂质在硫酸铜结晶时仍留在母液中,过滤时可与硫酸铜分离。
实验步骤
称取5g研细的粗硫酸铜放在100mL小烧杯中,加入20mL蒸馏水,加热搅拌促使溶解.
滴加1 mL 3% H2O2,将溶液加热,同时逐滴加入0.5 mol?L-1NaOH溶液,直到pH≈4,再加热片刻静置使水解生成Fe(OH)3沉淀用倾斜法在普通漏斗上过滤,滤液过滤到洁净的蒸发皿中。
在提纯后的硫酸铜滤液中,滴加1mol?L-1 H2SO4酸化,调节pH至1~2,然后在石棉网上加热,蒸发浓缩至液面出现薄层结晶时,即停止加热。
冷却至室温,结晶在漏斗上过滤,并用一干净的玻璃棒轻压漏斗上的晶体,以除去其中少量的水分。硫酸铜固体再用滤纸吸干水分。
取出晶体,把它夹在两张滤纸中,吸干表面的水分。
在台秤上称出产品质量,计算产率。
硫酸铜回收率 = (精硫酸铜质量/粗硫酸铜质量)×100%
思考题
1、粗硫酸铜溶液中杂质Fe2+为什么要氧化为Fe3+除去?
2、除Fe3+时,为什么要调节到pH≈4左右?pH值太小或太大有什么影响?
注意事项
1、注意各步的pH值控制。
2、蒸发浓缩时,要小火加热。
3、注意滤纸的使用。
第二篇:硫酸铜的提纯1
硫酸铜的提纯
实验目的:
1.了解用重结晶法提纯物质的原理;
2.学习常压过滤、减压过滤、以及称量、加热、溶解、溶液转移、蒸发、浓缩等基本操作。
实验原理:
粗硫酸铜中含有不溶性杂质和可溶性杂质离子Fe2+、Fe3+等,不溶性杂质可用过滤法除去。可溶性杂质离子Fe2+常用氧化剂H2O2或Br2氧化成Fe3+,然后调节溶液的pH值(一般控制在pH=3.5~4),使Fe3+水解成为Fe(OH)3沉淀而除去,反应如下:
2 Fe2+ + H2O2 + 2 H+ = 2 Fe3+ + 2 H2O
Fe3+ + 3 H2O = Fe(OH)3↓十3 H+
除去铁离子后的滤液经蒸发、浓缩,即可制得五水硫酸铜结晶。其它微量杂质在硫酸铜结晶时,留在母液中,过滤时可与硫酸铜分离。
仪器、试剂和材料:
仪器:台秤 漏斗和漏斗架 布氏漏斗 吸滤瓶 蒸发皿
药品:粗CuSO4 H2O2 (3%) H2SO4 (1moI·L-1) , NaOH (2 moI·L-1) ,
其它:滤纸 pH试纸 精密pH试纸(0.5~5.0)
实验步骤:
称取5g由实验室提供的粗CuSO4放在小烧杯中,加入大约30ml蒸馏水,搅拌,促使其溶解。再滴加2m1 3% H2O2,将溶液加热,使Fe2+氧化成Fe3+;用精密pH试纸测试溶液pH值,如果氧化后溶液的pH值很低,这时可在不断搅拌下,逐滴加入0.5~l mol·L-1 NaOH,直到pH=3.5~4,再加热,静置使Fe3+水解生成的Fe(OH)3沉淀,常压过滤,滤液转移到洁净的蒸发皿中。
在精制后的硫酸铜滤液中滴加l mol·l-1 H2SO4酸化,调节pH至l~2,然后加热蒸发 (注意加热时间不要太长),当浓缩至液面出现一层晶膜时,即停止加热,然后冷却至室温,抽滤,当抽至没有水滴时,停止抽滤,取出CuSO4晶体,称量,记录,回收产品。
数据记录与数据处理:

结果与讨论:
思考题:
1.在调节溶液pH值时要注意哪些方面?
2.粗硫酸铜中杂质Fe2+为什么要氧化为Fe3+后再除去? 而除去Fe3+时,为什么要调节溶液的pH值为4左右?pH值太大或太小有什么影响?
3.精制后的硫酸铜溶液为什么要滴几滴l mol·L-1 H2SO4酸化,然后再加热蒸发?
4. KMnO4、K2Cr2O7、Br2、H2O2都可使Fe2+氧化为Fe3+,你认为选用哪种氧化剂较为合适,
为什么?
5. 如何检验CuSO4溶液中少量Fe3+?
注意事项:
粗硫酸铜晶体要充分溶解
pH值的调整
滤纸折叠的方法

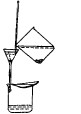
倾泻法过滤操作的要领

浓缩、结晶程度的掌握
抽滤操作
