五水合硫酸铜结晶水的测定 教案
讲授
先将沙浴开了。
总结实验报告,对不合格的要求重新写。
复习分析天平的使用,称量方法,有那几种?
一、实验目的:
1.了解结晶水合物中结水含量的测定原理和方法。
2.进一步熟悉分析天平的使用,学习研钵、干燥器等仪器的使用和沙浴加热、恒重等基本操作。
二、原理
很多离子型的盐类从水溶液中析出时,常含有一定量的结晶水(或称水合水)。结晶水与盐类结合得比较牢固,但受热到一定温度时,可以脱去结晶水的一部分或全部。
五水合硫酸铜晶体在不同温度下按下列反应逐步脱水: 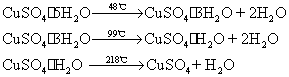
无水硫酸铜为白色或灰白色粉末。问题:无水硫酸铜什么颜色?
蓝色表明有什么?
因此对于经过加热能脱去结晶水,又不会发生分解的结晶水合物中结晶水的测定,通常是把一定量的结晶水合物(不含附水)置于已灼烧至恒重的坩埚中,加热至较高温度(以不超过被测定物质的分解温度为限)脱水,然后把坩埚移入干燥器中,冷却至室温,再取出用分析天平称量。由结晶水合物经高温加热后的失重值可算出该结晶水合物所含结晶水的质量分数,以及每物质的量的该盐所含结晶水的物质的量,从而可确定结晶水合物的化学式。由于压力不同、粒度不同、升温速率不同,有时可以得到不同的脱水温度及脱水过程。
∵
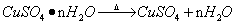
1mol 1mol n mol
∴ 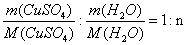
∴ 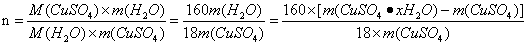
三、基本操作:
1. 分析天平的使用
分析天平的称量方法。
2. 沙浴加热(页码:26)
加热是实验室中常用的实验手段,有煤气灯、水浴、沙浴、电加热套、电炉、管式炉和马福炉加热(复习加热方法)。
油浴和沙浴加热(间接加热)
当被加热物质要求受热均匀,温度又高于100℃时,可用油浴或沙浴。油浴加热与水浴加热方法相似。沙浴是在铁制沙盘中装入细沙,将被加热容器下部埋在沙中,用煤气灯或电炉加热沙盘。沙浴温度可达300~400 ℃。
3.研钵的使用方法(演示)
研钵就是实验中研碎实验材料的容器,配有钵杵,常用的为瓷制品,也有玻璃、玛瑙、氧化铝、铁的制品。用于研磨固体物质或进行粉末状固体的混和。其规格用口径的大小表示。
进行研磨操作时应注意:
(1)按被研磨固体的性质和产品的粗细程度选用不同质料的研钵。一般情况用瓷制或玻璃制研钵,研磨坚硬的固体时用铁制研钵,需要非常仔细地研磨较少的试样时用玛瑙或氧化铝制的研钵。注意,玛瑙研钵价格昂贵,使用时应特别小心,不能研磨硬度过大的物质,不能与氢氟酸接触。
(2)进行研磨操作时,研钵应放在不易滑动的物体上,研杵应保持垂直。大块的固体只能压碎,不能用研杵捣碎,否则会损坏研钵、研杵或将固体溅出。易爆物质只能轻轻压碎,不能研磨。研磨对皮肤有腐蚀性的物质时,应在研钵上盖上厚纸片或塑料片,然后在其中央开孔,插入研杵后再行研磨,研钵中盛放固体的量不得超过其容积的1/3。
(3)研钵不能进行加热,尤其是玛瑙制品,切勿放入电烘箱中干燥。
(4)洗涤研钵时,应先用水冲洗,耐酸腐蚀的研钵可用稀盐酸洗涤。研钵上附着难洗涤的物质时,可向其中放入少量食盐,研磨后再进行洗涤。
若研磨材料用于提取DNA或RNA,用锡纸包裹后于烘箱内180度灭菌。
4、干燥器的准备和使用(演示)
由于空气中总含有一定量的水汽,因此灼烧后坩埚和沉淀等,不能置于空气中,必须放在干燥器中冷却以防吸收空气中的水分。
干燥器
结构 是一种具有磨口盖子的厚质玻璃器皿,磨口上涂着一薄层凡士林,使其更好地密合,底部放适当的干燥剂,其上架有洁净的的带孔瓷板,以便放置坩埚和称量瓶等。
使用 准备干燥器时要用干的抹布将内壁和磁板擦抹干净,一般不用水洗,以免不能很快干燥。放放干燥剂时,干燥剂不要放得太满,装至干燥器下室的一半就够了,太多容易玷污坩埚。
开启干燥器时,应左手按住干燥器的下部有右手握住盖的圆顶,向前小心推开器盖。盖取下时,将盖倒置在安全处。
放入物体后,应及时加盖。加盖时也应该拿住盖上的圆顶推盖严。当放入温热的坩埚时,应将盖留一缝隙,稍等几分钟再盖严;也可以前后推动器盖稍稍打开2~3次。搬动干燥器时,应用两手的拇指按住盖子,以防盖子滑落打碎。
四、实验内容
1.恒重坩埚
将一洗净的坩埚及坩埚盖置于泥三角上。小火烘干后,用氧化焰灼烧至红热。将坩埚冷却至略高于室温,再用干净的坩埚钳将其移入干燥器中,冷却至室温(注意:热坩埚放入干燥器后,一定要在短时间内将干燥器盖子打开1~2次,以免内部压力降低,难以打开)。取出,用电光天平称量。重复加热至脱水温度以上、冷却、称量,直至恒重。
2.水合硫酸铜脱水
(1)在已恒重的坩埚中加入1.0~1.2g研细的水合硫酸铜晶体(什么方法?),铺成均匀的一层,再在电光天平上准确称量坩埚及水合硫酸铜的总质量(什么方法?),减去已恒重坩埚的质量即为水合硫酸铜的质量。
(2)将已称量的、内装有水合硫酸铜晶体的坩埚置于沙浴盘中。将其四分之三体积埋入沙内,再靠近坩埚的沙浴中插入一支温度计(300℃),其末端应与坩埚底部大致处于同一水平。加热沙浴至约210℃,然后升温至280℃左右,调节煤气灯以控制沙浴温度在260~280℃之间.当坩埚内粉末由蓝色全部变为白色时停止加热(约需15~20min)。用干净的坩埚钳将坩埚移入干燥器内,冷至室温。将坩埚外壁用滤纸揩干净后,在电光天平上称量坩埚和脱水硫酸的总质量。计算脱水硫酸铜的质量。重复沙浴加热,冷却、称量,直到“恒重”(本实验要求两次称量之差小于等于1mg)。实验后将无水硫酸铜倒入回收瓶中。
思考题
- 在水合硫酸铜结晶水的测定中,为什么沙浴加热并控制温度在280℃左右?
- 加热后的坩埚能否未冷却至室温就去称量?加热后的热坩埚为什么要放在干燥器内冷却?
- 在高温灼烧过程中,为什么必须用煤气灯氧化焰而不能用还原焰中热坩埚?
- 为什么要进行重复的灼烧操作?为什么叫恒重?其作用是什么?
五、实验报告
参考,这是个什么类型的实验?
有效数字表达结果。
进行误差分析,绝对及相对。
实验注意事项
- 五水合硫酸铜的用量最好不要超过1.2 g
- 加热脱水一定要完全,晶体完全变为灰白色,不能是浅蓝色。
- 注意恒重
- 注意控制脱水温度
下周:容量瓶的相对校准
实验 五水合硫酸铜结晶水的测定
姓名_____________ 班级________________ 学号________________ 日期_______________
一、实验目的
二、实验原理
利用结晶水受热到一定温度时可以脱去结晶水的一部分或全部的方法。
CuSO4·5H2O晶体在不同温度下的逐步脱水:
∵
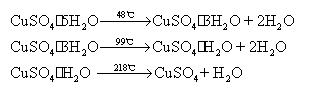
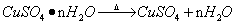
1mol 1mol n mol
∴ 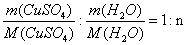
∴ 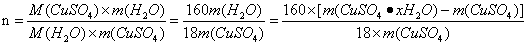
三、实验步骤
1、研磨:在_________中将硫酸铜晶体研碎(___________________________)。
2、称量:准确称量__________________的质量,并记录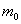 。
。
3、加样:在瓷坩埚中加入约 克的硫酸铜晶体,称量并记录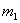 。
。
4、加热:把盛有硫酸铜晶体的瓷坩埚用__________________放在泥三角上慢慢加热,直到蓝色完全变白(___________________________),然后把坩埚移至__________________中冷却至室温。
5、称量:称量并记录加热后___________________________的质量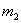 。
。
6、恒重操作:将盛有无水硫酸铜的坩埚再一次加热2分钟,放在干燥器中冷却后,再次进行称量,并记录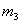 ,直到两次称量的结果(
,直到两次称量的结果(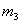 —
—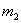 )相差不超过0.001g。
)相差不超过0.001g。
四、实验数据记录及处理
设硫酸铜晶体的化学式是: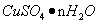

n的计算式: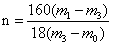
结论:硫酸铜晶体的化学式是____________________。
五、误差及其分析
理论值:1mol硫酸铜晶体中含有5.00 mol 水。
绝对误差:___________________;
相对误差:______________________。
八、实验小结
第二篇:无机化学实验教案
实验一 灯的使用,玻璃管操作及塞子的钻孔
[实验目的]:了解煤气灯或酒精灯、酒精喷灯的构造并掌握正确的使用方法; 学会截、弯、拉、熔烧玻璃管的操作,制作玻璃棒、滴管和弯管;练习塞子钻孔
的
基本操作。
[实验用品] 仪器:煤气灯 酒精灯 酒精喷灯 石棉网 锉刀 打孔器 直角
器
液体药品:工业酒精 95%酒精
材料:火柴 玻璃管 橡皮胶头 玻璃棒 橡皮塞
[建议]添置煤气灯,适用的喷灯
实验二 台秤与分析天平的使用,溶液的配置
[实验目的]了解台秤与分析天平的基本构造,学习正确的称量方法;了解使用 天平的规则;学习比重计、移液管、容量瓶的使用方法;掌握溶液的质量分数, 质量摩尔浓度,物质的量的浓度等一般配置方法和基本操作;了解特殊溶液的 配置。
[实验用品]仪器:台秤 分析天平 称量瓶 药匙 烧杯 移液管 容量瓶 比重计 量筒 试剂瓶 称量瓶
固体药品:氧化铜(干燥) CuSO4·5H2O NaCl NaOH
液体药品:弄盐酸 浓硫酸 醋酸 硝酸
[强调]:要求学生明确配置粗略浓度和精确浓度溶液的差别点:1)所用的称量 仪器不同。粗配时一般要用台秤即可,精配需用分析天平。2)所用稀释容器不
同。
粗配用烧杯,量筒,试剂瓶即可,精确配置需用容量瓶,比重计。
实验三 滴定操作练习
[实验目的]掌握酸碱滴定的原理;掌握滴定的操作,学会正确判断滴定终点。
[实验用品]仪器:碱式滴定管 25ml移液管 锥形瓶 量筒(10ml)
液体药品:0.1ml/LHCl标准溶液(准确浓度已知)0.1mol/LNaOH溶
液
(浓度待定)0.1mol/LHAc溶液(浓度待定) 酚酞溶液(质量分数为0.01)
实验四 二氧化碳相对分子量的测定
[实验目的]学习气体相对密度法测定相对分子质量的原理和方法;加深理解理想 气体状态方程式和阿佛加德罗定律;巩固使用启普发生器和熟悉洗涤、干燥气体 的装置。
[实验用品]仪器:分析天平 启普发生器 台秤 洗气瓶 干燥管 磨口锥形瓶
固体药品:石灰石 无水氟化钙
液体药品:HCl(6M) NaHCO3(1M) CuSO4(1M)
材料:玻璃棒 玻璃管 橡皮管
实验五 转化法制备KNO3
[实验目的]学习用转化法制备硝酸钾晶体。学习溶解、过滤、间接热溶解和重结 晶操作。
[实验用品]仪器:量筒、烧杯、台秤、石棉网、三角架、铁架台、布氏漏斗、吸 滤瓶、水流抽气泵、瓷坩埚、坩埚钳、温度计(200℃)、比色管(25ml)。
固体药品:硝酸钠(工业级)、氯化钾(工业级)。
液体药品:AgNO3(0.1M)、硝酸(5M)、氯化钠标准溶液。
材料:滤纸
实验六 Te3+,Al3+ 离子的分离
[实验目的]学习萃取分离法的基本原理,初步了解铁、铝离子不同的萃取行为。 学习萃取和蒸馏分离两种基本操作
[实验用品]仪器:园底烧瓶、直管冷凝器、尾接管、抽滤瓶、烧瓶、梨形分液漏 斗、
量筒、铁架台、铁环。
液体药品:TeCl3(5%)、AlCl3、浓盐酸、乙醚、K4F(CN)6(5%)、冰、 NaOH(2M、6M)、茜素S酒精溶液、热水。
材料:乳酸管、橡皮管、玻璃弯管、滤纸、PH试纸。
实验七 HAc电镀和电力常数的测定
[实验目的]测定醋酸的电离度和电离常数,进一步掌握滴定原理,滴定操作及 正确判断滴定终点,学会使用PH计。
[实验用品]仪器:碱式滴定管、吸量管、移液管、锥形瓶、烧杯、Ph计。
液体药品:Hac(0.20M、0.2M)、NaOH标准溶液、酚酞指示剂。
实验八 I3-□I-+I2常数的测定
[实验目的]测定I3-□I-+I2的平衡常数,加强对化学平衡、平衡常数的理解并了
解平衡移动的原理,练习滴定操作。
[实验用品]仪器:量筒、吸量管、移液管、碱式滴定管、碘量瓶、锥形瓶、吸耳
球。
固体药品:碘
液体药品:KI(0.0100M,0.0200M)、Na2S2O3标准溶液(0.0050M)、淀粉溶液(0.2%)。
实验九 化学反应速率与活化能
[实验目的]了解浓度、温度和催化剂对反应速率的影响。测定过二硫酸铵与碘化 钾反应的反应速率,并计算反应级数,反应速率常数和反应的活化能。
[实验用品]仪器:烧杯、量筒、秒表、温度计。
液体药品:(NH4)2S2O8(0.2M)、KI(0.2M)、Na2S2O3(0.01M)、KNO3(0.2M)、 (NH4)2SO4(0.2M)、Cu(NO3)2(0.02M)、淀粉溶液0.2% 。 材料:冰。
实验十 氧化还原反应和氧化还原平衡
[实验目的]学会装配原电池。掌握电极的本性、电对的氧化性或还原性物质的 浓度、介质的酸性等因素对电极电势、氧化还原反应的方向、产物、速率的影响。 通过实验了解化学电池电动势。
[实验用品]仪器:试管(离心)、烧杯、伏特计、表面皿、U形管。
固体药品:琼脂、氟化铵
液体药品:HCl(浓)、HNO3(2M、浓)、HAc(6M)、H2SO4(1M)、NaOH(6M、40%)、
NH3·H2O (浓)、ZnSO4(1M)、CuSO4(0.01M、1M)、KI(0.1M)、KBr(0.1M)、 FeCl3(0.1M)、Fe2(SO4)3(0.1m)、FeSO4(1M)、H2O2(3%)、KIO3(0.1M)、溴水、碘 水(0.1M)、氯水(饱和)、KCl(饱和)、CCl4、酚酞指示剂、淀粉溶液(40%)。 材料:电极(锌片、铜片)、回形针、红色石蕊试纸、导线、砂纸、滤纸。 [建议]购买一些伏特计(电压表)、电流计或检测电压、电流的一起。
实验十一 由海盐制备试剂级NaCl
[实验目的]学习由海盐制备试剂及氯化钠及其纯度的检验方法。练习溶解、过滤、 蒸发、结晶、气体的发生和净化等基本操作。了解用目视比色和比浊进行限量分 析的原理和方法。
[实验用品]仪器:烧杯、量筒、布氏漏斗、三角架、石棉网、台秤、分析天平、 表面皿、蒸发皿、水泵、滴液漏斗、蒸馏烧瓶、广口瓶、比色管架、比色管、 离心试管。 固体药品:粗食盐、氯化钠(c,p).
液体药品: H2SO4(浓)、NaCO3(1M)、BaCl2(1M)、HCl(2M、6M)、NaOH(2M、40%)、 KSCN (25%)、C2H5OH(95%)、(NH4)Fe(SO4)2、标准溶液(含Fe3+0.01g/l)、
NaSO4标准溶液(含SO42-0.01g/l)。
材料:滤纸、PH试纸。
实验内容及方法:利用倾析法及化学法提纯粗盐,产品纯度检验
实验十二 CuSO4·5H2O的制备 和结晶水含量的测定
【目的要求】
1. 利用废铜粉焙烧氧化的方法制备硫酸铜。
2. 掌握无机制备中加热、倾析法、过滤、重结晶等基本操作。
3. 学习间接碘量法测定铜含量。
【实验原理】
1. 制备及提纯
CuSO4 ·5H2O俗名胆矾,它易溶于水,而难溶于乙醇,在干燥空气中可缓慢 风化,将其加热至230℃,可失去全部结晶水而成为白色的无水CuSO4。 CuSO4 ·5H2O用途广泛,是制取其他铜盐的主要原料,常用作印染工业的媒 染剂、农业的杀虫剂、水的杀菌剂、木材防腐剂,也是电镀铜的主要原料。 CuSO4 ·5H2O的制备方法有许多种,如:利用废铜粉焙烧氧化的方法制备硫酸
铜,可先将铜粉在空气中灼烧氧化成氧化铜,然后将其溶于硫酸而制得硫酸铜。
也可采用浓硝酸作氧化剂,用废铜与硫酸、浓硝酸反应来制备硫酸铜。反应式:
Cu + 2HNO3 +H2SO4 = CuSO4 +2NO2↑+ 2H2O
溶液中除生成硫酸铜外,还含有一定量的硝酸铜和其它一些可溶性或不溶性
杂质,不溶性杂质可经过滤除去。可溶性杂质Fe2+ 和 Fe3+,一般是先将Fe2+
用氧化剂(如H2O2溶液)氧化为Fe3+,然后调节溶液pH 至3,并加热煮沸,
以Fe(OH)3形式沉淀除去。
2 Fe2+ +2 H+ +H2O2 = 2 Fe3+ +2 H2O
Fe3+ +3 H2O = Fe(OH)3↓+3 H+
CuSO4 ·5H2O在水中的溶解度,随温度变化较大,因此可采用蒸发浓缩,冷 却结晶过滤的方法,将CuSO4的杂质除去,得到蓝色水合硫酸铜晶体。
2. 组成分析
(1)结晶水数目的确定
通过对产品进行热重分析,可测定其所含结晶水的数目,并可得知其受热失 水情况,。
(2)铜含量的测定
可用间接碘量法测定样品中铜离子的浓度,计算得出产品中CuSO4 ·5H2O的 含量。其原理为:将含铜物质中的铜转化成Cu2+,在弱酸性介质中,Cu2+与过 量的KI作用,生成CuI沉淀,同时析出I2。析出的I2以淀粉为指示剂,用 Na2S2O3标准溶液滴定。反应如下:
2Cu2+ + 4I- = 2CuI ↓ + I2
或 2Cu2+ + 5I- = 2CuI ↓ + I3-
I2 + 2S2O32- = 2I- + S4O62-
不仅是还原剂,而且也是Cu(I)的沉淀剂和I2的配合剂。加入适当过量的KI, 可使Cu2+的还原趋于完全。上述反应须在弱酸性或中性介质中进行,通常用
NH4HF2控制溶液的pH为3.5~4.0(或加入磷酸和氟化钠)。这种介质对测定
铜矿和铜合金特别有利,因铜矿中含有的Fe、As、Sb及铜合金中的Fe对铜
的测定有干扰,而 F-可以掩蔽Fe3+,pH >3.5时,五价的As、Sb其氧化性
也
可降低至不能氧化I-。CuI的沉淀表面易吸附I2,使终点变色不够敏锐且产生
误差。通常在接近终点
时加入KSCN (或NH4SCN),将CuI转化成溶解度更小的CuSCN沉淀,CuSCN 更容易吸附SCN -从而释放出被吸附的I2,使滴定趋于完全,反应如下: CuI + SCN - = CuSCN↓ + I-
【仪器试剂】
微型滴定管(10 cm3),吸滤装置,电炉(或煤气灯),水浴锅,研钵,蒸发皿,
烧杯,容量瓶(50 cm3、10cm3),吸量管(5 cm3),热天平,分光光度计;废
铜粉或铜屑),H2O2溶液(3% ),H2SO4(3mol·dm-3),H3PO4(浓),HNO3(浓),
KI(1mol·dm-3),淀粉溶液(0.2%),KSCN溶液(10%),NaF(0.5mol·dm-3), HCl (1:1); 氨水(1:1);HAc(1:1)。Na2S2O3标准溶液(0.1mol·dm-3)。
【实验内容】
1. CuSO4 ·5H2O的制备与提纯
(1) 称取3g铜屑,放入蒸发皿中,灼烧至表面呈黑色,自然冷却(目的在
于
(2) 除去附着在铜屑上的油污,若铜屑无油污此步可略去)。
3-3(3) 在灼烧过的铜屑中,加入11cm3mol·dmH2SO4,然后缓慢、分批地加
入
(4) 5cm3浓HNO3(在通风橱中进行)。待反应缓和后盖上表面皿,水浴加热。
(5) 在加热过程中需要补加6cm3 3mol·dm-3H2SO4和1cm3浓HNO3(由于反应
(6) 情况不同,补加的酸量根据具体情况而定,在保持反应继续进行的情况
下,
(7) 尽量少加HNO3)。待铜屑近于全部溶解后,趁热用倾析法将溶液转至小
烧
(8) 杯中,然后再将溶液转回洗净的蒸发皿中,水浴加热,浓缩至表面有晶
体
(9) 膜出现。取下蒸发皿,使溶液冷却,析出粗的CuSO4 ·5H2O,抽滤,称
量。
(3) 重结晶。将粗产品以每克需1.2cm3水的比例溶于水中。加热使CuSO4·5H2O
完全溶解,趁热过滤,滤液收集在小烧杯中,让其自然冷却,即有晶体析出(如
无晶体析出,可在水浴上再加热蒸发)。完全冷却后,过滤,抽干,称量。
2. 产品的热重分析
按照使用热天平的操作步骤对产品进行热重分析。操作条件参考如下: 样品质量:10~15mg 、 热重量程: 25mg
升温速率:5℃/min 、 走纸速度:4格/min
设定升温温度:250℃
测定完成后,分析记录仪绘制的曲线,处理数据,得出水合硫酸铜分几步 失水,每步的失水温度,样品总计失水的质量,产品所含结晶水的百分数, 每摩尔水合硫酸铜含多少摩尔结晶水(计算结果四舍五入取整数),确定出 水合硫酸铜的化学式。再计算出每步失掉几个结晶水,最后查阅CuSO4 ·5H2O 的结构,结合热重分析结果,说明水合硫酸铜五个结晶水热稳定性不同的原因。
3. 产品百分含量的测定(微型碘量法)
(1) 配制CuSO4 ·5H2O样品的待测溶液
称取样品约1.2g(精确至0.0001g),用1cm32mol·dm-3 H2SO4溶解后,加入 少量水,定量转移至50 cm3容量瓶中定容,摇匀。
(2) 测定待测溶液中Cu2+的浓度
用吸量管移取5.00 cm3待测液,于150 cm3碘量瓶中,振荡后,加入2cm3 1mol·dm-3 KI,振荡,塞好瓶塞,置暗处10min后,加水10cm3摇匀,以 1mol·dm-3的Na2S2O3标准溶液滴定至溶液呈黄色,然后加入1cm3 0.2%
0. 的淀粉溶液,再加入2cm3 10% KSCN溶液,继续滴定至蓝色恰好消失为 终点。平行测定三次。
(3) 计算试样中Cu2+浓度和产品中CuSO4 ·5H2O的百分含量。
【扩展内容】
硫酸四氨合铜的制备
称2.5g自制的CuSO4·5H2O溶于3.5cm3水中,加入5cm3浓氨水,溶解后过 滤。将滤液转入烧杯中,沿烧杯壁慢慢滴加8.5cm3 95%乙醇,盖上表面皿 静置。晶体析出后过滤,晶体用乙醇与浓氨水的混合液洗涤,再用乙醇 与乙醚的混合液淋洗,室温干燥,称量。观察晶体的颜色、形状。
【附注】
1. Na2S2O3溶液(0.1mol·dm-3)的配制与标定参见定量分析部分实验 十七
2. (四)1. 。
3. 指示剂淀粉不能加入太早,因滴定反应中产生大量CuI沉淀,淀粉与I2过
4. 早形成蓝色配合物,大量I3-被吸附,终点颜色呈较深的灰色,不好观察。
5. 加入KSCN(或NH4SCN)不能太早,而且加入后要剧烈摇动,有利于沉
6. 淀的转化和释放出吸附的I3-。
实验十三 KMnO4 的制备
实验目的:学习碱熔法由二氧化锰制备高锰酸钾的基本原理和操作方法。 熟悉熔融、浸取。巩固过滤、结晶和重结晶等基本操作。
实验学时:4学时
基本操作:1. 固体的溶解、过滤、蒸发、结晶;
2. 启普发生器的安装和调试。
实验仪器设备:铁坩埚、启普发生器、坩埚钳、泥三角、布氏漏斗、烘箱、 蒸发皿
实验内容及方法:原理:3MnO2+KClO3+6KOH ═ 3K2MnO4+KCl+3H2O
3K2MnO4+2CO2 → 2KMnO4+MnO2↓+2K2CO3 内容:1. 二氧化锰的熔化氧化; 2. 浸取; 3. 锰酸钾的歧化;
4. 滤液的蒸发结晶; 5. 高锰酸钾晶体的干燥
实验十四 碱式碳酸铜的制备
实验目的:通过碱式碳酸铜制备条件的探求和生成物颜色、状态的分析, 研究反应物的合理配料比并确定反应合适的温度条件,以培养独立设计实验的 能力。
实验学时:4学时
基本操作:水浴加热
实验仪器设备:试管、烧杯、恒温水浴、布氏漏斗、吸滤瓶、台秤(所需仪 器、药品、材料由学生自行列出清单,经老师同意即可进行实验)
实验内容及方法: 原理:2CuSO4+2Na2CO3+H2O ═ Cu2(OH)2CO3↓+ 2Na2SO4+CO2
内容:1. 配制反应物溶液
2. 制备反应条件的探求(反应物配比及反应温度)
3. 碱式碳酸铜的制备
实验十五 P区非金属元素(一)(卤素、氧、硫)
实验目的:学习氯气、次氯酸盐、氯酸盐的制备方法,以及次氯酸盐、氯酸盐 强氧化性区别。掌握H2O2的某些重要性质。掌握不同氧化态硫的化合物的重要 性质。掌握气体发生的方法和仪器的安装。了解氯、溴、氯酸钾的安全操作。 基本操作:1. 气体的发生和收集;
2. 离心分离。
实验仪器设备:
制备氯气装置:
实验内容及方法: 制备氯气、氯酸钾、次氯酸钠
MnO2+4HCl(浓)=MnCl2+2H2O+Cl2↑
3Cl2+6KOH=KCl+KClO3+3H2O
Cl2+NaOH=NaCl+NaClO+H2O
设计实验验证Cl2、Br2、I2的氧化性及Cl-、Br-、I-的还原性,
验证氯酸钾、次氯酸钠的氧化性, 设计实验验证H2O2的性质
硫化合物的性质实验(金属硫化物的溶解性、亚硫酸盐的性质、硫代硫酸盐的 性质、过二硫酸盐的氧化性)
实验十六 P区非金属元素(二)(氮族、硅、硼)
实验目的:实验并掌握不同氧化态氮的化合物的主要性质;实验磷酸盐的酸碱性
合
溶解性以及焦磷酸盐的配位性;观察硅酸合硅酸盐的性质;掌握硼酸及硼酸的焰色
反
应以及硼砂珠反应
实验学时:3学时
基本操作:1. 试管操作;
2. 硼砂珠试验。
实验仪器设备:试管、烧杯、表面皿、酒精灯、蒸发皿
实验内容及方法:铵盐的热分解;亚硝酸和亚硝酸盐;硝酸和硝酸盐;磷酸盐的 性质;硅酸水凝胶的生成;硼酸及硼酸的焰色鉴定反应
实验十七 常见非金属阴离子的分离与鉴定
实验名称:常见非金属阴离子的分离鉴定
实验目的:学习和掌握常见阴离子的分离和鉴定方法,以及离子检出上午基本操作
实验学时:3学时
基本操作:离心分离操作。
主要实验仪器设备:
点滴板 ,离心机。
实验内容及方法: 常见11种非金属阴离子的鉴定反应;Cl-、Br-、I-混合物的分
离
和鉴定;S2-、SO32-、S2O32-混合物的分离和鉴定
实验十八 土族金属(碱金属、碱土金属、铝、锡、铅、锑、铋) 实验目的:比较碱金属碱土金属的活泼性和焰色反应;掌握镁、钙、钡、锡、铅、 锑、铋的氢氧化物的溶解性;锡、铅、锑、铋的难溶物及其转化
实验学时:6学时
基本操作:焰色反应
实验仪器设备: 试管、离心试管
实验内容及方法: 钠、钾、镁、铝的性质(钠与空气中氧气的作用、钠、钾、
镁、
铝与水的作用);镁、钙、钡、锡、铅、锑、铋的氢氧化物的溶解性;IA、IIA
元素
的焰色反应;锡、铅、锑、铋的难溶盐
附:IA、IIA元素的焰色反应:
实验十九 ds区金属(铜、银、锌、镉、汞)
实验目的:了解铜、银、锌、镉、汞氧化物或氢氧化物的生成和性质;了解锌、 镉、汞硫化物的生成和性质;掌握铜、银、锌、镉、汞重要配合物的性质;握 铜、银、汞重要的氧化还原性。
实验学时:3学时
基本操作:试管操作
实验内容及方法:铜、银、锌、镉、汞氧化物或氢氧化物的生成和性质;锌、镉、 汞硫化物的生成和性质;铜、银、锌、镉、汞重要配合物的性质
实验仪器设备:试管
实验二十 常见阳离子的分离与鉴定(一)
实验目的:巩固和进一步掌握一些金属元素及其化合物的性质。了解常见阳离子 混合液的分离和检出的方法以及巩固检出离子的操作。
实验学时:4学时
基本操作:试管操作和离心管的使用
实验仪器设备:试管、烧杯、离心机、离心管
实验内容及方法: 1. 5种碱金属、碱土金属离子的鉴定;2. 10种p区和ds区 金属离子的鉴定;3. Ag+、Cd2+、Al3+、Ba2+、Na+混合离子的分离和鉴定
实验二十一 第一过度系元素(一)(钛、钒、铬、锰)
实验目的:掌握钛、钒、铬、锰重要化合物的性质及各氧化态之间相互转化的条件
实验学时:6学时
基本操作:沙浴加热
实验仪器设备:试管、烧杯、离心机、离心管
实验内容及方法: 钛化合物的重要性质;钒化合物的重要性质;铬化合物的重
要
性质;锰化合物的重要性质。
实验二十二 第一过度系元素(二)(铁、钴、镍)
实验目的:掌握铁、钴、镍低价态的还原性高价态的氧化性;掌握铁、钴、镍 重要配合物的生成及 性质
实验学时:3学时
基本操作:试管操作和离心管的使用
实验仪器设备:试管、离心试管
实验内容及 实验方法: 铁(II)、钴(II)、镍(II)化合物的还原性;铁(III)、 钴(III)、镍(III)化合物的氧化性;铁、钴、镍配合物的生成
实验二十三 常见阳离子的分离与鉴定(二)
实验目的:学习混合离子分离的方法,进一步巩固离子鉴定的条件和方法。熟 练运用常见元素(Ag、Hg、Pb、Cu、Fe)的化学性质。
实验学时:4学时
基本操作:试管操作和离心管的使用
实验仪器设备:离心机、离心试管、烧杯、点滴板
实验内容及方法:NO3-、Fe3+的鉴定;Ag+、Pb2+和Cu2+、Hg2+、Fe3+的分离及 Ag+、Pb2+的分离和鉴定。
实验二十四 一种钴(Ⅲ)配合物的制备
实验目的:掌握制备金属配合物常用的方法——水溶液中的取代反应和氧化还原 反应; 掌握电导仪的使用以及通过电导仪测电导率确定化学式所含离子数的方法
实验学时:4学时
基本操作:1. 试剂的取用;
2. 水浴加热;
3. 试样的过滤、洗涤、干燥;
4. 电导率仪的使用。
主要实验仪器设备:电导率仪,参见实验10
实验内容及方法:1 制备钴(III)配合物(利用水溶液中的取代反应和氧化 还原反应)
2 组成的初步推断
实验二十五 硫酸亚铁铵的制备
实验目的
1. 学习复盐的制备及性质
2. 巩固无机制备基本操作,了解微型实验方法与操作
实验原理
硫酸亚铁铵(NH4)2Fe(SO4)2·6H2O, 俗称莫尔盐,为浅蓝绿色单斜晶体,易 溶于水,难溶于酒精。在空气中比亚铁盐稳定,不易被氧化,可做氧化还原滴 定法中的基准物。常用的制备方法是用铁与稀硫酸作用制得硫酸亚铁,再用 FeSO4与(NH4)2SO4水溶液中等物质的量相互作用,由于复盐的溶解度比单盐 要小,因此经冷却后复盐在水溶液中首先结晶,形成(NH4)2FeSO4·6H2O复盐。 试剂与器材
试剂 铁屑,10%Na2CO3, 3mol·L-1H2SO4,(NH4)2SO4(s)。
器材 微型锥形瓶(15mL),烧杯(15mL),抽滤瓶(口径19mm,容积 20mL),布氏漏斗(20mm,19mm),吸球,蒸发皿(10mL),锥形瓶,烧杯
,抽滤瓶,布氏漏斗,蒸发皿等。
实验方法
(1)碎铁片的准备 用台秤称取4.0g铁屑,放入150mL锥形瓶中,加入 20mL10%Na2CO3 , 加热煮沸除去油污。倾去碱液,用水洗至铁屑为中性。
(2)FeSO4溶液的制备 在上述锥形瓶内,加入20mL 3mol·L-1H2SO4,在
水浴中加热约30min,加热过程中可补充水分,防止结晶析出,然后趁热过滤,
分别用2mL 3mol·L-1H2SO4和少量蒸馏水洗涤。
滤液转移至蒸发皿中。
(3)硫酸亚铁铵的制备 在上述FeSO4溶液中加入9.5g化学纯硫酸铵,用
小火加热至溶解,继续加热蒸发浓缩至表面出现晶膜为止,冷却,结晶, 抽滤,
称量计算产率。
(4)微型实验 称取铁屑0.5g于15mL微型锥形瓶中;加入3mL10% Na2CO3,加热去油,然后用蒸馏水洗净,加入2.5mL 3mol·L-1H2SO4,在水浴中
加热5min,使反应完全,用微型布氏漏斗,吸球抽滤,依次用0.3mL 3mo·L-1 H2SO4,几滴蒸馏水洗涤,滤液转移至微型蒸发皿中,加入1.2g化学纯硫酸铵,
加热溶解并蒸发出现晶膜、冷却结晶、抽滤称量、计算产率。
思考题
1. 在制备FeSO4时,为什么开始时Fe过量,并用水浴加热?后又需
将溶
2. 液调节至强酸性?
2. 试比较微型实验与常规实验的利弊?
实验二十六 三草酸和铁(Ⅲ)酸钾的制备和性质
一、实验目的:
1、了解三草酸合铁(III)酸钾的制备方法及实验原理
2、掌握三草酸合铁(III)酸钾的性质
3、巩固冷却、结晶、重结晶、洗涤、干燥等基本操作
4、了解感光液、感光纸的简单制备
二、实验原理:
首先由硫酸亚铁铵与草酸反应制备草酸亚铁:
(NH4)2Fe(SO4)2·6H2O+H2C2O4 →FeC2O4·2H2O↓ +(NH4)2SO4+H2SO4 +4H2O 然后在过量草酸根存在下,用过氧化氢氧化草酸亚铁可得到三草酸 合铁(III)酸钾,同时有氢氧化铁生成:
6FeC2O4·2H2O+3H2O2+6 K2C2O4→K3[Fe(C2O4)3]+2 Fe(OH)3↓+12H2O
加入过量草酸可使氢氧化铁转化为三草酸合铁(III)酸钾配合物: 2Fe(OH)3+3 H2C2O4+3K2C2O4→2K3[Fe(C2O4)3] ·3H2O 再加入乙醇,放置即可析出产物的结晶。总反应式:
2FeC2O4·2H2O +H2O2+H2C2O4+3K2C2O4→2K3[Fe(C2O4)3] ·3H2O
三、基本操作:
冷却、结晶、重结晶、洗涤、干燥
四、实验内容:
(一)三草酸合铁(III)酸钾的制备
(二)性质实验
五、教学提示:
本实验的重点:了解三草酸合铁(III)酸钾的制备方法和性质;理解制备过程 中化学平衡原理的应用。
本实验的难点:掌握水溶液制备无机物的一般方法;练习溶解、沉淀、沉淀洗涤、 离心分离、过滤、浓缩等基本操作。
实验二十七 硫代硫酸钠的制备
实验目的:掌握用亚硫酸钠制备硫代硫酸钠的方法,进一步熟悉布氏漏斗抽滤的操作
实验学时:4学时
基本操作:1. 气体的发生、收集和净化;
2. 回流操作。
实验仪器设备:烧杯、表面皿、布氏漏斗、烘箱
实验内容及方法:原理:Na2SO3+S ═ Na2S2O3
内容:1. 硫代硫酸钠的制备; 2. 产品的鉴定
实验二十八 硫酸四氨合铜(Ⅱ)的制备
[试验步骤] 称2.5g自制的CuSO4·5H2O溶于3.5cm3水中,加入5cm3浓氨水,
溶解后过滤.将滤液转入烧杯中,沿烧杯壁 慢慢滴加8.5cm3 95%乙醇,盖上表面皿,
静置.晶体析出后过滤,晶体用乙醇与浓氨水的混合液洗涤,再用 乙醇与乙醚的混
合液淋洗,室温干燥,称量.观察晶体的颜色,形状.
【附注】
1. Na2S2O3溶液(0.1mol·dm-3)的配制与标定参见定量分析部分实验 十七(四)1. .
2. 指示剂淀粉不能加入太早,因滴定反应中产生大量CuI沉淀,淀粉与I2过早形成
蓝色配合物,大量I3-被吸附,终点颜色呈较深的灰色,不好观察.加入KSCN(或
NH4SCN)
不能太早,而且加入后要剧烈摇动,有利于沉淀的转化和释放出吸附的I3-.
