一、 选择题:(30%,每小题2分)
1. 下列各组分子中,中心原子轨道均发生sp3杂化(等性或不等性),而分子的空间构型各不相同的是( )
A、H2S、H2O、BeCl2 B、H2O、NH3、CH4
C、CO2、CH4、BF3 D、NH3、CH4 、SiCl4
2. 若设反应2 C6H6 (l) + 15O2 (g) = 12 CO2 (g) + 6 H2O (l) 的定容热效应为Qv,定压热效应为Qp, 则Qv与Qp两者数值间的关系为( )
A. Qv > Qp B. Qv < Qp C. Qv = Qp D. 无法确定
3. 在某温度下,反应C (s) + H2O (g) =CO (g) + H2 (g) 的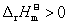 , 达平衡时,可使H2的量增加的操作是( )
, 达平衡时,可使H2的量增加的操作是( )
A. 加入催化剂 B. 减小H2O (g) 的压力
C. 增大系统压力 D. 提高体系温度
4. 若反应A + B =C + D 的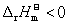 ,当反应体系的T增加时,将会有( )
,当反应体系的T增加时,将会有( )
A. k正 和k逆 都减少, 同时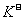 增大 B. k正 和k逆 都增大, 同时
增大 B. k正 和k逆 都增大, 同时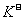 减小
减小
C. k正 增大和k逆 减少,同时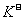 增大 D. k正 减小和k逆 增大,同时
增大 D. k正 减小和k逆 增大,同时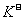 减小
减小
5. 下列哪种分子偶极距不等于零( )
A、CCl4 B、PCl5 C、PCl3 D、SF6
6. 具有下列电子排布式的原子中,何者处于激发态?( )
A. 1s22s22p2 B. 1s22s22p3 C. 1s22s12p2 D. 1s22s22p63s23p63d54s1
7. 已知H3PO4的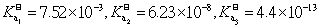 。欲配制pH = 7.00 的缓冲溶液,选择的缓冲对应是( )
。欲配制pH = 7.00 的缓冲溶液,选择的缓冲对应是( )
A. H3PO4-NaH2PO4 B. NaH2PO4-Na2HPO4
C. Na2HPO4-Na3PO4 D. NaH2PO4-Na3PO4
8. 已知平衡体系A2B3 (s)=2A3+ + 3B2-中有x mol L-1的A2B3溶解,则
L-1的A2B3溶解,则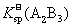 与x的关系可表示为 ( )
与x的关系可表示为 ( )
A. 27x3 B. 108x3 C. 27x5 D. 108x5
9. 下列配合离子能在强酸介质中稳定存在的是( )
A. FeF63- B. FeCl4- C. Fe(C2O4)33- D. Ag(NH3)2+
10. 下列电对中,其E(电极电势)不受溶液酸度变化而变化的是( )
A. Cr2O72-/Cr3+ B. MnO2/Mn2+
C. MnO4-/Mn2+ D. MnO4-/MnO42-
11. 已知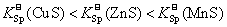 ,则有( )
,则有( )
A. 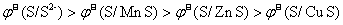
B. 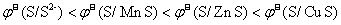
C. 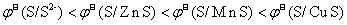
D. 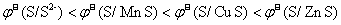
12. AgF易溶于水,AgBr难溶于水,主要是因为F-与Br-相比,F-的( )
A、变形性小 B、极化力强
C、变形性大 D、极化力弱
13. 从物质结构判断卤化氢(HF, HCl, HBr和HI),其酸的强度由低度到高的顺序为( )
A.HF>HCl>HBr>HI B. HCl>HF>HBr>HI
C.HI>HBr>HCl>HF D. HF>HCl>HI>HBr
14. 下列分子中中心原子未采用sp杂化轨道类型的是( )
A.BeCl2 B. CHCH C. H2O D. HgCl2
15. 下列化合物熔点由高到低的顺序为( )
A. SiCl4>KCl>SiBr4>KBr B. KCl>KBr>SiBr4>SiCl4
C. SiBr4>SiCl4>KBr>KCl D. KCl>KBr>SiCl4>SiBr4
二、填空题(30%,每小题2分)
1、K3[FeCl(NO2)(C2O4)2]配位化合物的命名为 。
2. 标态卤素单质氧化性顺序为: ,标态卤离子还原性顺序为: 。
3. 同浓度卤化氢水溶液酸性顺序为: 。
4. H2的标准摩尔燃烧焓(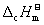 )与H2O(l)的标准摩尔生成焓(
)与H2O(l)的标准摩尔生成焓(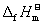 )的数值关系是 。
)的数值关系是 。
5. 0.10 moL L-1 NaAc水溶液的pH= (已知
L-1 NaAc水溶液的pH= (已知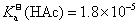 )。
)。
6. H3PO2(次磷酸)是 元质子酸,它与AgNO3水溶液的反应方程式为: 。
7. 根据分子轨道法,分子或离子C2(g) 、N2(g) 和O2+(g)的键级顺序是: 。
8. 配离子[Fe(CN)6]4-的中心原子采用的杂化轨道类型为 ,磁矩为 。
9. 分子的极性常用偶极矩(μ= q×d)来衡量。HI分子与HCl分子中偶极矩较大的分子是 。
10. 在2000 oC时,反应N2(g)+O2(g) 2NO(g)的
2NO(g)的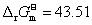 kJ·mol-1。当p(N2) = 2.0 kPa, p(O2) = 5.1 kPa, p(NO) = 4.1 kPa条件下反应的
kJ·mol-1。当p(N2) = 2.0 kPa, p(O2) = 5.1 kPa, p(NO) = 4.1 kPa条件下反应的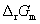 ,此时反应进行的方向是 。
,此时反应进行的方向是 。
11.CO中两元素电负性差很大,但其分子电偶极矩很小,原因是 。
三、 简答题:(10%,每小题5分)
1、Ag不能置换1 .0 moL L-1HCl中的氢,但是Ag却能置换1.0 moL
L-1HCl中的氢,但是Ag却能置换1.0 moL L-1HI溶液中的氢。为什么?请解释原因(不必计算)。
L-1HI溶液中的氢。为什么?请解释原因(不必计算)。
2、什么叫“镧系收缩”,它对第六周期中镧系后各元素的性质影响如何?
四、计算题(30%,1题5分,2题15分,4题10分)
1、计算pH=10.00时Mg(OH)2的溶解度。已知Mg(OH)2的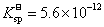 。
。
2、有一原电池,其电池符号为
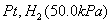
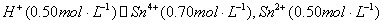
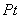
(1)写出半电池反应;
(2)写出电池反应;
(3)计算原电池的电动势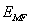 ;
;
(4)当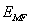 =0时,在保持
=0时,在保持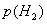 和
和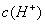 不变的情况下,
不变的情况下,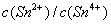 等于多少?
等于多少?
已知: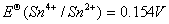
3、将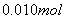 的
的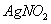 晶体溶解在
晶体溶解在 盐酸溶液中,最后溶液中
盐酸溶液中,最后溶液中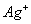 和
和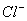 浓度各是多少?此时溶液中是否存在
浓度各是多少?此时溶液中是否存在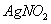 沉淀?已知:
沉淀?已知: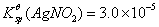 ,
,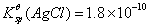 ,
,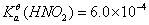 。
。
