20##无机化学

考试科目:无机化学 共4页,第1页

考试科目:无机化学 共4页,第2页

考试科目:无机化学 共4页,第3页

考试科目:无机化学 共4页,第4页
第二篇:暨南大学无机化学20xx
20##暨南大学无机






(二)
选择题 (选择一个正确答案,每小题2分, 25题共 50分 )
1. CO2晶体升华时,需要克服的作用力主要是……………………………( )
(A)离子键 (B)氢键 (C)共价键 (D)范德华力
2. Fe(CO)5的中心离子采用dsp3杂化, 试问其的空间构型 ………………( )
(A) 正四体形 (B)三角双锥形 (C) 平面四边形 (D) V形
3.N2分子中存在的共价键为…………………………………………………( )
A. 只有s键 B. 只有p键
C. 一个s键和二个p键 D. 二个s键和一个p键
4.在[Co(en)(NH3)4]3+ 配离子中,中心离子的配位数为……………………( )
A. 3 B. 4 C. 5 D. 6
5.下列反应的平衡常数可以用Kp = 1/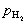 表示的 …………………………( )
表示的 …………………………( )
(A) H2(g) + S(g) H2S(g) (B) H2(g) + S(s)
H2S(g) (B) H2(g) + S(s) H2S(g)
H2S(g)
(C) H2(g) + S(s) H2S(l) (D) H2(l) + S(s)
H2S(l) (D) H2(l) + S(s) H2S(s)
H2S(s)
6.下列元素属于ds区元素的是………………………………………………( )
A. 4d105s1 B. 4s24p6 C. 4s2 D. 3d14s2
7.过量AgCl溶解在下列各物质中,问哪种溶液中Ag+浓度最小…………( )
(A) 100 cm3水 (B) 1000 cm3水
(C) 100cm3 0.2mol·dm-3 KCl溶液 (D) 1000 cm3 0.5mol·dm-3 KNO3溶液
8.在工业上欲除去ZnSO4溶液中的Fe3+ 杂质,需加入最合适的试剂是……( )
(A) NaOH (B) Na2CO3
(C) ZnCO3 (D) Zn
9.H2O(l, 100℃, 101.3 kPa) H2O(g, 100℃, 101.3 kPa),设H2O(g)为理想气体,则由始态到终态体系所吸收的热量Q为……………………………………( )
H2O(g, 100℃, 101.3 kPa),设H2O(g)为理想气体,则由始态到终态体系所吸收的热量Q为……………………………………( )
(A) >ΔH (B) <ΔH (C) =ΔH (D) =ΔU
10.Li、Be、B原子失去一个电子,所需要的能量相差不是很大, 但最难失去第二个电子的原子估计是……………………………………………………… ( )
(A) Li (B) Be (C) B (D) 都相同
11.性质最相似的两种元素是…………………………………………………( )
(A) Zr和Hf (B) Ru和Rh (C) Mn和Mg (D) Cu和Cr
12.pH 计上所用的指示电极是………………………………………………( )
(A) 饱和甘汞电极 (B) 铂电极
(C) 氯化银电极 (D) 玻璃电极
13.下列分子和离子中,中心原子的价层电子对几何构型为四面体,且分子(离子)空间构型为角形(V形)的是……………………………………………………( )
(A) (B) SO2 (C) H3O+ (D) OF2
(B) SO2 (C) H3O+ (D) OF2
14.CrO5中Cr的氧化数为 ………………………………………………… ( )
(A) 4 (B) 6 (C) 8 (D) 10
15.由下列反应设计的电池不需要惰性电极的是……………………………( )
(A) H2(g) + Cl2(g) = 2HCl(aq) (B) Ce4+ + Fe2+ = Ce3+ + Fe3+
(C) Zn + Ni2+ = Zn2+ + Ni (D) Cu + Br2 = Cu2+ + 2Br-
16.在FeCl3与KSCN的混合液中加入过量NaF,其现象是…………………( )
(A) 产生沉淀 (B) 变为无色 (C) 颜色加深 (D) 无变化
17.含有下列离子的溶液,与Na2S溶液反应不生成黑色沉淀的一组是……( )
(A) Fe2+,Bi3+ (B) Cd2+,Zn2+ (C) Fe3+,Cu2 (D) Mn2+,Pb2+
18.0.50 mol·dm-3 HAc的电离度是(Ka = 1.8 ´ 10-5)……………………………( )
(A) 0.60 % (B) 0.90 % (C) 0.030 % (D) 1.3 %
19.已知,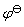 (Sn4+ / Sn2+) = 0.14 V,
(Sn4+ / Sn2+) = 0.14 V,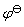 (Fe3+ / Fe2+) = 0.77 V,则不能共存于同一溶液中的一对离子是…………………………………………………………… ( )
(Fe3+ / Fe2+) = 0.77 V,则不能共存于同一溶液中的一对离子是…………………………………………………………… ( )
(A) Sn4+,Fe2+ (B) Fe3+,Sn2+
(C) Fe3+,Fe2+ (D) Sn4+,Sn2+
20.下列物质的酸性强弱顺序正确的是……………………………………… ( )
(A) HF> HI > HCl (B) HF> HCl > HI
(C) HI > HF > HCl (D) HI > HCl >HF
21.273 K 时, 蒸气压最高的物质是……………………………………………( )
(A) 汽油 (B) 甘油 (C) 冰 (D) 食盐
22.下列量子数合理的一组是………………………………………………… ( )
(A) n= 1 l = 0 m= 1 (B) n= 1 l = 1 m= 1
(C) n= 3 l = 2 m= 1 (D) n= 2 l = 1 m= 2
23.某中心离子d5在八面体场中处于高自旋,由公式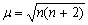 (n为未成对电子数)计算的数据应为………………………………………………………( )
(n为未成对电子数)计算的数据应为………………………………………………………( )
(A) 5.48 (B) 0
(C) 5.92 (D) 不能计算
24.能生成氮气的方法是…………………………………………………… ( )
(A) 将硝酸铵(NH4NO3)加热 (B) 将亚硝酸铵(NH4NO2)加热
(C) 将氯气与氨混合 (D) B和C
25.下列各组混合液中,能作为缓冲溶液的是……………………………( )
(A) 10 cm3 0.2 mol·dm-3 HCl和10 cm3 0.1 mol·dm-3 NaCl
(B) 10 cm3 0.2 mol·dm-3 HAc和10 cm3 0.1 mol·dm-3 NaOH
(C) 10 cm3 0.2 mol·dm-3 HAc和10 cm3 0.3 mol·dm-3 NaOH
(D) 10 cm3 0.2 mol·dm-3 HCl和10 cm3 0.2 mol·dm-3 NaOH
二、填空题(1、5题每空2分,其余每空1分,共 33分)
1. 在Al3+和Cu2+的混合溶液中加入过量的NH3· H2O,生成的沉淀是________。
2.Cr原子(Z=24)基态时电子组态________________________________________,
价层上的电子数为_______________, 属于第_____周期第_____族元素。
3. (1) BBr3熔点-46℃,属________晶体,微粒之间的作用力为_________。
(2) KF熔点880℃,属________晶体,微粒之间的作用力为________。
(3) Si熔点1423℃,属________晶体,微粒之间的作用力为_______。
4.  N2 +
N2 +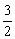 H2
H2 NH3
NH3  = -46 kJ·mol-1
= -46 kJ·mol-1
气体混合物处于平衡时,N2生成NH3的转化率将会发生什么变化?
(1) 压缩混合气体_____________; (2) 升温___________________;(3) 引入H2__________________; (4) 恒压下引入惰性气体_________;
(5) 恒容下引入惰性气体____________________。
6. 配平下列方程式:
(1).( )Cu +( )HNO3 —( )Cu (NO3)2 + ( )NO + ( )H2O
(2).( )P4 +( )HClO3 + ( ) H2O—( )H3PO4+ ( )HCl
7. 下列物质 ,
,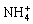 ,Ac-中,属于质子酸的是______________,其共轭碱是________________。属于质子碱的是________________,其共轭酸是_________________。
,Ac-中,属于质子酸的是______________,其共轭碱是________________。属于质子碱的是________________,其共轭酸是_________________。
三、问答题 (共4题,共22分 )
1.5分,试用分子轨道理论写出N2的分子轨道结构式,说明是否具有磁性?并计算键级。
2. 5分,试给下配合物命名或写出化学式:
(1)[Cu(NH3)4]SO4 , (2)[Co(en)3]Cl3,(3)Li[AlH4]
(4)氯化二氯一水三氨合钴(Ⅲ),(5)六氯合铂(Ⅳ)酸钾
3. 6分,将Zn+ Cu2+ = Cu + Zn2+ 氧化还原反应设计为一个原电池。试写出电池的负极和正极发生的半反应以及原电池符号的表达式?已知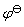 (Zn2+ / Zn) = -0.76 V,
(Zn2+ / Zn) = -0.76 V,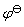 (Cu2+ / Cu) = 0.34 V,则原电池的电动势
(Cu2+ / Cu) = 0.34 V,则原电池的电动势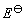 和
和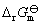 分别是多少?
分别是多少?
4.6分,已知反应FeO(s) + CO(g) Fe(s) + CO2(g)的
Fe(s) + CO2(g)的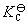 = 0.5 (1273K)。若起始浓度CO=0.05mol·L-1, CO2=0.01mol·L-1,问:(1) 反应物,生成物的平衡浓度各是多少?(2) 增加FeO是否对平衡有影响?(简单说明道理)
= 0.5 (1273K)。若起始浓度CO=0.05mol·L-1, CO2=0.01mol·L-1,问:(1) 反应物,生成物的平衡浓度各是多少?(2) 增加FeO是否对平衡有影响?(简单说明道理)
四、计算题 ( 共3题,每题15分,共45分)
1. 某化工厂生产中需用银作催化剂,它的制法是将浸透AgNO3溶液的浮石在一定温度下焙烧,使发生下列反应:AgNO3(s) Ag(s) + NO2(g) +
Ag(s) + NO2(g) +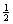 O2(g)
O2(g)
试从理论上估算AgNO3分解成金属银所需的最低温度。已知:
AgNO3(s) 的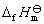 = -123.14 kJ·mol-1,
= -123.14 kJ·mol-1, = 140 J·mol-1·K-1
= 140 J·mol-1·K-1
NO2(g) 的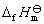 = 35.15 kJ·mol-1,
= 35.15 kJ·mol-1, = 240.6 J·mol-1·K-1
= 240.6 J·mol-1·K-1
Ag(s) 的 = 42.68 J·K-1·mol-1,O2(g) 的
= 42.68 J·K-1·mol-1,O2(g) 的 = 205 J·mol-1·K-1
= 205 J·mol-1·K-1
2. 计算AgCl在6mol·L-1氨水中的溶解度。(已知:K稳[Ag(NH3)2]+=1.6×107,中Ksp,AgCl=1.7×10-10)
3. 3.25g固体KCN溶于水配成500mL水溶液,试计算该溶液的酸度。(已知:HCN的酸度常数为4.93×10-10,KCN的式量为65)
