第一部分 知识要点及解题模型归纳
1.由K层→Q层,电子的能量:低→高,离核的距离:近→远。
2.任一能层的能级总是从s能级开始,而且能级数等于该能层序数:K层(n=1)只有1s一个能级,L层(n=2)有 2s、2p两个能级,M层(n=3)有3s、3p、3d三个能级,N层(n=4)有4s、4p、4d、4f四个能级,…
3.每个能级最多容纳的电子数是能层序数平方的两倍,即2n2(n=1,2,3,4,…,2n2=2,8,18,32,…)
4.当同一能级上的电子排布为全充满(p6、d10、f14)、半充满(p3、d5、f7)和全空状态(p0、d0、f0)时,具有较低的能量和较大的稳定性。这是洪特规则的特例。根据这个规律,铬(24Cr)的外围电子排布是3d54s1(3d、4s能级均为半充满)而不是3d44s2,铜(29Cu)的外围电子排布是3d104s1(3d全充满、4s半充满)而不是3d94s2等等。
5.21—30号元素的价电子排布依次为:3d14s2→3d24s2→3d34s2→3d54s1→3d54s2→3d64s2→3d74s2→3d84s2→3d104s1→3d104s2。
6.ns、np、nd、nf能级分别有1、3、5、7个原子轨道,最多容纳2、6、10、14个电子。所以n能层的能级数为n,原子轨道数为n2,最多容纳的电子数为2n2。
7.非金属元素并不都在p区(H元素在s区);最外层只有1个电子,并不一定在ⅠA族(可能为ⅠA族及Cr、Cu等元素);最外层只有2个电子,并不一定在ⅡA族(可能为ⅡA族、He及Sc、Ti、V等多数过渡元素);最外层有3-7个电子,则一定在ⅢA~ⅦA族。
8.各周期所包含的元素种数为2、8、8、18、18、32、32(现在排了26种,若排满则为32种),即可巧记为1个2、2个8、2个18、2个32(联系2n2)。因此,记住“2-8-8-18-18-32-32”、“1-3-11-19-37-55-87”(ⅠA族)、“2-10-18-36-54-86”(O族)类3组数字中的任意一组及族序数的顺序即可由任意原子序数推知元素的位置。
9.元素周期表中的相等规律:核电荷数=质子数=原子序数;基态原子的电子层数(能层数)=周期序数;基态原子的最外层电子数=主族序数=最高正价=8—|最低负价|(氧、氟例外)。
10.不能由非金属元素单质的熔沸点、与氧气反应的难易、氢化物的沸点或水溶液的酸性、非最高价氧化物对应的水化物的酸性来比较和判断元素的非金属性的强弱。
11.同周期元素,自左到右,原子半径逐渐减小;同主族元素,自上而下,原子半径逐渐增大。如A、B、C、D四种元素在周期表中的位置关系为,则原子半径r(A)>r(B)>r(C)>r(D),即原子半径按 或 方向逐渐减小,如r(K)>r (Mg)>r(S)>r(F);但如果是 或方向,则不能比较其原子半径大小,切不可形成“能层数(电子层)越多,原子半径越大”的误区。
12.同种元素:阳离子半径<原子半径;阴离子半径>原子半径。如 r(H+)<r(H)<r(H-)。
13.同主族元素,从上到下,离子半径逐渐增大。如r(Na+)<r(K+),r(O2-)<r(S2-)。
14.同周期元素,从左至右,阳离子半径逐渐减小,阴离子半径逐渐减小。如r(Na+)>r(Mg2+),r(S2-)>r(Cl-),但阴离子半径大于阳离子半径,如r(S2-)>r(Cl-)>r(Na+)>r(Mg2+)>r(Al3+)。
15.电子层结构相同的离子:“序大径小”。
注意:同周期中,离子半径最小的是最后一种金属的阳离子,如第三周期是Al3+。
16.①同周期,元素的第一电离能呈增大的趋势。碱金属的第一电离能最小,稀有气体的第一电离能最大。②同周期,电离能的增大有一些曲折。一般而言,ⅡA族元素的I1>ⅢA族元素,ⅤA族元素的I1>ⅥA族元素,如I1(Be) >I1(B),I1(N)>I1(O),这是由于ⅡA族元素(如Be、Mg)有着比较稳定的ns2np0(s能级全满,p能级全空)结构,ⅤA族元素(如N、P)有着比较稳定的ns2np3(p能级半充满)结构而使其原子稳定的缘故。③同主族,随着电子层数的增加,元素的第一电离能逐渐减小。
特别提醒:Be与B、N与O、Mg与Al、P与S第一电离能大小的反常现象。
17.用电离能判断原子失去电子的数目和形成阳离子所带的电荷(元素的化合价)。若I2》I1,则电子易形成+1价阳离子而不易形成+2价阳离子;若I3》I2>I1,则主要化合价为+2价。
如果,即电离能在In与In+1之间发生突变,则元素的原子易形成+n价离子面不易形成+(n+1)价离子,对于主族元素而言,最高化合价为+n价(或只有0价、+n价)。
18.同周期元素从左到右,电负性逐渐增大,表明金属性逐渐减弱,非金属性逐渐增强。同主族元素从上到下,电负性逐渐减小,表明元素的金属性逐渐增强,非金属性逐渐减弱。
图形强记:
19.①金属的电负性一般小于1.8,非金属的电负性一般大于1.8,通常电负性越大,非金属性越强;金属性越强,电负性越小。②一般认为:若两种成键元素原子间的电负性差值大于1.7,它们之间通常形成离子键,所形成的化合物是离子化合物;若两种成键元素原子间的电负性差值小于1.7,它们之间通常形成共价键,所形成的化合物是共价化合物(如AlCl3)。③成键原子的电负性之差越大,键的极性越强,如H-F>H-Cl>H-Br>H-I。④两种非金属元素形成的化合物中,通常电负性大的元素显负价,电负性小的显正价,如、 、 。⑤Li与Mg、Be与Al、B与Si等构成对角线的元素性质相似是由于它们的电负性相近的缘故。
特别提醒:不能将电负性1.8作为划分金属与非金属的绝对标准;不能将电负性差值1.7作为判断离子键和共价键的绝对标准。
20.离子键和金属键没有饱和性和方向性。共价键具有饱和性和方向性,但H2分子中的共价键即H—H键(s-s σ键)没有方向性。
21.共价单键是σ键,共价双键一个是σ键,一个是π键;共价叁键中一个是σ键,两个是π键(常见的双键有C=C、C=O,常见的叁键有C C、C N、N N等)。
22.共价分子中可能只有σ键而无π键,不可能只有π键而无σ键。
23.正四面体分子中的键角不一定是109°28/,如白磷P4分子中的键角为60°。
24.键参数:键能越大,共价键越稳定;键长越短,共价键越稳定;键能和键长用于衡量共价键的稳定性和原子晶体的熔沸点、硬度,键长和键角决定分子的立体构型和分子的极性。
键参数是描述物质结构的重要因素,影响物质的物理性质和化学性质。
特别提醒:由共价分子形成的物质的熔沸点高低不是由共价键键能大小决定的。如HF很稳定是由于H-F键键能大,而HF的沸点高与键能无关(是由于分子间形成氢键,分子间作用力强)
25.等电子体具有相似的化学键特征。它们的结构相似,许多性质相似。(类推的重要依据)
26.①常见的直线形分子:CO2、BeCl2、HCN、C2H2等;②V形分子:H2O、H2S、SO2、SCl2等;③平面三角形分子:BF3、SO3、CH2O等;④平面形分子:C2H4、苯(C6H6)、CH2=CH—CH=CH2(丁二烯)、CH2=CH—C CH(乙烯基乙炔)等;⑤三角锥形分子:NH3、PH3、NCl3等;⑥正四面体形分子:CH4、CCl4、SiF4、SiH4等;⑦CH3Cl、CH2Cl2、CHCl3等是四面体形分子而不是正四面体形。
27.常见等电子体(必须牢记,可作为解题模型):
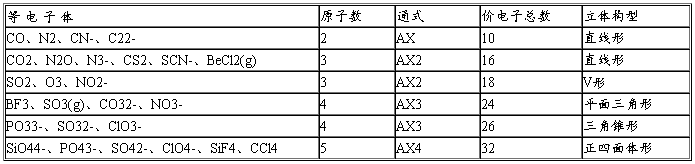
28.①杂化规律:杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。以sp3杂化形成的都是σ键,若碳原子采取sp2或sp杂化,则还有未参与杂化的p轨道,可用于形成π键。
②C原子形成4个σ键(N原子形成3个σ键、O原子形成2个σ键),则杂化轨道类型必为sp3;
③C原子形成3个σ键和1个π键(N原子形成2个σ键和1个π键),则杂化轨道类型必为sp2;
④C原子形成2个σ键和2个π键(N原子形成1个σ键和2个π键),则杂化轨道类型必为sp;
29.配位物的电离发生内界和外界间,内界离子难电离。如[Co(NH3)5Cl]Cl2的电离方程式为
[Co(NH3)5Cl]Cl2=[Co(NH3)5Cl]2+ + 2Cl-,1 mol 该配合物中,只有2 mol Cl-能被Ag+沉淀。
30.在ABn分子中,当A的化合价的绝对值等于该元素所在主族序数时,该分子为非极性分子,相反则为极性分子。如BF3、CO2等为非极性分子,NH3、H2O、SO2等为极性分子。
特别提醒:O3、H2O2是极性分子;PCl5(三角双锥)、SF6(正八面体)是非极性分子;CH4、C2H4、C2H2、均为非极性分子。
31.①只含非极性键的单质A2(如H2、O2、Cl2、N2、P4、C60等)一定是非极性分子;
②只含有极性键的双原子分子如HCl、NO等一定是极性分子;
③非极性分子中可能只含有非极性键(如Cl2)或只含有极性键(如CS2)或既含有极性键又含有非极性键(如C2H2);
④极性分子可能只含有极性键(如NH3)或既含有极性键又含有非极性键(如H2O2)。
32.ⅣA、ⅤA、ⅥA、ⅦA族元素氢化物的沸点变化规律:
ⅣA:PbH4>SnH4>GeH4>SiH4>CH4 ⅤA:BiH3>SbH3>NH3>AsH3>PH3
ⅥA:H2O>H2Te>H2Se>H2S ⅦA:HF>HI>HBr>HCl
33.①极性溶剂(如水)易溶解极性溶质;
②非极性溶剂(如苯、汽油、CCl4、CS2等)能溶解非极性物质(Br2、I2等);
③含有相同官能团的物质互溶,如水中含羟基(—OH)能溶解含有羟基的醇、酚、羧酸。
④如果存在氢键,则溶剂与溶质之间的氢键作用力越大,溶解性越好。
34.对于同种元素的不同含氧酸,该元素的化合价越高,其含氧酸的酸性越强。
特别提醒:酸的元数不一定等于酸中羟基上的氢原子数[如H3BO3是一元酸:B(OH)3+H2O B(OH)4- + H+],不一定等于酸中的氢原子数(如CH3COOH是一元酸)。
35.一般而言,晶胞是8个顶角相同的最小平行六面体,晶胞的平行棱相同,晶胞的平行面相同。因此晶胞的顶角、棱上、面上的原子分别是8个、4个、2个晶胞共用。
36.稀有气体晶体属于分子晶体,但不含化学键。
37.分子间只存在范德华力的晶体的共同特征:以1个分子为中心,其周围有12个分子紧邻,如CO2。
38.非金属单质和共价化合物中,大部分属于分子晶体,少数为原子晶体。
39.①金刚石中,每个C原子(sp3杂化)与4个C原子以共价键结合形成正四面体,键角为109°28′,最小环碳环为六元环,由于每个键为2个原子共有,所以1mol(12g)金刚石中含有2 mol C—C键。
②晶体硅的结构与金刚石相似。SiO2晶体中,每个Si原子与4个O原子结合形成正四面体,键角为109°28′,最小环为十二元环,含有6个Si原子和6个O原子, 1 mol (60g)SiO2中含有4 mol Si—O键,而不是2 mol。
③混合晶体——石墨,六边形平面层状结构。既有共价键(C—C),又含有金属键,还有范德华力(层间)。C原子数与C—C键个数之比为2:3。
40.金属键的强度差别很大,所以金属的熔点、沸点、硬度、密度差别很大。
41.①在金属晶体中只有阳离子没有阴离子。晶体中有阳离子不一定有阴离子,晶体中若有阴离子则一定有阳离子。
②金属Na、Mg、Al的熔点逐渐升高,金属Li、Na、K、Rb、Cs的熔点逐渐降低。
③离子化合物都是离子晶体,如强碱、活泼金属氧化物、大多数盐等。
④结构类型相同的离子晶体,离子电荷越高,离子半径越小,则晶体的晶格能越大。
42.晶体熔沸点高低比较:
离子晶体:比晶格能大小——看离子电荷和离子半径;
原子晶体:比共价键强度——看键能和键长的大小;
分子晶体:比分子间作用力的大小——看相对分子质量大小和是否存在氢键;
金属晶体:比金属键强弱——看阳离子半径和价电子多少。
43.1~20号元素原子核外电子排布的特殊性:
(1)最外层电子数为1的原子有H、Li、Na、K。
(2)最外层电子数为2的原子有He、Be、Mg、Ca。
(3)最外层电子数和次外层电子数相等的原子有Be、Ar。
(4)最外层电子数是次外层电子数2倍的原子是C。
(5)最外层电子数是次外层电子数3倍的原子是O。
(6)最外层电子数是次外层电子数4倍的原子是Ne。
(7)次外层电子数是最外层电子数2倍的原子有Li、Si。
(8)内层电子总数是最外层电子数2倍的原子有Li、P。
(9)电子层数和最外层电子数相等的原子有H、Be、Al。
(10)电子层数是最外层电子数2倍的原子是Li。
(11)最外层电子数是电子层数2倍的原子有He、C、S。
(12)最外层电子数是电子层数3倍的原子是O。
44.基态原子核外电子未成对电子个数的判断规律:
(1)有1个未成对电子:ⅠA、ⅢA、ⅦA;(2)有2个未成对电子:ⅣA、ⅥA;
(3)有3个未成对电子:ⅤA; (4)没有未成对电子:ⅡA、0族。
45.(1)离子晶体中一定含有离子键,可能含有极性共价键、非极性键、配位键。
(2)含有离子键的化合物一定是离子化合物。
(3)离子晶体一定是由阴、阳离子构成的,但晶体中可以含有分子,如结晶水合物。
(4)离子晶体中一定含有阳离子,但含有阳离子的晶体不一定是离子晶体。
(5)非金属元素间也可以形成离子化合物,如NH4Cl、NH4NO3等都是离子化合物。
(6)分子晶体中一定含有分子间作用力,可能含氢键。
(7)稀有气体形成的晶体是分子晶体,但稀有气体是单原子分子,其晶体中只含有分子间作用力。
(8)除稀有气体外的其他分子晶体均含有分子间作用力和分子内共价键。
(9)分子晶体中的分子间作用力决定物质的物理性质(如熔、沸点。硬度、溶解性等),而共价键决定分子的化学性质。
(10)原子晶体中一定有共价键,且只有共价键,无分子间作用力。
(11)原子晶体一定是由原子构成的,可以是同种元素的原子,也可是不同种元素的原子。
(12)共价化合物形成的晶体可能是原子晶体,也可能是分子晶体。
(13)含有共价键的化合物不一定是共价化合物。
(14)原子晶体可以是由极性键构成,也可以是非极性键构成。
(15)金属晶体中一定含有金属键,但有时也有不同程度的其他键,如合金中可能含共价键。
(16)金属键不一定就比分子间作用力强,如汞在常温下为液态,就说明汞中的金属键弱。第二部分高考真题“杂化”旨在“重组”,提高解题能力
1.以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是( )
(A):He (B) (C)1s2 (D)
2.某原子核外共有6个电子,分布在K与L电子层上,其基态原子在L层中分布正确的是( )
3.某元素的原子3d能级上有1个电子,它的N能层上的电子数是( )
(A)0 (B)2 (C)3 (D)5
4.下列有关物质结构的表述正确的是( )
(A)次氯酸的电子式 (B)二氧化硅的分子式SiO2
(C)硫原子的最外层电子排布式3s23p4 (D)钠离子的结构示意图
5.下列有关电子云和原子轨道的说法正确的是( )
(A)原子核外的电子象云雾一样笼罩在原子核周围,故称电子云
(B)s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
(C)p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多
(D)与s电子原子轨道相同,p电子原子轨道的平均半径随能层的增大而增大
6.下列表达式错误的是( )
(A)甲烷的电子式: (B)氮原子的L能层电子排布图:
(C)硫离子的核外电子排布式:1s22s22p63s23p4 (D)碳-12原子: C
7.某物质的实验式为PtCl4·2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
(A)配合物中中心原子的电荷数和配位数均为6
(B)该配合物可能是平面正方形结构 (C)Cl-和NH3分子均与Pt4+配位
(D)配合物中Cl-与Pt4+配位,而NH3分子不配位
8.下列叙述中正确的是( )
(A)离子化合物中不可能存在非极性键
(B)非极性分子中不可能既含极性键又含非极性键 (C)非极性分子中一定含有非极性键
(D)不同非金属元素原子之间形成的化学键都是极性键
9.若已知晶体中最近的Na+与Cl-核间距离为a cm,氯化钠的相对分子质量为M,NA为阿伏加德罗常数,则NaCl晶体的密度(单位:g/cm3)为( )
(A) (B) (C) (D)
10.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
(A)金属性Y>Z (B)氢化物的沸点X>W
(C)离子的还原性X>W (D)原子及离子半径Z>Y>X
11.同周期的A、B、C三种非金属元素,已知最高价氧化物对应的水化物的酸性由强到弱的顺序是HAO4>H2BO4>H3CO4,则下列判断正确的是( )
①原子半径A<B<C;②非金属性A>B>C;③单质氧化性A>B>C;④气态氢化物的稳定性HA<H2B<CH3;⑤阴离子(或负价态)的还原性A-<B2-<C3-;⑥第一电离能A>B>C;⑦最低负化合价的绝对值C<B<A;⑧电负性A>B>C。
(A)①②③⑤⑧ (B)②③⑥⑧ (C)④⑥⑦ (D)除④、⑦以外
12.具有下列电子层结构的原子,其第一电离能由大到小排列正确的是( )
①3p轨道上只有一对成对电子的原子;②外围电子排布为3s23p6的原子;③其3p轨道为半充满的原子;④正三价的阳离子的电子层结构与氖原子相同的原子。
(A)①②③④ (B)③①②④ (C)②③①④ (D)②④①③
13.下列有关σ键和π键的说法错误的是( )
(A)含有π键的分子在反应时,π键比σ键易断裂
(B)当原子形成分子时, 一定形成σ键,可能形成π键
(C)有些原子在与其他原子形成分子时,只能形成σ键,不能形成π键
(D)在分子中,化学键可能只有π键而没有σ键
14.下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2 ③HCHO ④CH CH ⑤NH3 ⑥CH4
(A)①②③ (B)①⑤⑥ (C)②③④ (D)③⑤⑥
15.下列分子中,中心原子以sp2杂化且属于极性分子的是( )
(A)NH3 (B)BF3 (C)CH2O (D)CCl4
16.下列有关性质判断正确且可以由范德华力来解释的是( ),与氢键有关的是( )
(A)沸点:HBr>HCl (B)沸点:CH3CH2Br<C2H5OH
(C)稳定性:HF>HCl (D)—OH上氢原子的活泼性:H—O—H>C2O5—O—H
17.下列说法中正确的是( )
(A)离子晶体中每个离子的周围均吸引着6个带相反电荷的离子
(B)金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动
(C)分子晶体的熔、沸点很低,常温下均呈液态或气态
(D)原子晶体中的各相邻原子都以共价键相结合
18.下列化合物,按其晶体的熔点由高到低排列正确的是( )
(A)SiO2、CsCl、CBr4、CF4 (B)SiO2、CsCl、CF4、CBr4
(C)CsCl、SiO2、CBr4、CF4 (D)CF4、CBr4、CsCl、SiO2
19.下列各选项所述的两个量,前者一定大于后者的是( )
①Al原子和N原子的未成对电子数;②Ag+、Cu2+与NH3形成配合物时的配位数;③NaCl的晶格能与MgO的晶格能;④F元素和O元素的电负性;⑤N和O元素的第一电离能;⑥H原子和H+的半径。
(A)①④⑤ (B)②④⑥ (C)④⑤⑥ (D)③⑤⑥
20.下列有关几种气体分子的说法不正确的是( )
(A)CO的结构式可表示为C=O (B)CO2与OCS(硫化羰)互为等电子体
(C)NH3分子中氮原子采用sp2杂化 (D)HCN分子呈直线形
21.(1)铝元素的原子核外共有 种不同运动状态的电子, 种不同能级的电子。
(2)W元素的原子的最外层电子数是次外层电子数的3倍,W元素原子的L层电子排布式为
(3)Ni原子核外电子排布式为 。
(4)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为 。
22.(1)①CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为 。
②黑火药是中国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑(已配平),除S外,其他四种元素的电负性从大到小依次为 。
(2)已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
(A)非金属性:Y比X弱 (B)气态氢化物稳定性:HmY比HnX强
(C)最高价含氧酸的酸性:X对应酸的酸性强于Y对应酸的酸性
(D)X和Y形成的化合物中,X显负价,Y显正价
23.①CS2是一种常用的溶剂,CS2的分子中存在 个σ键。
②已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为 。
24.(1)科学家常用等电子体来预测不同物质的结构,例如CH4与NH4+有相同的电子数和空间构型,依此原理在下面的空格中填上相应化学式。

(2)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ;1 mol O22+中含有π键的数目为 。
25.(1)用价层电子对互斥理论确定HCN、BF3、NH4+和SO32-的VSEPR模型和它们的立体构型。
(2)下列分子或离子中,VSEPR模型名称与分子或离子的立体构型名称不相同的是( )
(A)CO2 (B)H2O (C)CO32- (D)CCl4
26.(1)NiO、FeO的晶体结构类型均与氯化钠的相同。
①Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”)
②NiO晶胞中Ni和O的配位数分别是 、 ;
(2)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心。该化合物化学式为 ,每个Ba2+与 个O2-配位。
27.(1)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为 ,Q2+的未成对电子数是
(2)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示:
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是 ,氮镍之间形成的化学键是 ;
②该结构中,氧氢之间除共价键外还可存在 ;
③该结构中,碳原子的杂化轨道类型有 。
(3)下列判断中正确的是( )
(A)二氧化硅的分子式为SiO2 (B)晶体中一定存在化学键
(C)熔点:Si3N4>NaCl>SiI4 (D)沸点:NH3>PH3>AsH3
【强烈建议】未经自己独立完成上述各题之前,请不要往后看!版面所限,大型元素推断从略,若有需要,敬请访问:http://81928819.qzone.qq.com/ http://792669199.qzone.qq.com/ 自行下载
参考答案 仅供参考
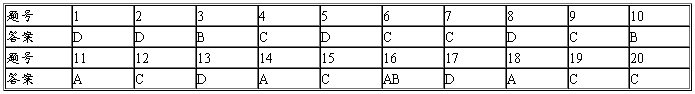
21.(1)13 5(2)2s2sp4 (3)1s22s22p63s23p63d 84s2或[Ar]3d84s2 (4)1s22s22p63s23p63d10.
22.(1)①C>H>Si ②O>N>C>K (2)B 23.①2 ②1:1
24.(1)C2H6 NO3- CO2 N2O4 C22- (2) 2NA 25.B
26.(1)①> ②6 6 (2)BaPbO3 12
27.(1)3d84s2 4 (2)①σ键和π键 配位键 ②氢键 ③sp3、sp2 (3)C
