人教版高中化学选修3知识点
第一章 原子结构与性质
第一节 原子结构
1. 什么叫能层 能级
2. 能层中能级符号顺序
3. 能级数与能层序数的关系
4. 画出构造原理图
5. 练习写出1-36号元素原子基态电子排布式
6. 练习简化电子排布式的写法(铁 硅)
7. 能量最低原理
8. 基态 激发态
9. 可见光产生的原因
10. 电子云 原子轨道
11. S .P原子轨道的形状
12. 练习画基态原子的 电子排布图
13. 泡利原理 洪特规则的内容
14. 原子排布规律
第二节 原子结构与元素的性质
1. 画出前36号元素在周期表中的位置
2. 什么叫价电子
3. 周期表中的5个区
4. 电离能 电负性的概念及应用 .电离能 , 电负性最大的原子
5. 元素周期律的具体内容(原子半径,得失电子能力,氧化性,还原性,化合价,金属性,非金属性,气态氢化物的稳定性。最高价氧化物对应的水化物的酸碱性,第一电离能,电负性)
6. 对角线规则的 含义
7. 惰性气体的相对稳定性
第二章 分子结构与性质
第一节 共价键
1. 什么叫化学键 离子键 共价键 电子式
2. 运用电子云 原子轨道怎样理解共价键
3. 怎样判断化学键的类型
4. 键能 键长 键角(应用)
5. 共价键的特性
6. 西戈马键 派键的特征及比较
7. 等电子原理
第二节 分子的立体结构
1. 分析分子的结构(三原子,四原子,五原子)
2. CO2 H2O CH2O NH3 CH4的立体结构
3. 价层电子对互斥模型理论
A 中心原子都用于形成共价键
B中心原子上有孤对电子
4. 理解杂化轨道理论(SP,SP2,SP3)及应用
5. 什么叫配位键 中心离子 配位体 配位数 配位化合物(举例)
6. 向硫酸铜溶液中逐滴加入氨水的实验现象 离子方程式
7. 向氯化铁溶液中加入硫氰化钾溶液的现象 离子方程式(指出中心离子 配位体)
8. 用配位键表示四氨合铜络离子
第三节 分子的性质
1. 共价键的分类
2. 怎样区分极性分子 非极性分子
3. 什么叫范德华力
4. 范德华力对分子晶体的熔沸点有怎样的影响
5. 对结构相似的分子晶体怎样判断范德华力的大小
6. 什么叫氢键 易形成氢键的原子有那些 氢键是否属于化学键
7. 分子内形成氢键 分子间形成氢键有什么不同
8. 影响物质的溶解性的因素有那些
9. 什么叫手性原子 手性分子
10. 怎样比较无机含氧酸的酸性
第三章 晶体结构与性质
1. 晶体的分类
2. 晶体与非晶体的区别
3. 形成晶体的方法
4. 什么叫晶胞
5. 平行六面体晶胞中微粒个数的算法
6. 什么叫分子晶体
7. 特征
8. 典型的分子晶体
9. 干冰的密度为什么比冰高
10. 什么叫原子晶体
11. 原子晶体特征
12. 典型原子晶体
13. 什么叫金属键
14. 电子气理论
15. 用电子气理论解释金属的延展性 导电性
16. 金属原子在二维平面放置的方式 配位数都是多少
17. 金属原子的三维堆积方式有几种
18. 什么叫离子晶体
19. NaCl CsCl CaF2中各离子的配位数是多少
20. 离子晶体的特征
21. 同族元素的碳酸盐稳定性怎样判断
22. 什么叫晶格能
23. 影响晶格能的因素
24. 晶格能的应用
第二篇:【人教版】高中化学选修3知识点总结:第二章分子结构与性质
第二章分子结构与性质
课标要求
1.了解共价键的主要类型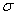 键和
键和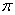 键,能用键长、键能和键角等说明简单分子的某些性质
键,能用键长、键能和键角等说明简单分子的某些性质
2.了解杂化轨道理论及常见的杂化轨道类型(sp、sp2、sp3),能用价层电子对互斥理论或者杂化轨道理论推测常见的简单分子或离子的空间结构。
3.了解简单配合物的成键情况。
4.了解化学键合分子间作用力的区别。
5.了解氢键的存在对物质性质的影响,能列举含氢键的物质。
要点精讲
一.共价键
1.共价键的本质及特征
共价键的本质是在原子之间形成共用电子对,其特征是具有饱和性和方向性。
2.共价键的类型
①按成键原子间共用电子对的数目分为单键、双键、三键。
②按共用电子对是否偏移分为极性键、非极性键。
③按原子轨道的重叠方式分为σ键和π键,前者的电子云具有轴对称性,后者的电子云具有镜像对称性。
3.键参数
①键能:气态基态原子形成1 mol化学键释放的最低能量,键能越大,化学键越稳定。
②键长:形成共价键的两个原子之间的核间距,键长越短,共价键越稳定。
③键角:在原子数超过2的分子中,两个共价键之间的夹角。
④键参数对分子性质的影响
键长越短,键能越大,分子越稳定.

4.等电子原理[来源:学§科§网]
原子总数相同、价电子总数相同的分子具有相似的化学键特征,它们的许多性质相近。
二.分子的立体构型
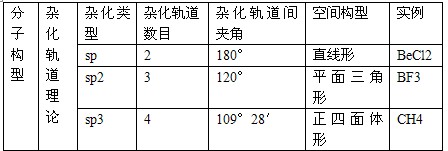
1.分子构型与杂化轨道理论
杂化轨道的要点
当原子成键时,原子的价电子轨道相互混杂,形成与原轨道数相等且能量相同的杂化轨道。杂化轨道数不同,轨道间的夹角不同,形成分子的空间形状不同。
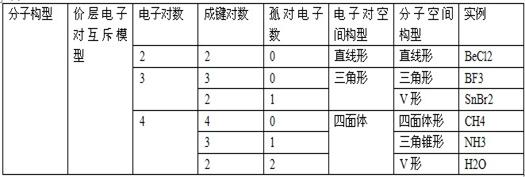
2分子构型与价层电子对互斥模型
价层电子对互斥模型说明的是价层电子对的空间构型,而分子的空间构型指的是成键电子对空间构型,不包括孤对电子。
(1)当中心原子无孤对电子时,两者的构型一致;
(2)当中心原子有孤对电子时,两者的构型不一致。
3.配位化合物
(1)配位键与极性键、非极性键的比较
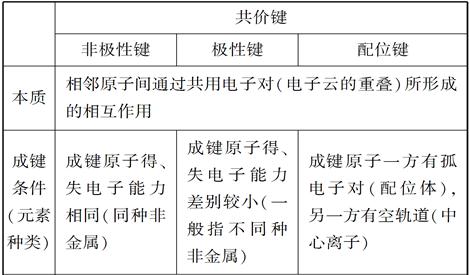

(2)配位化合物
①定义:金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物。
②组成:如[Ag(NH3)2]OH,中心离子为Ag+,配体为NH3,配位数为2。
三.分子的性质
1.分子间作用力的比较
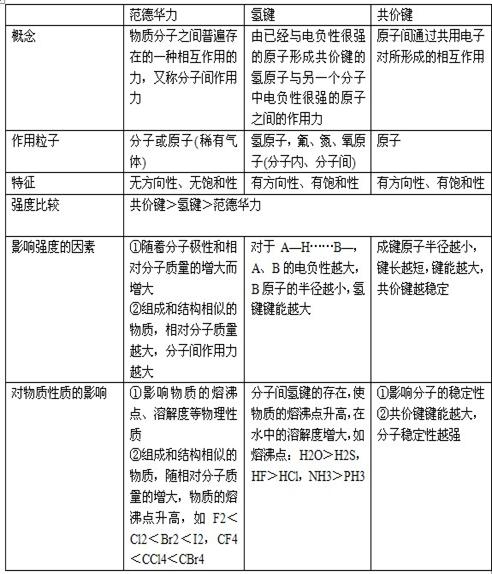
2.分子的极性
(1)极性分子:正电中心和负电中心不重合的分子。
(2)非极性分子:正电中心和负电中心重合的分子。
3.溶解性
(1)“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,
极性溶质一般能溶于极性溶剂.若存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越好。
(2)“相似相溶”还适用于分子结构的相似性,如乙醇和水互
溶,而戊醇在水中的溶解度明显减小.
4.手性
具有完全相同的组成和原子排列的一对分子,如左手和右手一样互为镜像,在三维空间里不能重叠的现象。
5.无机含氧酸分子的酸性
无机含氧酸可写成(HO)mROn,如果成酸 元素R相同,则n值越大,R的正电性越高,使R—O—H中O的电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如HClO<HClO2<HClO3<
元素R相同,则n值越大,R的正电性越高,使R—O—H中O的电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如HClO<HClO2<HClO3< HClO4。
HClO4。
