第四单元 自然界中的水 知识点
1、水的组成:
(1)电解水的实验
A.装置―――水电解器
B.电源种类―――直流电
C.加入硫酸或氢氧化钠的目的―――增强水的导电性
D.化学反应:2H2O2H2↑+ O2↑
产生位置 负极 正极
体积比 2 :1
质量比 1 :8
F.检验:
O2---出气口置一根带火星的木条----木条复燃
H2---出气口置一根燃着的木条------气体燃烧,产生淡蓝色的火焰
(2)结论:
①水是由氢、氧元素组成的。
②一个水分子是由2个氢原子和1个氧原子构成的。
③化学变化中,分子可分而原子不可分。
例:根据水的化学式H2O,你能读到的信息
化学式的含义 H2O
①表示一种物质 水这种物质
②表示这种物质的组成 水是由氢元素和氧元素组成的
③表示这种物质的一个分子 一个水分子
④表示这种物质的一个分子的构成 一个水分子是由两个氢原子和一个氧原子构成的
2、水的化学性质
(1)通电分解:2H2O2H2↑+O2↑
(2)水可遇某些氧化物反应生成碱(可溶性碱),例如:H2O+CaO==Ca(OH)2
(3)水可遇某些氧化物反应生成酸,例如:H2O+CO2==H2CO3
3、水的污染:
(1)水资源
A.地球表面71%被水覆盖,但供人类利用的淡水小于 1% 。
B.海洋是地球上最大的储水库。海水中含有80多种元素。海水中含量最多的物质是 H2O,最多的金属元素是 Na ,最多的元素是 O 。
C.我国水资源的状况分布不均,人均量少。
(2)水污染
A、水污染物:工业“三废”(废渣、废液、废气);农药、化肥的不合理施用:生活污水的任意排放。
B、防止水污染:工业三废要经处理达标排放、提倡零排放;生活污水要集中处理达标排放、提倡零排放;合理施用农药、化肥,提倡使用农家肥;加强水质监测。
(3)爱护水资源:节约用水,防止水体污染。
4、水的净化
(1)水的净化效果由低到高的是静置、吸附、过滤、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭。
(2)硬水与软水
A.定义: 硬水是含有较多可溶性钙、镁化合物的水;
软水是不含或含较少可溶性钙、镁化合物的水。
B.鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水。
C.硬水软化的方法:蒸馏、煮沸。
D.长期使用硬水的坏处:浪费肥皂,洗不干净衣服;锅炉容易结成水垢,不仅浪费燃料,还易使管道变甚至引起锅炉爆炸。
(3)过滤:
过滤是一种将固体和液体分离的基本操作方法,操作时注意“一贴二低三靠”。 “一贴”:滤纸紧贴漏斗内壁,中间不要留有气泡;
“二低”:滤纸边缘低于漏斗边缘;液面低于滤纸边缘;
“三靠”:玻璃棒靠在滤纸的三层折叠处;装混合液的烧杯口紧靠玻璃棒;漏斗下端管口紧靠盛接滤液的烧杯内壁。
5、氢气(H2)
A、物理性质:密度最小的气体(向下排空气法);难溶于水(排水法)。
B、化学性质:
a.可燃性(用途:高能燃料;氢氧焰焊接,切割金属)
2H2+O22H2O(点燃前,要验纯)
现象:发出淡蓝色火焰,放出热量,有水珠产生。
b.还原性(用途:冶炼金属)
H2+CuO Cu+H2O(氢气“早出晚归”)
现象:黑色粉末变红色,试管口有水珠生成
(小结:既有可燃性,又有还原性的物质:H2、C、CO)
C、氢气的实验室制法
原理:Zn+H2SO4 === ZnSO4+H2↑ Zn+2HCl === ZnCl2+H2↑
不可用浓盐酸的原因 浓盐酸有强挥发性;
不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性。
D、氢能源 三大优点无污染、放热量高、来源广。
6、其他
(1)水是最常见的一种溶剂,是相对分子质量最小的氧化物。
(2)水的检验:用无水硫酸铜,若由白色变为蓝色,说明有水存在;CuSO4+5H2O = CuSO4·5H2O
(3)水的吸收:常用浓硫酸、生石灰。
7、化学式
A、定义:由元素符号表示物质组成的式子叫做化学式
B、只有纯净物才能用化学式表示其组成,一种物质只能用一个化学式来表示。
C、意义:
①表示一种物质;
②表示一种物质由哪几种元素组成(物质-元素-组成);
③表示该物质的一个分子;
④表示该物质的一个分子中有哪几种原子,每种原子各有几个(分子-原子-构成)。
D、化学式写法:
a.单质:金属、稀有气体及大多数固态非金属通常用元素符号表示它们的化学式;而氧气、氢气、氮气、氯气等非金属气体的分子由两个原子构成,其化学式表示为O2、H2、N2、Cl2。
b.化合物:正价在前,负价在后(NH3,CH4除外)。
E、意义:
例:化学式的含义 H2O
①表示一种物质 水这种物质
②表示这种物质的组成 水是由氢元素和氧元素组成的
③表示这种物质的一个分子 一个水分子
④表示这种物质的一个分子的构成 一个水分子是由两个氢原子和一个氧原子构成的
8、化合价
A、化合价表示原子之间相互化合的数目
B、原子团:作为一个整体参加反应的原子集团,也叫做根。如:SO4、CO3、NO3、NH4、OH。
C、注意事项:
(1)元素的化合价是元素的原子在形成化合物时表现出来的性质,因此,在单质分子里,元素的化合价为“0” 。
(2)化合价有正负之分,在化合物里:
①氧元素通常显“-2”价;氢元素通常显“+1”价;
②金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价; ③非金属氧化物中,非金属元素显正价;
④一些物质在不同(或相同)物质中可显不同的化合价;
⑤在化合物里正负化合价的代数和为0;
⑥原子团的化合价等于其中元素化合价的代数和(不为0)应标在原子团的整体正上方。
附:化合价记忆法:
一价:钾、钠、氯、氢、银;
二价:氧、钙、钡、镁、锌;
三(价)铝,四(价)硅,五价磷;
二、三(价)铁,二、四(价)碳;
二、四、六(价)硫都齐全;
铜、汞二价最常见。
9、根据化合价求化学式
(1)最小公倍数法
a.写出元素符号,正价在左,负价在右。
b.求两种元素化合价绝对值的最小公倍数。
c.求各元素的原子数。
d.把原子数写在各元素符号的右下方。
e.按正负化合价的代数和为0的原则检查化学式。
(2)十字交叉法
a.写出元素符号,标出化合价,正价在左,负价在右。 b.取化合价绝对值,约去最大公约数。
c.用约后的数十字交叉写在元素符号右下角。
10、利用化学式推求化合价
在化合物里正负化合价的代数和为0。
如:KClO3中氯元素的化合价;+1 + x +(-2)×3 = 0,解得 x= + 5。
11、根据化学式的有关计算
a.元素质量比:
化学式AmBn中A,B元素质量比为(a×m) :(b×n)(a,b为A,B元素的相对
原子质量)
如:H2O中 H:O (1×2):(16×1)=1:8。
b.相对分子质量:
化学式AmBn相对分子质量为(a×m)+(b×n)
如:H2O相对分子质量为 (1×2)+(16×1)=18
c.元素质量分数
元素质量分数=×100%
×100% =11.11%。 如:H2O中H元素的质量分数=
d.R元素质量=化合物质量×R元素的质量分数 如:求100克水(H2O)中氢元素的质量。
100g×11.11%=11.11g
第二篇:九年级化学人教版第四单元《自然界的水》测试题
九年级人教版化学第四单元《自然界的水》测试题
(测试时间60分钟 满分80分)
一、选择题(每题只有一个选项符合题意,每小题1分,共20分)
1、普鲁卡因(化学式是C13H20O2N2)是一种止痛药剂,下列说法中正确的是?( )
A、普鲁卡因是由碳、氢、氧、氮四种元素组成的 B、普鲁卡因中含有氮气分子
C、普鲁卡因中碳、氢、氧、氮四种元素质量比为13∶20∶2∶2
D、普鲁卡因的相对分子质量为37
2、元素X核外有11个电子元素Y核外有16个电子,这两种元素可能形成的化合物是( )
A、XY
B、X2Y C、XY2 D、XY6
3有关水的电解实验,下列说法正确的是 ( )
A.与电源正级相连的一端产生的气体能燃烧 B.正、负二极产生气体的质量比为1:2 C.证明水是由氢气和氧气组成的 D.证明水是由氢元素和氧元素组成的
4. 水是生命之源,以下生活中的“水”能看成纯净物的是 ( )
A.矿泉水 B.结冰的海水 C.自来水 D.结冰的蒸馏水 5.下列常见物质中,属于氧化物的是 ( )
A.氯化钾(KCl) B.四氧化三铁(Fe3O4) C.甲烷(CH4) D.氯酸钾(KClO3) 6 保持水的化学性质的最小粒子是 ( )
A.水分子 B.氢分子 C.氧分子 D.氢原子和氧原子
7. 图中分别表示三种不同的分子,它们在一定条件下反应,前后的变化如右图所示:下列叙述错误的是 ( )
A.分子是在不断运动的 B.分子之间有间隔的
C.化学反应前后分子的种类发生改变 D.化学反应前后原子的种类发生改变
8.20xx年世界水日的主题是“应对水短缺”。下列应对水短缺的措施:①推广使用无磷洗衣粉;②加强工业废水的达标排放;③加快生活污水净化处理的建设;④合理使用农药和化肥;⑤提倡节约用水,合理的的是 ( )
A.①②③ B.①②④⑤ C.②③④⑤ D.①②③④⑤ 9.下列实验的最终现象可以证明分子总是在不断运动着的是( )。
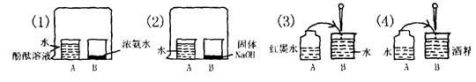
A.只有⑴ B.只有⑴⑵ C.只有⑴⑵⑶ D.全部 10.下列水的净化操作,净化程度最高的是 ( ) A.静置沉淀 B.吸附沉淀 C.过滤 D.蒸馏
11.下列鉴别硬水和软的方法,最简单的是( ) A. 煮沸 B.加肥皂水 C.过滤 D.蒸馏
12.一瓶气体,经检验得知只含有一种元素,对该气体的叙述错误的( )
A. 可能是一种单质 B.一定不是化合物 C.可能是一种混合物 D.可能是一种氧化物 13.下列现象与空气的水蒸气无关的是( )
A. 酥脆的饼干放置在空气中变软B.夏天打开冰箱时,冒白气
C.寒冷冬季,清晨的窗玻璃上出现冰花D.放置在空气的石灰水表面出现一层白膜 14.水是人类赖以生存的重要物质。下列关于水的说法中正确的是( )
A.水是取之不尽,用之不竭的 B.在水中加入明矾可将硬水变为软水 C.长期饮用蒸馏水对人体健康无益 D.雨水是天然的纯净物
15.小明同学对泥水进行过滤后发现液体仍然混浊,下列解释有误的是( )
A. 仪器不洁净
B.液面超过的滤纸的边缘
C.滤纸破损 D.漏斗下端未靠在下面烧杯的内壁上
16、交警用于检测司机是否酒后开车的检测仪中含有的一种成份是重铬酸钾(K2Cr2O7),其中铬元素的化合价是( )
A、+3 B、+4 C、+5 D、+6
17、下列符号不具有宏观意义,只有微观意是

………………………( )
A.Zn
B.H2 C.2NO D.MgCl2
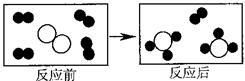
18、下图是表示气体分子的示意图,图中“●”和“Ο”分别表示质子数不同的两种原子,其中表
示化合物的是 ?????????????????( )
19、我国科学家发现用含硒(Se)的化合物亚硒酸钠能消除加速人体衰老的活性氧,亚硒酸钠中的硒
元素为+4价,氧元素为-2价,则亚硒酸钠的化学式为 ( )
A.Na2SeO3 B.Na2SeO4 C.NaSeO2 D.Na2SeO2
20、下列五种物质中均含有碘元素,它们按碘的化合价的顺序排列:①KI ②I2 ③HIO ④X ⑤
NaIO4。则根据这种排列规律,X不可能是 ( ) A.AgI B.KIO3 C.I204 D.I205
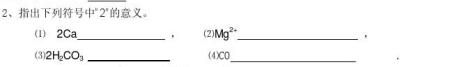
二、填空(每空1分,共47分) 1、用文字或化学符号表示。
钠元素 三个钾原子 两个氧分子
4个硫酸根离子
② ; ③ 。
7.黄曲霉素AFTB(化学式是C17H12O6)是污染粮食(大米、花生等)的真菌霉素,人类的特殊基因在黄曲霉素作用下会发生突变,继而转为肝癌。
(1)黄曲霉素AFTB由 种元素组成。
(2)一个黄曲霉素AFTB分子中共 个原子。 (3)黄曲霉素AFTB的相对分子质量是 。
(4)黄曲霉素AFTB分子中氧元素的质量分数是 。
-2价的硫元素 氢氧化钠 食盐(氯化钠) 氧化钙 四 计算题 (13分)
1、市售尿素中,主要成分甲酰胺[化学式为:CO(NH2)2]含量在96%以上为达一级产品。请回答:
⑴ 甲酰胺中氢、氧、氮三种元素质量比为 _____________。
标
硫化锌 MnO2AgCl 2MnO42 3个氢分子 2个钙离子 硝酸根离子 铵根离子
⑵ 甲酰胺中,氮元素的质量分数为
⑶经测定,某块农田需补充氮元素93.4Kg,请计算需要施用这种尿素多少千克?(注:第⑵、⑶
题结果保留一位小数)
(解答本题需要用到的相对原子质量H—1,C—12,N—14,O

—16.)
3、科学研究证实,物质是由粒子构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具
体粒子的名称。 2、20xx年10月16日,我国自行研制的“神舟”五号载人飞船顺利发射和返回。运送飞船的
长征二号F型运载火箭所使用的燃料是偏二甲肼(化学式是C2H8N2)。偏二甲肼相对分子质量
(1)体温计中的汞是由 构成的。
是 ,各元素的质量比是 。
(2)植物光合作用产生的氧气是由 构成的。
(3)用于配制生理盐水的氯化钠晶体是由 构成的。
3、某厂生产的化肥硝酸铵的包装袋上注明有如图 4. 现有①铁屑;②液态空气;③水;④二氧化硫;⑤过氧化氢;⑥混浊的泥水;⑦红磷;⑧氯酸
字样,问:如果杂质不含氮元素,则该化肥的纯度
钾和二氧化锰完全反应的剩余固体,其中属于单质的是 (填序号,下同),属于化合
物的是 ,属于氧化物的是 ,属于混合物的是 。
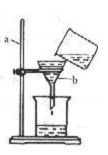
5. 含有较多可溶性钙和镁的化合物的水叫 ,不含或含有较少可溶性钙和镁的化合物的水叫 ,区别这两种水可用 ,如果泡沫多,浮渣少,则是 ,在生活中可用 的方法将硬水软化。 6. 下图是某同学用来除去水中难溶性杂质时所采用的过滤装置图。 试回答:(1)写出标号仪器的名称:a ,b 。 (2)该图中存在的三处明显错误,你能指出来并加以改正吗?:
① ;
