光明香烟
座谈会定性分析报告
二〇##年九月三日
座谈会城市:沈阳、大连、长春、通化
目 录
第一部分 香烟消费的消费者状况... 3
一、香烟消费的消费者状况... 3
二、消费者抽烟原因... 3
第二部分 对香烟品牌的分析... 4
一、对香烟的品牌认知... 4
二、主要地产烟及最受欢迎的香烟品牌... 6
三、消费者对当前香烟市场上主要吸味的认识度及偏好... 6
四、对常抽香烟品牌形象的认知... 7
五、对于新品牌的香烟投放当地市场的接受度... 7
六、怎样的香烟才使烟民心目中最理想的烟... 7
七、广告及促销... 8
第三部分 对光明香烟的评价... 8
一、对光明香烟包装、吸味、价格评价... 8
二、对光明香烟包装视觉心理测试结果... 10
第一部分 香烟消费的消费者状况
一、香烟消费的消费者状况

分析:长春、通化、沈阳、大连四地被访者在抽烟量、月香烟花费、购买渠道等方面的情况基本一致。同时也可以看出,价格在3~4元的香烟在当地占主流。在购买地点的选择上都为随机性选择购买地点,多集中在小卖铺或日杂店。这就印证了香烟作为一种特殊的快速消费品,足够大的“上柜率”是产生良好销量的一个前提保证。
二、消费者抽烟原因

分析:毫无疑问,对于中度的烟民和重度的烟民来说,香烟已经成为他们生活中不可或缺的一部分。香烟不仅仅是作为一种日常消费品进入一般人的生活,更深深的融入烟民每日的生活。对它的依赖就好比对油盐酱醋茶的依赖一样,在某种意义上已成为生活的“必需品”。而香烟的依赖又高于一般的生活必需品,因为香烟是一种长期吸会上瘾的东西,一旦上瘾就没有其他的替代品可以替代。
第二部分 对香烟品牌的分析
一、对香烟的品牌认知

1、被访者更换品牌的原因分析:
在长春、通化被访者中,都有更换品牌的经历,但这种更换多在没有成为真正烟民的初始阶段。一旦成为真正的烟民,这种更换的频率幅度会越来越小。另外被访者基本对当地品牌烟的忠诚度相对较高,“本地人,抽本地烟”,是两地烟民对当地烟偏好的固有观念。
沈阳、大连被访者中年龄层次相对小一些、个性更为外向多语的年轻人、以沟通作为职业手段的人(如保险推销员)更倾向于更换香烟品牌。这部分人对生活的态度和对待新事物的接受程度就决定他们一定是会在不同品牌之间作尝试。烟对于他们来说是用来炫耀展示自己或者联络工作的“工具”甚至“道具”。大连没有当地产的烟,但是当地的烟民对云烟的忠诚度普遍高于其他。同时,大连的被访者对更换自己最常吸的香烟品牌的意愿程度和沈阳的烟民相比要低很多。
2、被访者保持相对品牌忠诚的原因分析
保持相对品牌忠诚的基本是年龄层次上相对大一些的被访者,他们对生活的积累就决定了他们不可能有太多的冲动去改变自己的长期形成的生活模式。吸烟是他们日常生活的一部分,和某个品牌之间建立起来的信任和亲切感暂时是很难有其他品牌可以替代的。烟对于他们来说更多的是陪伴自己过日子的“必需品”。
与会的烟民对自己目前正在吸的烟表示出非常高的忠诚度,基本上在品牌的转换方面没有太多需求。并且是比较强烈的表示不会考虑更换品牌,除非是自己最常吸的香烟有新产品投放市场才有可能会尝试一下。
二、主要地产烟及最受欢迎的香烟品牌

三、消费者对当前香烟市场上主要吸味的认识度及偏好
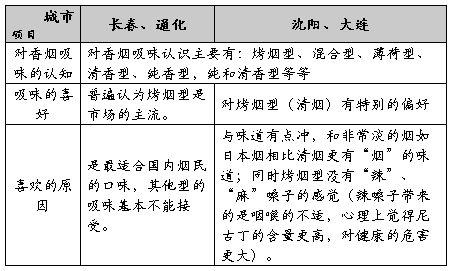
四、对常抽香烟品牌形象的认知
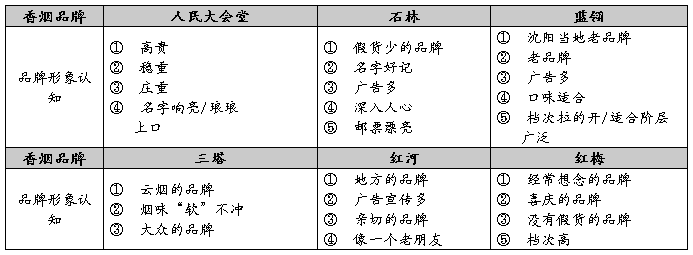
五、对于新品牌的香烟投放当地市场的接受度
多数被访者反映不会主动性的购买,观望现象是主流(如果大家都抽,也会去买),如果购买也是尝试性的购买,试试口味,完全替换现有的品牌不太可能,但如果是云南生产的某个香烟品牌就另当别论,因为云南产地的香烟在国内的知名度、信赖度都高于其他的外产烟。
六、怎样的香烟才使烟民心目中最理想的烟
吸味第一(被访者认为,包装再精致,价格再便宜,如果吸味不好,不会第二次购买,甚至第一次买了也有上当的感觉);
包装第二(吸味好,价格又便宜,如果包装不好,只能在家中抽,在日常交往和大众场合下,很难拿出手);
价格第三(如果价位高出了地产烟中某个最受当地人欢迎的香烟价格,就很难被接受了,毕竟当地的工薪阶层的月收入摆在这里。所以烟民月收入的水平决定了购买香烟的价位)。
七、广告及促销
通过长春、通化、沈阳、大连四个城市的座谈,多数被访者对“大红鹰”和“白沙”香烟的电视广告的认识度较高,但对其广告语的知晓度“白沙”——“鹤舞白沙,我心飞翔”远高于“大红鹰”——“大红鹰,胜利之鹰”。对于国内其他香烟品牌电视广告的知晓度较低。长春、通化、沈阳三个城市地产烟的广告多集中在,灯箱、路牌、横幅和店堂的海报上。他们对外烟中“三五”、“万宝路”、“七星”的广告(主要是灯箱、路牌)的形象,多给予较高的评价。
在促销方面,东北人爽朗的性格,决定了大多数的烟民对于香烟销售中采取的积攒烟盒、册子积点、收集卡片再兑付奖品的促销形式不感兴趣,认为太麻烦、太小气、不爽快,还是直接点好,如有中奖就现场兑付,如香烟或返还现金等。
第三部分 对光明香烟的评价
一、对光明香烟包装、吸味、价格评价
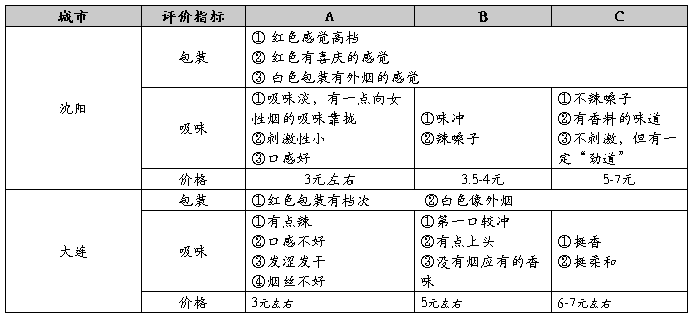
一、对光明香烟包装、吸味、价格评价(续)

二、对光明香烟包装视觉心理测试结果


第二篇:分析实验报告
验证某未知混合试液含有Fe3+、Cu2+、Ni2+、Pb2+离子并测量各离子含量
一、实验目的
通过用配位滴定方法定性与定量分析混合溶液中各金属离子的浓度;熟悉配位滴定的原理和操作,以及各金属离子的性质和配位滴定中需要注意的问题(包括PH的控制以及副反应,掩蔽剂的选择,直接滴定法和返滴定法以及置换滴定的条件)。
二、目前有关本次实验中所测元素常量测定方法的概述
1.络合滴定法
实验室常用的方法之一,采用有机络合剂与所需要检验的金属离子发生络合反应,生成稳定的络合物或络合离子,借用合适的指示剂指示反应的终止。而常采用的络合剂是EDTA溶液,在使用EDTA之前要利用Zn2+ 标准溶液进行标定再使用。通过EDTA滴定消耗的体积量,间接求得所求金属离子含量。
2.ICP-AES法测量重金属,即电感耦合等离子体原子发射光谱法
目前,金属元素测定方法主要有原子吸收分光光度法和电感耦合等离子体原子发射光谱法(ICP-AES)。原子吸收分光光度法虽是一种成熟方法,但测定速度较慢、干扰物质复杂。电感耦合等离子体原子发射光谱法是以电感耦合等离子矩为激发光源的一类光谱分析方法。
其原理为等离子体发射光谱法可以同时测定样品中多元素的含量。当氩气通过等离子体火炬时,经射频发生器所产生的交变电磁场使其电离、加速并与其他氩原子碰撞。这种链锁反应使更多的氩原子电离,形成原子、离子、电子的粒子混合气体,即等离子体。等离子体火炬可达6000~8000K的高温。过滤或消解处理过的样品经进样器中的雾化器被雾化并由氩载气带入等离子体火炬中,气化的样品分子在等离子体火炬的高温下被原子化、电离、激发。不同元素的原子在激发或电离时刻发射出特征光谱,所以等离子体发射光谱可用来定性样品中存在的元素。特征光谱的强弱与样品中原子浓度有关,与标溶液进行比较,即可定量测定样品中各元素的含量。
3.原子吸收分光度法
原子吸收分光光度法的测量对象是呈原子状态的金属元素和部分非金属元素,是由待测元素灯发出的特征谱线通过供试品经原子化产生的原子蒸气时,被蒸气中待测元素的基态原子所吸收,通过测定辐射光强度减弱的程度,求出供试品中待测元素的含量。
原子吸收一般遵循分光光度法的吸收定律,通常借比较对照品溶液和供试品溶液的吸光度,求得供试品中待测元素的含量。本方法适用于地表水和污水中Al、As、Ba、Be、Ca、Cd、Co、Cr、Cu、Fe、K、Mn、Na、Ni、Pb、Sr、Ti、V和Zn等20种元素总量的测定。(1)溶解态元素:未经酸化的样品中,能通过0.45um滤膜的元素成分。(2)元素总量:未经过滤的样品,经消解后测得的元素浓度。即样品中溶解态和悬浮态两部分元素浓度的总和。
三、实验原理
1 定性分析
采用K4[Fe(CN)6],鉴定Fe3+。
利用HCl沉淀Pb2+,根据PbCl2易溶于热水,在弱酸介质中,Pb2+与CrO42-反应生成黄色PbCrO4沉定来鉴定Pb2+,必要时加入NaOH溶液,将沉淀溶解,以确证Pb2+的存在。
利用NH3·H2O将Fe3+、Pb2+与Cu2+、Ni2+分离为:Fe(OH)3、Pb(OH)2 和Cu(NH3)42+、Ni(NH3)42+。滤液在弱酸(HAc)介质中,K4[Fe(CN)6]溶液与Cu2+生成红棕色沉淀鉴定Cu2+;在氨性介质中,Ni2+与丁二酮肟生成鲜红色丁二肟镍沉淀鉴定Ni2+。
2 定量分析
根据Fe3+与Pb2+、Cu2+和Ni2+的稳定常数的差别( ),采用控制酸度的方法,测定Fe3+。选用磺基水杨酸作为指示剂,指示终点为溶液由紫红色变成黄绿色。
),采用控制酸度的方法,测定Fe3+。选用磺基水杨酸作为指示剂,指示终点为溶液由紫红色变成黄绿色。
利用NH3·H2O将Fe3+、Pb2+与Cu2+、Ni2+分离为:Fe(OH)3、Pb(OH)2 和Cu(NH3)42+、Ni(NH3)42+。过滤后的Cu(NH3)42+、Ni(NH3)42+滤液用酸中和,Na2S2O3掩蔽Cu2+,采用返滴定法测定Ni2+,以二甲酚橙为指示剂,亮黄色变成酒红色为终点,再利用返滴定法测定Cu2+、Ni2+总量,其中铜的指示剂采用二甲酚橙,终点为溶液由红色变为黄绿色。滴定终点后,采用差减法,确定Cu2+的含量。
利用返滴定法测定Fe3+、Ni2+、Cu2+、Pb2+总量,采用差减法,确定 Pb2+ 的含量。
分步滴定判断所需数据
logKFe(III)Y=25.10,logKCuY=18.80,logKNiY=18.62,logKPbY=18.04。
Ksp[Fe(OH)3] =4.0×10-38,Ksp[Cu(OH)2] =2.2×10-20;
Ksp[Ni(OH)2] =2.0×10-15,Ksp[Pb(OH)2] =1.2×10-15。
四、试剂、材料和仪器
药品
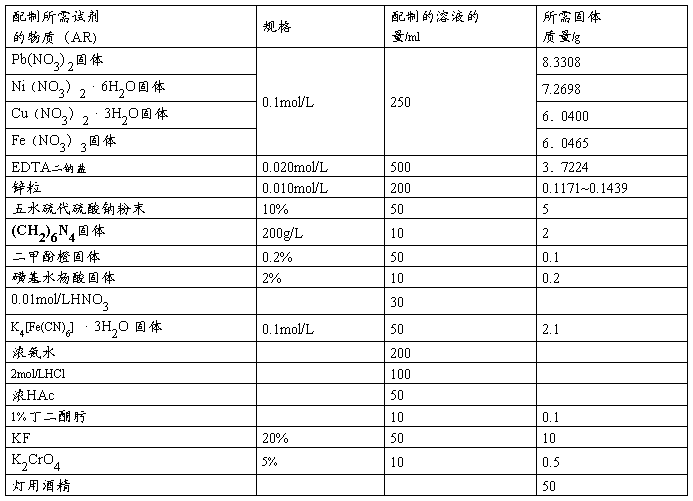
溶液的配制
0.01 mol·L-1Zn2+标准溶液的配制
用干净的小烧杯(或称量纸)准确称取0.1171~0.1439g配制200 mL 0.01mol·L-1 的锌溶液所需的纯锌粒于150 mL烧杯中,加入5 mL 6 mol·L-1的HCl 溶液,立即盖上表面皿,微热,待锌完全溶解后,以少量水冲洗表面皿和烧杯内壁,冷却后,定量转移至200.00 mL的容量瓶中,以水稀释至刻度,摇匀。计算其准确浓度。
0.01mol·L-1 EDTA标准溶液的配制及标定
用洁净的1000 mL容量瓶称取配制1000 mL 0.01 mol·L-1 EDTA溶液所需的EDTA二钠盐(Na2H2Y·2H2O)固体3.8g,在烧杯中加水、温热溶解、冷却后转移入试剂瓶中,摇匀。
吸取20.00 mL 0.01 mol·L-1 的Zn2+ 标准溶液于锥形瓶中。加入 2滴二甲酚橙指示剂,滴加200g/L六亚甲基四胺溶液至溶液呈现稳定的紫红色,再过量5 mL。用0.01 mol·L-1 EDTA溶液滴定至溶液由紫红色变为亮黄色即为终点。平行标定三份,计算EDTA溶液的准确浓度。数据记录和结果表达如表1所示。
约0.01mol·L-1 未知混合溶液的配制
称取配制各离子浓度约0.01mol·L-1 的固体于100ml小烧杯当中,用20ml去离子水溶解,转移至250.00ml的容量瓶中,洗涤烧杯,玻棒3~4次,将洗液移至容量瓶中,定容,摇匀。备用。
200g/L的六亚甲基四胺溶液的配制
称取所需的六亚甲基四胺固体,溶于小烧杯中,加入少量水溶解后,移至50.00ml容量瓶中,洗涤,移液,3~4次,最后,定容,摇匀,备用。
10%Na2S2O3 ,%的磺基水杨酸,0.2%的二甲酚橙溶液等配制操作如上。
除实验柜中以外仍需的仪器
五、实验内容和步骤
混合溶液中各离子的测定
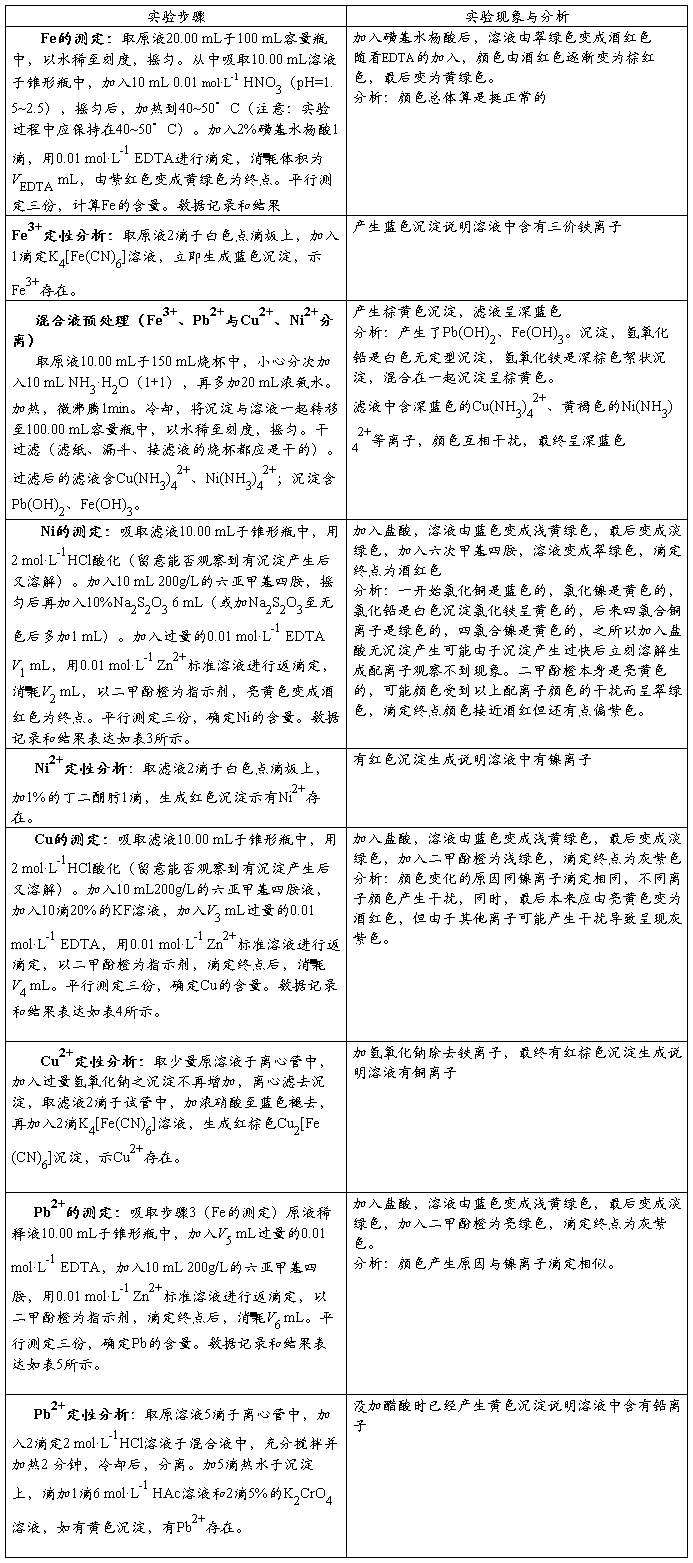
六、实验数据与结果
表1 0.01mol·L-1 EDTA溶液的标定
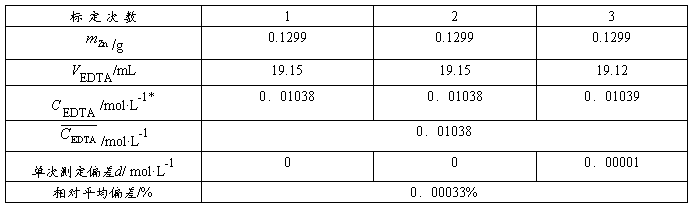
* mol·L-1
mol·L-1
表2 Fe含量的测定
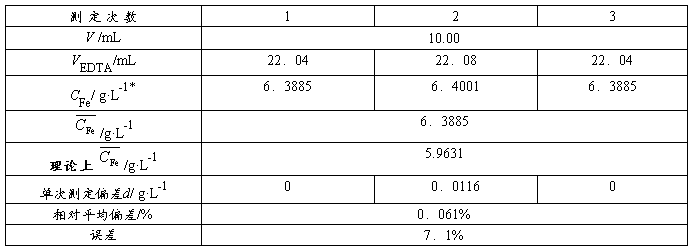
*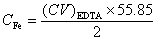 g·L-1,
g·L-1,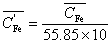 mol·L-1
mol·L-1
表3 Ni含量的测定
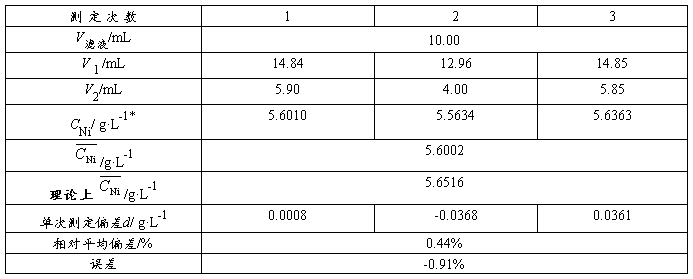
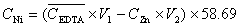 g·L-1,
g·L-1, mol·L-1
mol·L-1
表4 Cu含量的测定
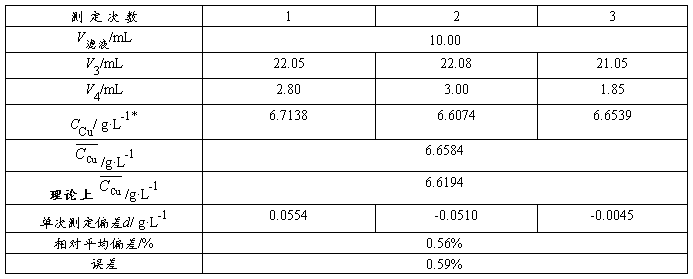
 g·L-1,
g·L-1, mol·L-1
mol·L-1
表5 Pb含量的测定
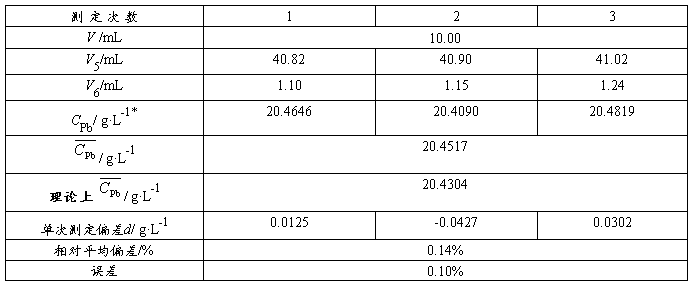
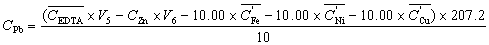 g·L-1
g·L-1
七、结果与讨论
通过处理比较滴定的数据,发现在铁含量的滴定与实验理论结果有较大偏差。可能原因:
1、铁与EDTA在PH=2时并不是严格按1:1反应,可能是1:2甚至是1:3反应。为了验证假设,配了含铁的纯溶液,在采用相同处理条件的情况下,用EDTA滴定时消耗的体积与铁几乎1:1.也就是说在PH=2的情况下,铁与EDTA也应是1:1.
2、在PH=2的情况下,混合样液中的其他离子会影响铁与EDTA的反应,即在滴定铁的同时可能会有部分其他离子被同时滴定。但是在查看林邦曲线时发现,lgKFe(III)Y=25.10,lgKCuY=18.80,lgKNiY=18.62,lgKPbY=18.04。?lgK(Fe-Cu)=6.30,只是略大于6.虽然?lgK≥6是在允许滴定终点误差为0.1%时准确滴定的条件。所以,应该配制3种分别含有铁和铜,铁和镍,铁和铅混合溶液,进行EDTA的滴定,验证是否其他离子会影响滴定结果的猜想。
3、可能原样在存放过程中可能因为是由于原液储存在玻璃瓶中置换出部分Al和Ca,从未影响了在后来滴定以及铁含量的测定。
.对于镍的定性检测,在加入丁二酮肟后,溶液并不是生成理论上丁二酮肟与镍的桃红色沉淀,而是红棕色的浑浊溶液。原因可能是丁二酮肟还会与Pb 生成沉淀,还可以跟Cu2+ 、Fe3+ 生成水溶性的络合物。这也可以解释为什么定性分析中出现的是红棕色的浑浊溶液而不是鲜红色的沉淀。
八、参考文献
[1] 第一届广东省大学生化学实验竞赛_实验操作试题
[2]华南师范大学,华中师范大学.分析化学.高等教育出版社.2011,4,第四版
[3]汤又文,分析化学实验,化学工业出版社,2008,2
[4]《 Pb2、Co2、CU2、Ni2混合液中Pb2的分离和测定》,新疆医科大学学,20##年,12,,24
[5]南京同普分析仪器制造有限公司,《铜合金中铜锌铅铁镍锰元素测定法》,2012,10,09
