7 附件1:
可疑医疗器械不良事件报告表
报告日期: 年 月 日 编 码:£ £ £ £ £ £ £ £ £ £ £


报告来源:£ 生产企业 £ 经营企业 £ 使用单位 单位名称:
联系地址: 邮 编: 联系电话:
报告人签名: 国家食品药品监督管理局制
附件2:
医疗器械不良事件补充报告表
报告时间: 年 月 日 编码:£ £ £ £ £ £ £ £ £ £ £
首次报告时间: 年 月 日

报告人: 省级监测技术机构接收日期: 国家监测技术机构接收日期:
生产企业(签章)
国家食品药品监督管理局制
附件3:
医疗器械不良事件年度汇总报告表
报告时间: 年 月 日 编码:£ £ £ £ £ £ £ £ £ £ £
汇总时间: 年 月 日至 年 月 日

报告人: 省级监测技术机构接收日期: 国家监测技术机构接收日期:
生产企业(签章)
国家食品药品监督管理局制
附件4:
市级监测机构年度考核评分表

注:评分表总分值为100分,满70分为合格。
附件5:
生产、经营企业MDR监测工作检查评分表
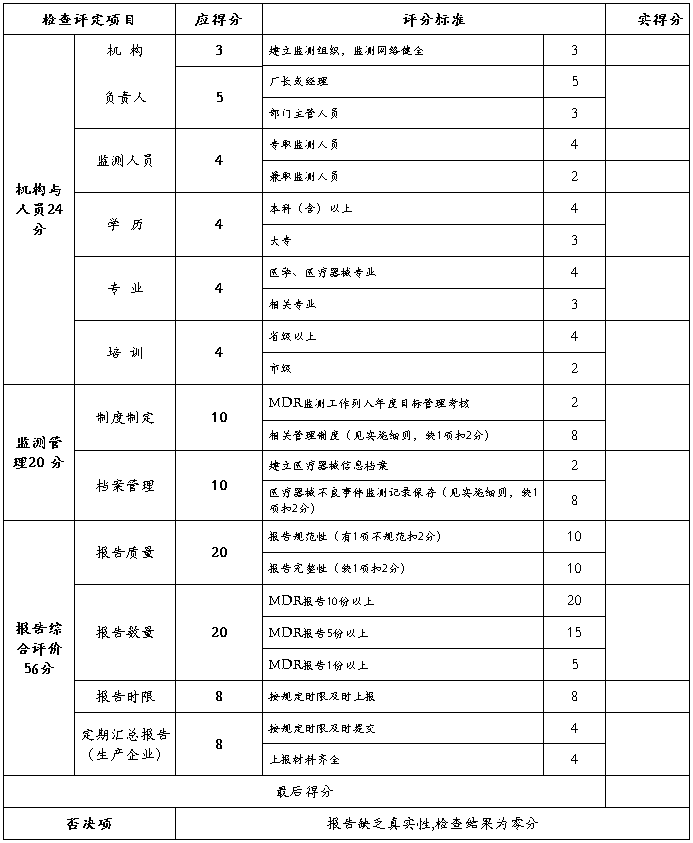
注:评分表总分值为100分,满70分为合格。
附件6:
使用单位MDR监测工作检查评分表

注:评分表总分值为100分,满70分为合格。
第二篇:医疗器械不良事件报告表
附表一:
国家食品药品监督管理局监制
医疗器械不良事件报告表
报告日期: 年 月 日
报告来源:? 生产企业 ? 经营企业 ? 使用单位 单位名称:
联系地址: 邮编: 联系电话: 编码:? ? ? ? ? ? ? ? ? ? ?

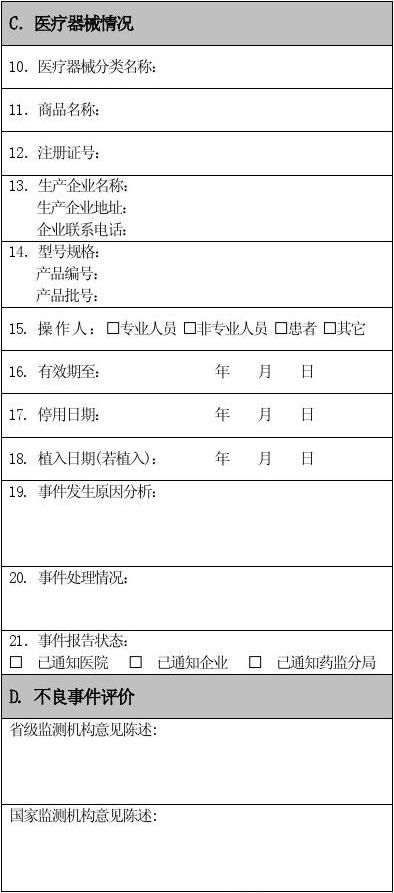
医疗器械不良事件报告表填写说明
一、 医疗器械不良事件定义:
获准上市的、合格的医疗器械在正常使用情况下,发生的或可能发生的任何与医疗器械预期使用效果无关的有害事件。
二、 报告范围:
需要医疗器械生产企业、经营企业、使用单位提供的可疑医疗器械不良事件报告是死亡和严重伤害报告。其中,严重伤害指①危及生命;②导致机体功能的永久性伤害或者机体结构的永久性损伤;③必须采取医疗措施才能避免上述永久性伤害或损伤。“永久性”是对身体结构或功能的不可逆的伤害,不包括小的伤害或损害。
三、 报告原则:
1、 基本原则:造成患者、使用者或其他人员死亡、严重伤害的事件已经发生,并且可能与所使用医疗器械有关,需要按可疑医疗器械不良事件报告。
2、 濒临事件原则:
有些事件当时并未造成人员伤害,但临床医务人员根据自己的临床经验认为再次发生同类事件时会造成患者或医务人员死亡或严重伤害,则也需要报告。
3、 可疑即报原则:
在不清楚是否属于医疗器械不良事件时,按可疑医疗器械不良事件报告。这些事件可以是与使用医疗器械有关的,也可以是不能除外与医疗器械有关的事件。
四、 免除报告规则:
1、 使用者在应用前能够发现医疗器械有缺陷;
2、 完全是患者因素导致了不良事件发生;
3、 事件发生仅仅是因为器械超过有效期限;
4、 事件发生时,医疗器械预先设计的安全保护措施正常工作,并不会对患者造成伤害。
注意事项:1、请务必填写清楚您的联系方式、产品名称和生产企业名称
2、进口产品在生产企业联系方式一栏请填写境内代理企业联系方式
3、如有问题请与国家药品不良反应监测中心联系
联系地址:北京市崇文区法华南里11号二层 100061
联系电话:010-67164989 010-67102266-805
e-mail: mdae@
国家药品不良反应监测中心
