7 附件1:
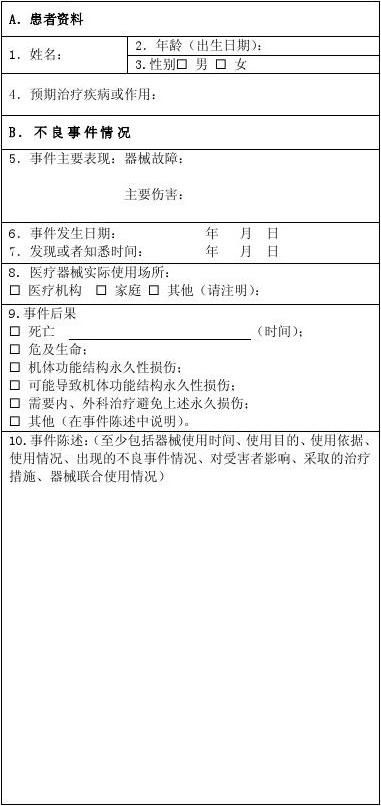
可疑医疗器械不良事件报告表
报告日期: 年 月 日 编 码:£ £ £ £ £ £ £ £ £ £ £
报告来源:£ 生产企业 £ 经营企业 £ 使用单位 单位名称:
联系地址: 邮 编: 联系电话:
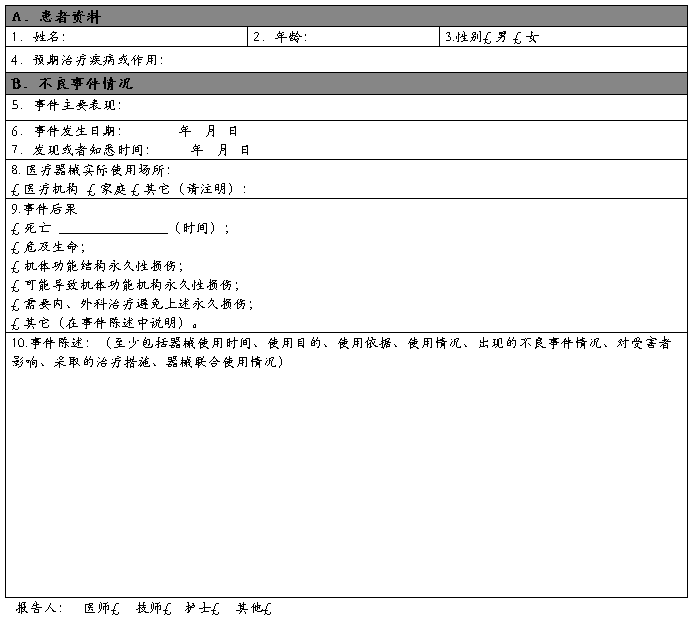

报告人签名: 国家食品药品监督管理局制
附件2:
医疗器械不良事件补充报告表
报告时间: 年 月 日 编码:£ £ £ £ £ £ £ £ £ £ £
首次报告时间: 年 月 日

报告人: 省级监测技术机构接收日期: 国家监测技术机构接收日期:
生产企业(签章)
国家食品药品监督管理局制
附件3:
医疗器械不良事件年度汇总报告表
报告时间: 年 月 日 编码:£ £ £ £ £ £ £ £ £ £ £
汇总时间: 年 月 日至 年 月 日

报告人: 省级监测技术机构接收日期: 国家监测技术机构接收日期:
生产企业(签章)
国家食品药品监督管理局制
附件4:
市级监测机构年度考核评分表
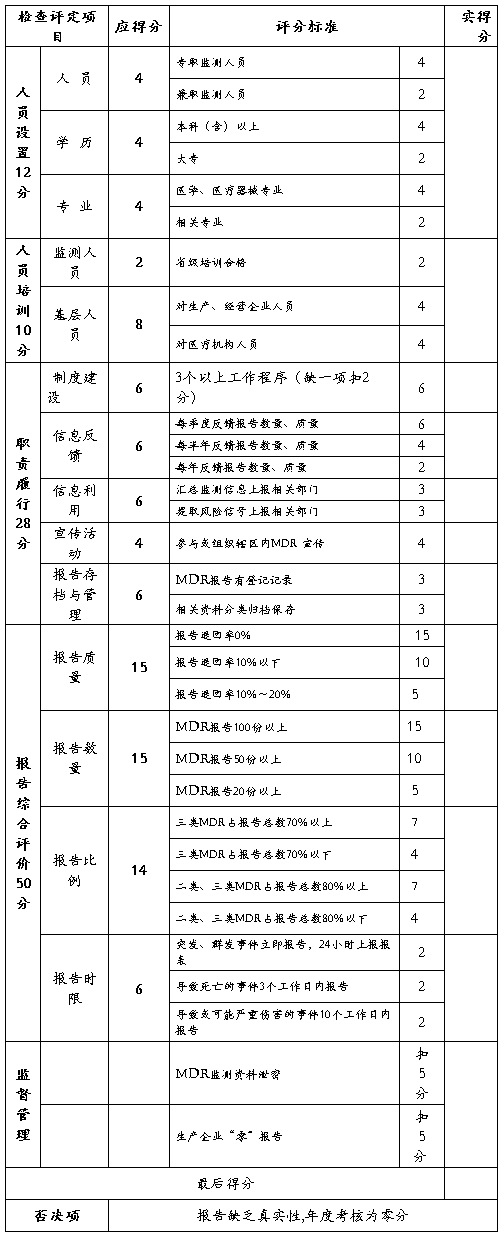
注:评分表总分值为100分,满70分为合格。
附件5:
生产、经营企业MDR监测工作检查评分表

注:评分表总分值为100分,满70分为合格。
附件6:
使用单位MDR监测工作检查评分表
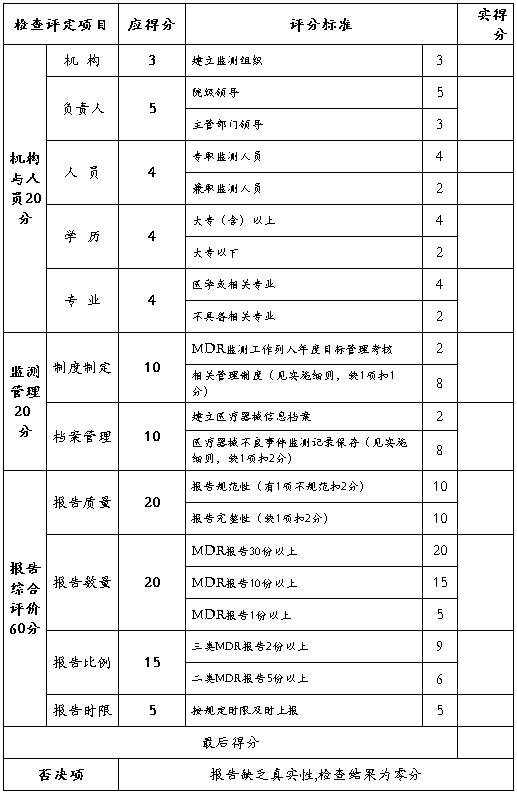
注:评分表总分值为100分,满70分为合格。
第二篇:20xx可疑医疗器械不良事件报告表
可疑医疗器械不良事件报告表
报告日期: 年 月 日
报告来源:? 生产企业 ? 经营企业 ? 使用单位 单位名称:
联系地址: 邮 编: 联系电话:
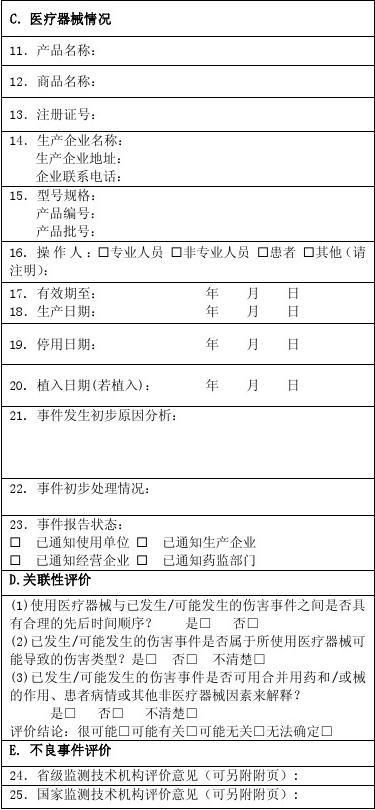
报告人签名:
