分子遗传学基础综合性实验报告
10农生一班第一组 卢** 胥** 闫**
摘要
抽取水稻叶片总DNA,利用PCR仪扩增使其总量增加,在利用琼脂糖凝胶电泳分离DNA的原理和方法,检测DNA的纯度与分子量,同时通过对电泳带型分析判断水稻样品是属于粳稻或籼稻。
关键词 DNA PCR 琼脂糖凝胶电泳
引言
DNA 分子标记技术的研究始于1980 年, 本质上是指能反映生物个体或种群间基因组中某种差异的特异性DNA 片段, DNA 分子标记大多以电泳谱带的形式表现生物个体之间DNA 差异, 通常也称为DNA 的指纹图谱。DNA 分子标记具有的优越性有: 大多数分子标记为共显性, 对隐性的农艺性状的选择十分便利; 基因组变异极其丰富, 分子标记的数量几乎是无限的; 在生物发育的不同阶段, 不同组织的DNA 都可用于标记分析; 分子标记揭示来自DNA 的变异; 表现为中性, 不影响目标性状的表达, 与不良性状无连锁; 检测手段简单、迅速。DNA 分子标记以其显著的优点广泛应用于动植物遗传育种、基因组作图、基因定位、物种亲缘关系鉴别、基因库构建、基因克隆等诸多方面。
DNA微量抽取:先用机械的方法使组织和细胞破碎,然后加入十二烷基磺酸钠(SDS)等离子型表面活性剂,溶解细胞膜和核膜蛋白,使细胞膜和核膜破裂。再加入酚和氯仿等表面活性剂,使蛋白变性。最后加入无水乙醇沉淀DNA;沉淀的DNA,即为植物总DNA,溶于TE溶液中保存备用。
多聚酶链式反应:多聚酶链式反应是在模板DNA、引物和4种脱氧核苷酸存在的条件下依赖于DNA聚合酶的体外酶促合成反应。由高温变性,低温退火和适温延伸三步反应组成一个循环,通过多次循环反应,使目的DNA得以迅速扩增。
1. 变性:加热使模板DNA在高温下(94-95℃)变性,双链间的氢键断裂而形成两条单链,即变性阶段。
2. 退火:在体系温度降至37-65℃,模板DNA与引物按碱基配对原则互补结合,使引物与模板链3’端结合,形成部分双链DNA,即退火阶段。
3. 延伸:体系反应温度升至中温72℃,耐热DNA聚合酶以单链DNA为模板,在引物的引导下,利用反应混合物中的4种脱氧核苷三磷酸(dNTP),按5’到3’方向复制出互补DNA,即引物的延伸阶段。
琼脂糖凝胶电泳:琼脂糖是一种天然聚合长链状分子,沸水中溶解,45℃开始形成多孔性刚性滤孔,凝胶孔径的大小决定于琼脂糖的浓度。DNA分子在碱性条件下带负电荷,在外加电场作用下向正极泳动。DNA分子在琼脂糖凝胶中泳动时,有电荷效应与分子筛效应。不同的DNA,其分子量大小及构型不同,电泳时的泳动率就不同,从而分出不同的区带。
1 材料及方法
1.1实验材料、器具及试剂
水稻幼叶【21号、22号、27号、28号、223号、224号、249号、台中65号、IR64、9311(籼稻)、日本晴(粳稻)】
高速台式离心机,振荡器,水浴箱,1.5ml离心管架,玻璃滴管,移液器,研钵,1.5ml离心管,2ml离心管,枪头,烧杯,量筒等。无水乙醇,氯仿,异戊醇,TE缓冲液(pH8.0),抽提液(200mM Tris-HCl, PH7.5; 250mM NaCl; 25mM EDTA; 0.5%SDS)
PCR仪,2ml离心管架,移液枪,1. 5ml离心管,0.2ml离心管, dNTP,Taq酶,引物一对(RM1 F,RM1 R),10×PCR反应缓冲液,灭菌双蒸水。
电泳仪,电泳槽,电子天平,移液器,枪头,点样板,微波炉。 琼脂糖,TBE电泳缓冲液,GoldenView,载样缓冲液
1.2实验步骤
DNA提取:
① 取幼叶0.1g左右放于研钵中,加入液氮,将叶片磨成粉状,倒入1.5ml离心管中。
②约用400μl抽提液洗涤研钵,也倒入离心管,混匀。 置于65℃水浴中30分钟。
③ 加入800ul氯仿,振荡,充分混匀。
④12000rpm离心15分钟。取上清液于1.5ml离心管。
⑤加入等体积预冷的无水乙醇,轻轻混匀,静置直到DNA析出。
⑥12000rpm离心5分钟,去上清液。加入70%乙醇漂洗。适当风干,溶于100-200μl TE溶液中待用。
PCR扩增DNA:
①PCR反应混合液的制备(n为样品数)
n× 0.4μl dNTP
n×2.0μl 10× PCR buffer(含15mM MgCl2)
n×0.2μl 引物F
n×0.2μl 引物R
n×0.2μl Taq酶
n×16μl ddH2O 混匀
②吸取19ul混合液与PCR管中,加入1ulDNA样品,盖好盖子,混匀,立即置于PCR仪上进行扩增。
③结束反应,PCR产物放置于4℃冰箱中待电泳。
琼脂糖凝胶电泳:
①称取0.8g琼脂糖加入盛有100ml 1×TBE电泳缓冲液的500 ml三角瓶中,摇匀。在微波炉上加热至琼脂糖完全溶解,冷却到60℃,加入10μl的GoldenView,并摇匀。
②用胶带将制胶板两端封好,插入适当梳子,将溶解的琼脂糖(约50℃)倒入,室温冷却凝固。
③充分凝固后撕掉两端的胶布,将凝胶置入电泳槽中,加1×TBE电泳缓冲液至液面覆盖凝胶1-2mm,小心垂直向上拔出梳子,以保证点样孔完好。
④用移液器吸取上次实验抽提的水稻总DNA 4μl样品于点样板小孔中,再加入5μl 1×TBE电泳缓冲液及1μl 的载样缓冲液,混匀后,小心加入点样孔,蓝色样品混合物将沉入点样孔下部。同时点10μl λDNA(HindIII酶切,30ng/ul)作为分子量标准。
⑤打开电源开关,调节电压至3-5V/cm,可见到溴酚蓝条带由负极向正极移动,约20分钟后即可观察。
⑥将凝胶置于紫外透射检测仪上,戴上防护观察罩,打开紫外灯,可见到白色条带。根据条带粗细和荧光强度,可粗略估计该样品DNA的浓度。同时根据已知分子量的标准DNA,通过线性DNA条带的相对位置初步估计样品的分子量,并确定是粳稻或籼稻。
2 实验结果与分析
2.1.水稻总DNA带型:
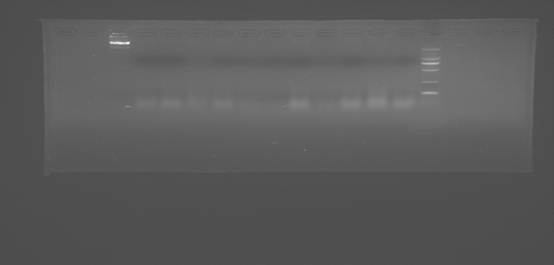
分析:
从水稻总DNA的带中看出,有部分DNA已经降解,因为当时提取DNA时没有及时进行处理,而是在冰箱中保存,一周后才进行电泳。DNA在溶液中,尤其是水的稀溶液中,会发生自然的降解作用。降解作用速率和温度关系不大,但是反复的冻融会加速DNA的断裂和降解。还有是可能因为在提取DNA是污染了DNA样品,导致DNA加速降解。
还有将样品DNA与Marker DNA作比较,可以发现样品DNA分子量较小
2.2.水稻各个样品的带型:
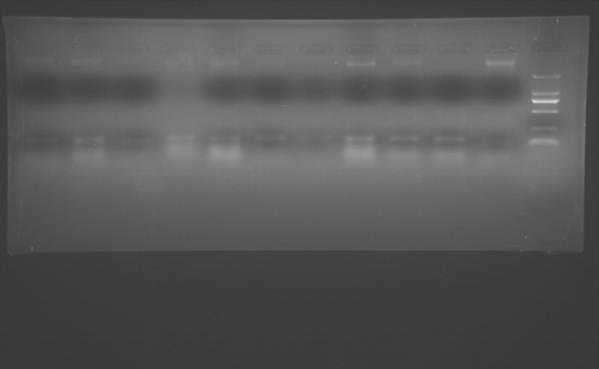
分析:
从上图可以看出有不同带型,其中的序号对应的水稻样品如下:

已知9311为籼稻品种,日本晴为粳稻品种,则可以粗略判断21号、223号、224号为籼稻品种;28号、27号、249号、22号、台中65为粳稻品种;而IR64的带型介于9311与日本晴之间,无法判定。
3 讨论
通过对水稻的总DNA进行琼脂糖凝胶电泳可知,DNA容易降解,不宜久放,即使是在冰箱里面,故DNA适于当天提取当天进行PCR扩增。在对PCR 的产物进行琼脂糖凝胶电泳时,对得到的带进行分析,可以得到如下结果:21号、223号、224号为籼稻品种;28号、27号、249号、22号、台中65为粳稻品种;而IR64的带型介于9311与日本晴之间,无法判定。
参考文献
【1】 普通遗传学综合性实验 /刘向东,李亚娟主编.中国农业出版社,2011.7,第四章
【2】 遗传学综合实验/主编李雅轩, 赵昕,北京:科学出版社,2006
第二篇:实验七 DNA指纹的遗传分析
实验七 DNA指纹的遗传分析
【实验原理】
u “DNA指纹”是指利用DNA差异来进行与传统指纹分析相似的身份识别。DNA指纹是以DNA的多态性为基础,而卫星DNA的发现则是其最重要的奠基石。
u 卫星DNA是由一短序列(即重复单位或核心序列)多次重复而成,因此也有人称其为可变数目串联重复序列(variable numbers of tandem reprat,VNTR),在人类基因组中存在多种由不同重复单位组成的卫星DNA,重复单位的碱基序列在不同个体中具有高度的保守性,而卫星DNA的多态性则来源于重复单位的重复次数不同,并形成了众多的等位基因。例如,人类1号染色体上的VNTR D1S80,核心序列由16个核苷酸组成,拷贝数在14~41个之间,已知有29种不同的等位基因。
DNA指纹图谱的基本特点:
u 多位点性:基因组中某些位点的小卫星重复单位含有相同或相似的核心序列。在一定的杂交条件下,一个小卫星探针可以同时与十几个甚至几十个小卫星位点上的等位基因杂交。
u 高变异性:DNA指纹图谱反应的是多个位点上的等位基因的特征,具有很高的变异性。发现两个无血缘关系个体具有相同DNA指纹图谱的概率仅为5×10-19,因此,除了同卵双胞胎,几乎不可能有两个人的DNA指纹图谱完全相同。
u 稳定的遗传性:DNA指纹图谱中的谱带能够稳定遗传,杂合带遵守孟德尔遗传规律。子代DNA指纹图谱中产生与双亲都不同的新带的概率(基因突变)仅在0.001~0.004之间。DNA指纹图谱还具有体细胞稳定性,即用同一个体的不同组织如血液、肌肉、毛发、精液等的DNA作出的DNA指纹图谱是一致的。
【材料】
人类口腔细胞。
【仪器与试剂】
1. 仪器
微量移液器,小型离心机,恒温水浴锅,漩涡振荡器,PCR仪,电泳仪,电泳槽,透射式紫外分析仪(或凝胶成像仪)。
枪头,1.5mL,0.2 mL离心管,棉签,使用前均需121℃高温灭菌
2.试剂
NaCl,琼脂糖,溴化乙锭,Na2-EDTA,SDS,Tris,Proteinase K,冰醋酸,溴酚蓝,二甲苯腈蓝,蔗糖,甘油,DNA相对分子质量标记,Chelex 100树脂(Bio-Rad),PCR pre-mix。
3.溶液配制
(1)5% Chelex树脂
Chelex 100(Bio-Rad) 0.5g
50mmol/L Tris-HCl 10mL
用4mol/L NaOH调pH至11,室温可保存3个月,使用前充分混匀。
(2)2.0%琼脂糖凝胶
称2.0g琼脂糖放入250ml三角烧瓶,加 入1×TAE溶液100mL微波炉加热溶解,冷却至60℃左右加入1μg/mL溴化乙锭(EB),缓慢混匀后倒胶板。
(3)溴化乙锭(EB)
用无菌水配制5mg/mL储藏液,工作浓度1μg/mL。
注意;溴化乙锭为诱变剂,有致癌作用。配制、稀释和染色时必须戴手套。
(4)0.5mol/L EDTA(pH8.0)
Na2-EDTA 18.61g
NaOH 2g
蒸馏水定容至100mL,室温保存。
(5)10×TAE电泳缓冲液
Tris 48.4g
冰醋酸 11.42mL
0.5mol/L EDTA(pH8.0) 20mL
蒸馏水定容至1000mL,室温保存。
(6)10%SDS
SDS 10g用无菌水溶解后(可加热),定容至100mL,室温保存。
(7)蛋白酶K溶液
20mg/mL蛋白酶K水溶液 5mL
10%SDS 1mL
无菌水 94mL
冰箱冷藏。
(8)无菌水:蒸馏水或去离子水,高温灭菌。
(9)1mol/L Tris-HCl(pH8.0)
将12.1g Tris溶解在80mL蒸馏水中,加盐酸调节pH至8.0,加蒸馏水定容至100mL。
4.引物
Primer1:5’-GAAACTGGCCTCCAAACACTGCCCGCCG-3’
Primer2:5’-GTCTTGTTGGAGATGCACGTGCCCCTTGC-3’
【实验步骤】
1.收集DNA样本
(1)先漱口,然后用灭菌的牙签充分擦刮口腔内壁,将该牙签放入 1.5mL装有1mL无菌水的小离心管中,使粘附在牙签表面的口腔细胞悬浮其中(以能看到悬浮物为好)。震荡10s,10000 r/min离心1min。
(2)从离心管中吸出970μL无菌水,注意不要吸到沉淀。
(3)向离心管中加入200μL 5% Chelex 100,震荡10s混匀。
(4)加入2μL蛋白酶K,混匀,56℃保温5min。
(5)剧烈震荡10s,沸水浴8min。
(6)10000r/min离心3min,离心管中溶液分成上下两层:下层为Chelex100和细胞碎片的沉淀,上层溶液含DNA分子,可以直接用作PCR模板。
此DNA样本可在4℃或-20℃保存,必要时可在使用前再次加热并离心,使管内物质分层。
2.PCR扩增D1S80等位基因
(1)每个人用记号笔在0.2mL PCR管上做好标记。
(2)准备冰盒,开始反应前尽量使PCR管保持在冰上。
(3)依次加入下列成分,配制25μL体系的PCR反应溶液:
PCR pre-mix 12.5μL
引物1 1μL
引物2 1μL
口腔细胞DNA样本 10μL
加无菌水至总体积25uL。
(4)轻弹管壁,混匀溶液。
(5)离心10s,使管壁上的液滴落下。
(6)按下列程序开始PCR反应:
94℃,1min
$
94℃,15s
68℃,15s
72℃,15 s
30个循环
$
72℃,10min
$
4℃暂时放置,直至开始电泳
3.PCR扩增产物鉴定与D1S80等位基因分析
(1)用1×TAE电泳缓冲液配制2.0%琼脂糖电泳凝胶。
(2)60V预电泳1~2min。
(3)在凝胶上选一孔加入6µL的DNA相对分子质量标记(DNA100bp Ladder)。
(4)每位同学将各自的20µLD1S80 PCR扩增产物加入指定凝胶样孔,注意不要有气泡进入。
(5)60V电泳40min-50min。
(6)取出凝胶用清水漂洗。
(7)用紫外分析仪观察凝胶,记录每个个体的DNA条带数目及其位置。
【结果与分析】
本次实验所选择的方法是D1S80指纹图谱分析的常用方法。人群中D1S80座位的杂合率约为86%。从理论上讲,可能存在435种不同的等位基因组合。利用D1S80座位两侧序列设计的引物(Kasai et al,1990),通过PCR反应,很容易确定特定个体的D1S80等位基因构成,纯合体只有一条DNA带,而杂合体有两条不同的DNA带。
1. 将小组的电泳结果拍照,并把照片贴在实验报告上,对照片进行必要的说明,例如,相对分子质量的标记各片段的大小(bp)。
(见附图)
2. 根据电泳结果,填写D1S80等位基因分析结果(表7-1):
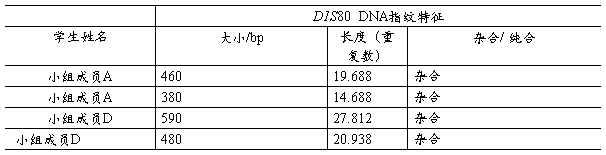
表7-1 结果记录表
注:因为重复数为l的DIS80 PCR 产物长161bp,所以,重复数每增加一个,序列增加长度16 bp。据此可以催算:
重复数=1+(PCR产物大小-161)/16
3.在班级中调查有无同学D1S80指纹图谱完全相同或部分相同。自行查找有关人群中D1S80各等位基因频率的资料,计算两个没有亲缘关系的个体,其D1S80指纹图谱完全相同或部分相同的概率。
从各小组的电泳紫外图谱看,有一些同学的DNA指纹图谱看起来有些相似,但鉴于本次实验误差大,难以确定其指纹图谱是相同的。理论上可能存在435种不同的等位基因组合。那么D1S80指纹图谱完全相同的概率应为1/(435*435)=1/189221.
【讨论】
从图电泳图可以看出,只有A、D两小组成员的条带清晰明显。小组成员E的PCR产物聚集在加样孔中没有迁移,可能是因为其产物不存导致的;其他成员均没有条带或很浅,可能是由于收集的DNA样本过少,未能PCR出足够的扩增产物。
【思考题】
用PCR、RFLP、RAPD方法产生DNA指纹图谱各有哪些利弊?
答:RFLP分析对样品纯度要求较高,样品用量大,步骤繁琐、工作量大、成本较高;RADP图谱中某些弱带重复性较差,而且目前该法在引物长度和序列及应用的引物数目、扩增反应条件等实验技术方面未标准化,影响了不同条件下结果的可比性;
