昆明理工大学医学院 医学遗传学实验报告册
姓名:班级: 学号:
遗传学教研室
实验报告一
一、实验原理:
无精子因子(azoospermiafactor,AZF)是在19xx年发现的已经被确认为精子发生所必须的。AZF基因位于Y染色体(Yq11)上,并在睾丸内特异性表达。探讨Y染色体上无精子因子(AZF)微缺失与男性不育的关系。应用多重PCR技术,检测AZF片段缺失。
二、实验材料:
1、病人全血标本样品。
2、上下游引物一对。
3、PCR反应体系(酶、buffer、DNTP等。)。
4、琼脂糖、TAE溶液、EB、DNAloaldingbuffer。
5、琼脂糖电泳仪(套),凝胶成像系统。
6、PCR仪。
三、实验方法:
1、制备PCR反应体系。
2、将引物和模板分别加入反应体系中。
3、设置PCR反应程序、将反应体系放入PCR仪中。
4、制备琼脂糖凝胶。
5、将反应完毕的PCR体系取出适量,与loalding buffer混合加入到琼脂糖当中。
6、设置电泳条件及时间,结束后用凝胶成像系统观察结果。
四、实验结果:
五、思考题:
1、根据实验结果,检测自己的实验结果是阳性还是阴性? 2、实验的检测结果说明了什么?
实验报告二
一、 实验原理:
人类外周血细胞本来是终末分化细胞,一般没有分裂能力,但经PHA(植物血球凝集素)或ConA等药物刺激后,转变成可分裂的转化细胞。向培养物中加入适量的秋水仙素,使纺锤体微管解聚,这样细胞停留在中期,可以获得大量的分裂细胞。用低渗盐溶液(一般是0.075mol/L的KCl)处理,使其中的红细胞及分裂相细胞膜和一部分细胞质除去,最后以气干法制片,可获得较好的染色体标本。
二、实验材料:
(1)2ml注射器、培养瓶、离心管、吸管、量筒、载玻片。
(2)超净工作台,恒温培养箱,天平,离心机、显微镜等。
(3)试剂:
① 培养基的配制:(RPMI 1640培养基 4ml+小牛血清 1ml+双抗各100IU/ml+PHA 0.2ml)以5% NaHCO3调pH至7.2~7.4, 4℃备用。 ② 肝素:称取0.2g溶于100ml双蒸水中,浓度为0.2%,灭菌。 ③ 秋水仙素:生理盐水配制成20μg/ml浓度,灭菌,分装,置-20℃。
④ 低渗液:0.075mol/L KCl。
⑤ 固定液: 甲醇∶冰乙酸(3∶1),临时配制。
⑥ Giemsa工作液:1份原液和9份磷酸缓冲液,临时配制。 ⑦ 磷酸缓冲液:1/15mol/L Na2HPO4、1/15mol/L KH2PO4等体积
混合。
⑧ 5% NaHCO3灭菌滤器抽滤备用。
三、实验方法:
1、外周血接种:取新鲜血液样本0.5-0.8ml,加入到配置好的1640培养基中。利用PHA刺激细胞增殖,培养72-96H。
2、在收取细胞前加入秋水仙素(10ug/ml)10ul终止细胞分离,继续培养细胞2小时。
3、将处理好的细胞标注清楚,放入离心机中,1600转离心7分钟。
4、弃上清,加入已预热额kcl低渗溶液8ml,充分混匀,使细胞与低渗液充分接触,静置30分钟后1600转离心7分钟。
5、弃上清,加入新配置的固定液1.5—2ml,充分混匀,静置30分钟后1600转离心7分钟。
6、弃上清,再次加入固定液8ml,充分混匀,静置30分钟后1600转离心7分钟。
7、弃上清,再次加入固定液6ml,充分混匀,静置30分钟后1600转离心7分钟。
8、弃上清、加入1-2ml固定液,制成悬液。
9、取悬液,滴在载玻片上,用酒精灯短暂烧烤。
10、将制好的标本放入烘箱中老化。
四、实验结果:
五、思考题:
1、染色体提取过程中要注意哪些事项?
2、染色制备过程中哪些步骤最重要?
实验报告三
一、实验原理:
人们用物理、化学因素处理后,再用染料对染色体进行分化染色,使每条染色体上出现明暗相间,或深浅不同带纹的技术称为显带技术(banding technique)。染色带的数目、部位、宽窄和着色深浅均具有相对稳定性,所以每一条染色体都有固定的分带模式,即称带型。染色体带型是鉴别染色体的重要依据。
二、 实验材料:
1、染色体标本(实验二中制备完毕)。
2、Giemsa工作液:1份原液和9份磷酸缓冲液,临时配制。
3、 磷酸缓冲液:1/15mol/L Na2HPO4、1/15mol/L KH2PO4等体积混合。
4、 5% NaHCO3灭菌滤器抽滤备用。
5、吉姆萨染色液。
7、胰酶消化液。
三、实验方法:
1、将制备好的染色体标本放入Na2HPO4+ KH2PO4+胰酶消化液的混合液中2分钟。
2、取出染色体标本,放入Na2HPO4+ KH2PO4+吉姆萨的混合液体中染色。
3、待染色体标本晾干以后,上镜观察。
四、实验结果:
五、思考题:
1、制备出良好的G带染色体标本需要注意哪些事项?
2、染色体显带有何意义?
第二篇:动物遗传学实验报告
动物遗传学实验报告 环境对果蝇生长发育的影响
实验小组成员:刘楠辛(20083770) 李洪建 (20081420) 廖成成(20081378) 段婷 (20080871)
张伯睿(20081424) 李大锐(20070822)
目录
综述................................................2
实验所需器材及药品....................2
实验基本操作................................2
实验一.温度的影响....................3
实验二.光照的影响........................4
实验三.酒精的影响........................5
- 1 -
综述:我组的综合性实验题目是研究环境对果蝇生长发育的影响。经过讨论,我组成员得出结论:气温、湿度、空气、光照、噪声等环境要素均可能对果蝇的生长发育造成影响。另一方面,果蝇的饲喂环境及营养水平也可能会影响其生长发育。
所以我们选择了温度、光照因素从环境要素方面进行研究;选择在饲料中添加酒精从营养水平方面进行研究;选择孤独实验从思维环境方面进行研究
实验器材及药品
1.实验动物:野生型果蝇(红眼长翅)残翅果蝇
2.实验器材:果蝇培养瓶,麻醉瓶,生化培养箱,温度箱,光照箱
镊子,100ml小烧杯,小烧杯,100ml量筒,称量天平, 药品匙 ,毛笔,酒精灯,铁架台,铁丝网等。
3.实验药品:乙醚,医用白酒,经柠檬天然发酵产生的有浓郁酒精气 味的液体,玉米粉,琼脂,葡萄糖,酵母膏,水等
实验基本操作
1.培养基的配置:
果蝇以酵母菌为食,常采用发酵的培养基繁殖酵母菌来饲养果蝇
先将果蝇培养瓶,棉塞高温灭菌20分钟,灭菌期间可用来配置培养基。最常用培养基为玉米粉培养基:100ml水,琼脂1.5g,葡萄糖10g,玉米粉14g,酵母膏适量。按顺序加入
配置时,取70ml水煮琼脂,30ml的水溶化玉米粉和葡萄糖(防止加入时块集)。琼脂煮化后加入玉米粉与葡萄糖,熬煮过程中应不断搅拌,有香味溢出即为煮熟。待培养基冷却至不烫手时加入酵母膏搅拌。随后将煮好的培养基用玻璃棒引流分装进培养瓶中。待培养瓶冷却后,用酒精棉球将瓶壁上的水汽擦干净,塞上经消毒处理的棉塞。
2.果蝇接种
- 2 -
①麻醉:取一培养瓶作为麻醉瓶,迅速将麻醉瓶与装有果蝇的培养瓶相对,用手捂住培养瓶,利用果蝇趋光性,促使果蝇飞向麻醉瓶中。再由两人配合,快速将滴有乙醚的棉塞塞在麻醉品上,培养瓶棉塞塞回培养瓶。待果蝇麻醉后倒出。注意麻醉时间不得过长,否则导致果蝇致死,经本组成员研究,大约在一分钟左右为宜。
②接种:将被麻醉的果蝇区分雌雄,按要求分装入各培养瓶,塞上棉塞,放入不同培养箱设定不同环境进行观察
实验一.温度对果蝇生长发育的影响
一.实验目的及原理
果蝇一个生活周期所需时间因饲养温度和营养条件而异。
对于非常温度(较高温度或较低温度),变温动物会在不同的方面表现出自己的适应性反应,如改变表型大小、增加或减弱外表的颜色、升高或降低自身的代谢率、增强或减小生育率、提高竞争力等等。
温度对果蝇表型的影响主要表现在果蝇的翅长和身体大小方面,而果蝇的翅长就是描述其身体大小的一个很重要的指标,翅长的大小在一定程度上就能够代表果蝇身体的大小。
目的:希望通过实验观察到温度对残翅果蝇翅长性状的影响
二.实验的方法及步骤
选取残翅果蝇作为研究对象,以雌雄2:1的比例在每只培养瓶中加入9只果蝇,两瓶放入温度箱中作为观察组,一瓶放入生化培养箱中作为对照组。温度箱中的温度控制在36.5~34.5℃。
三.实验结果
由于温度较高,培养基干燥,温度培养箱中的果蝇死亡。实验失败。
四.实验结果分析及经验总结
第一次实验时,我们将温度定在36.5℃.在接种果蝇后,培养基很快干燥,于是我们采取了补水措施:在培养基表面直接洒水及在培养基中间挖一个凹槽注水,但培养基依然干燥,导致果蝇死亡
在进行第二次实验时我们先将温度降至34.5℃,并在熬煮培养基时多添加了20ml的水,仍按原比例数量接种果蝇,并在实验过程中人工洒水,接种果蝇仍然死亡
在试验过程中,我们观察到温度箱中的培养基表面往往迅速长出一层很薄的白色菌体,经判断为酵母菌,说明酵母菌在高温下生长快。由此可以猜测,高温下果蝇生长周期减短可能是因为酵母菌数量增多,而果蝇正好是以酵母菌为食的。
- 3 -
经小组讨论,该实验技术重点在于控制培养基水分与温度的平衡,如何在高温下保证培养基的湿润是关键,温度对果蝇的生长发育固然重要,水分更为重要(尤其在高温环境下)
在今后设计温度试验中,我们会注意以上因素,并提高实验组果蝇数量,对果蝇子一代,子二代,子三代等进行连续研究
同时我还有一个设想就是可将高温培养出的子代果蝇一部分转正常温度环境下进行繁殖,观察其后代的性状又怎样变化
实验二. 光照对果蝇生长发育的影响
一. 实验目的及原理
任何生物都有一定的生活节律性,即有各自特定的生物钟
我们希望通过光照试验观察不同的作息规律会对果蝇造成怎样的影响,以及长时间的光照是否会造成果蝇某些性状的突变
在实验中,可将果蝇的活动情况分为强活动(飞行和爬行),弱活动(梳理觅食等原地发生的运动),静息(身体不发生运动的活动)。以便于观察后进行相应描述。
二. 实验方法及步骤
分别选取残翅果蝇及野生型果蝇,以雌雄2:1的比例在每只培养瓶中加入9只果蝇,两瓶放入光照箱中作为观察组,一瓶放入生化培养箱中作为对照组。调整光照至40%,持续光照,控制与生化培养箱中相同的温度24.5℃。对果蝇的活动行为进行连续观察。以及对果蝇后代数量进行统计。
三. 实验现象及结果
果蝇放入光照箱中第1~2天,活动相较与对照组的果蝇更加活跃,大多数时间属强活动行为,弱活动行为少,几乎无静息行为。情绪焦躁。
第3天,果蝇强活动行为时间减少,弱活动行为增加,静息活动增加。果蝇逐渐失去活力
此后几天果蝇活动力呈不断衰减趋势
一周后已基本处于弱活动和静息状态。
观察果蝇后代蛹的数量,可以看到果蝇后代数量明显减少,光照组各瓶中蛹数均不超过20只,但并未发生性状方面的变化
该实验说明,长时间的光照会导致果蝇繁殖力的明显下降,究其原因,我们猜测可能是因长时间的光照打破了果蝇正常生活节律,致使果蝇不能较好的休息,劳累过度,身体机能紊乱,无法正常交配和产卵,或是对卵子精子的可育性有影响。
四.实验结果分析及经验总结
- 4 -
1 研究光照对果蝇的影响应长时间对果蝇进行持续观察,我们组在实验开始时尚能保持观察,后来观察时间减少,致使错过部分果蝇行为活动的变化
2若有足够长时间,还可研究长时间光照对果蝇寿命的影响
3该实验可通过设置不同光照强度,研究不同光照强度对果蝇生长的影响
实验三. 酒精对果蝇生长发育的影响
一. 实验的目的及原理
酒的化学成分为乙醇,分为食用酒精和工业酒精。在日常生活中,少量适当的摄入酒精有祛寒,除湿,提神等保健作用。但若饮酒过量,往往会对身体造成一定伤害
我组以果蝇作为实验对象,研究酒精对果蝇生长发育的影响,为研究酒精对人类的影响提供帮助。
二. 实验方法及步骤
1.培养基的制备
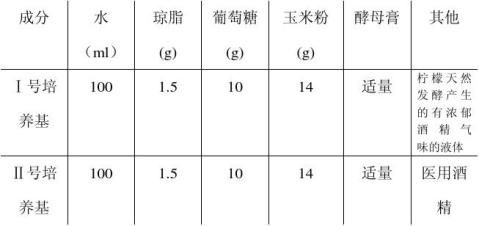
按照下表配置培养基
注意:在加入葡萄糖及玉米粉煮沸丙飘出香味后加入柠檬天然发酵产生的有浓郁酒精气味的液体以及医用酒精。一是为了防止酒精含量过高使果蝇亲本死亡。而是防止高温使酒精完全挥发,保证有一定酒精残留。带培养基冷却只一定
- 5 -
2.将六只培养瓶分为两组
第一组:两只Ⅰ号培养基 ——对照组:一只玉米培养基
第二组:两只Ⅱ号培养基——对照组:一只玉米培养基
3.分别在每个培养瓶中加入9只果蝇(雌雄比2:1)。为防止昏迷果蝇因酒精作用 较长时间无法醒来以至被淹死,可将培养瓶放倒。然后在瓶壁贴好标签注明。
4.一周后倒掉所有亲本果蝇。
5.四天后观察F1代果蝇的生长状况。
三.实验现象及结果
第一组中,F1代果蝇数量相对于对照组较少,精神状态不佳,不活跃
第二组中,F1代果蝇数量明显减少,个体体型偏小,精神状态不佳,不活
跃,雌雄比例与对照组差异大
该实验说明:酒精会破坏果蝇的生长发育于后代繁殖,由于第一组培养基添
加的酒精是柠檬天然发酵产生,浓度较低,故对果蝇生长发育影响较小;第二组
中则添加的医用酒精,浓度高。故对果蝇后代数量及体型的影响都较大
通过该实验,我们可推测饮酒会影响人类胎儿的生长发育及生长。怀孕期
间不宜饮酒。
四.实验结果分析及经验总结
1本实验在酒精浓度的选择上不够精准严谨,为提高成功率,我采用了天然
发酵较为温和的含酒精液体,但该液体中尚含有大量维生素C,一定程度上有缓
冲酒精危害的效力
2培养基中添加酒精,会杀死和抑制酵母菌的生长,果蝇的食物减少,很可
能是这一点导致果蝇体型较小;另外设置对照组时因在熬煮时要添加酒精的缘
故,对照组培养基和实验组培养基不是同一批次进行配置,本身存在一定水平的
营养差异。
在酒精实验的过程中,我们还获得了一下结论
1 .在不给果蝇提供任何养分包括水的情况下,果蝇在接近20小时候死亡
2.过量酒精亦可使果蝇致死,在需要直接致死果蝇的实验中可选用酒精代替乙 醚。安全环保,价格低廉酒精对果蝇不同年龄幼虫影响不同,挑取不同年龄阶段
的幼虫置于含有酒精的
3.培养基中,可观察到一龄幼虫致死率最大,二龄幼虫其次,三龄幼虫存活率
较 高。说明随幼虫长大,其适应外界环境的能力逐步增强。
4.将挑选出的雄性果蝇和雌性果蝇分别装入瓶中,塞上滴加了酒精的瓶塞,可
观察到雌,雄果蝇活动迅速加剧,变得兴奋,且雄性果蝇在适应瓶内环境后会出
现追尾聚集等类似交配的行为。
- 6 -
在观察过程中,要准备一个未滴加酒精的瓶塞与滴加了就进过得瓶塞相互替换,期间不应去碰触或拿起培养瓶,以使果蝇尽快的适应当前环境,方便后续的观察。
- 7 -
