编号:XJ/FX2014005
设备验证的范围及程度
风险评估报告
药业有限公司
质量风险评估报告批准页


目 录
1. 概述
2.风险管理的目的
3. 风险管理小组成员及职责
4. 风险评估
4.1 风险识别
4.2 风险分析与评估
5. 风险控制
1、概述
我公司片剂生产(含中药前处理及提取)使用的设备主要有热风循环烘箱、粉碎机组、双锥混合机、多能提取罐、双效浓缩器、减压干燥柜、离心式喷雾干燥塔、万能粉碎机、喷雾干燥制粒机、高速旋转压片机、荸荠式糖衣机、高效包衣机、铝塑包装机以及其他辅助设施设备等。
2、风险管理的目的
20##年版《药品生产质量管理规范》第七章确认与验证中第一百三十八条指出“企业应当确定需要进行的确认或验证工作,以证明有关操作的关键要素能够得到有效控制。确认或验证的范围和程度应当经过风险评估来确定。”
为满足公司生产的产品持续性的符合国家注册标准要求,并能满足市场客户的需求,安全有效的上市销售。本系统引入质量风险管理的理念,对各生产设备的风险等级进行评估,对可能的危害进行判定,对于每种危害可能产生损害的严重性和危害的发生概率进行了评估,在某一风险水平不可接受时,建议采取降低风险的措施,并对生产设备所处工艺点风险的高低进行等级划分,在日常管理中进行有效的控制,以确保生产出的产品符合质量标准要求。
3、风险管理成员及其职责
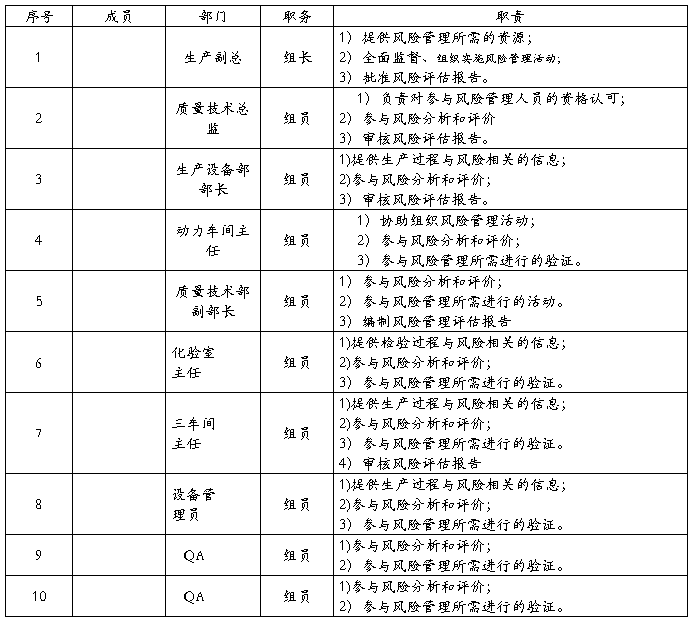
4、风险评估
4.1风险识别
4.1.1影响产品质量的设备一览表及所处工艺点
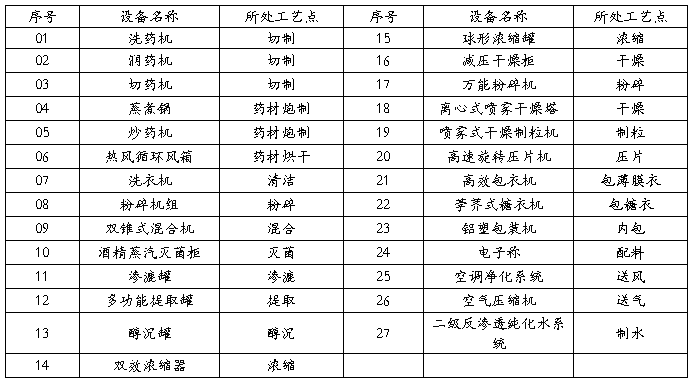
4.2风险分析与评估
4.2.1风险等级判定
采用风险系数(RPN)进行风险优先数量等级判定。
严重程度(S):根据对药品质量的影响判定

? 可能性程度(P):根据出现频次判定

? 可检测性(D):根据风险发生时能够检测的程度判定

4.2.2风险评级及措施要求
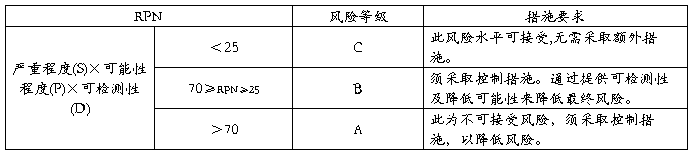
4.2.3生产设备风险分析
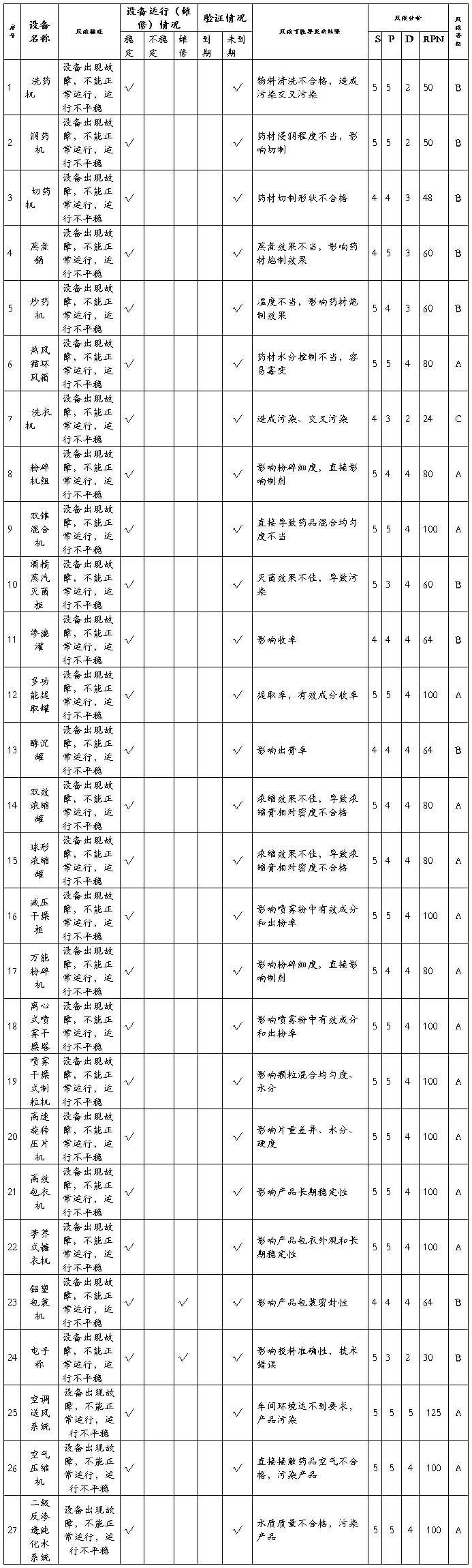
5.风险控制
5.1根据风险优先度排序,以确定需要立即实行风险控制措。
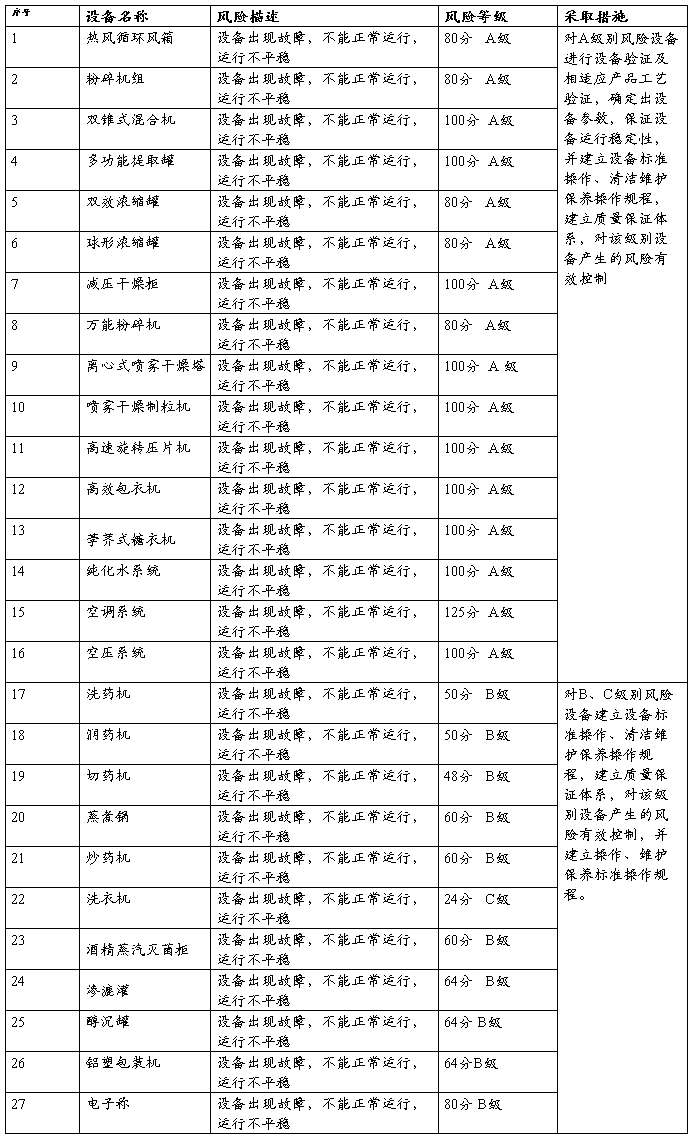
5.2具体设备验证程度见各设备验证报告。
第二篇:清洁验证的风险评估报告
风险评估项目名称 清洁验证风险评估报告
风险评估组组长
参 加 人
起草人/日期
审核人/日期
批准人/日期
一.质量风险评估的目的
2010版GMP第七章“确认与验证”的第一百四十三条规定:“清洁方法应经过验证,证实其清洁的效果,以有效防止污染和交叉污染。清洁验证应综合考虑设备使用情况、所使用的清洁剂和消毒剂、取样方法和位置以及相应的取样回收率、残留物的性质和限度、残留物检验方法的灵敏度等因素。”
本报告的目的,就是运用风险管理的工具,全面评估公司新车间的清洁验证,通过质量风险管理方法评估后确定清洁验证中的风险及相应CAPA措施,以确保经过清洁验证证明的清洁方法具有有效性,能够保证不会产生污染与交叉污染。
二 .范围
评估包括生产系统需要清洁所涉及的工艺设备及管道、物料、控制系统、关键设施、环境控制和人员操作。据此,范围主要是:
? 生产系统需要清洁的所有工艺设备及管道。
? 物料:包括活性成分、中间体、试剂、辅料、清洁剂等。
? 清洁操作时相关的控制系统、关键设施、环境控制:其它辅助设备、公用工程系统(如空调、制水、压缩空气、纯蒸汽系统)等。
?该岗位操作人员的规范操作及培训。
三 .评估方法
进行风险评估所用的方法遵循因果关系图(鱼骨图)以及FMEA技术(失效模 1
式与影响分析),其中FMEA技术包括以下几点。
? 风险确认:可能影响产品质量、产量、工艺操作或数据完整性的风险。 ? 风险判定:包括评估先前确认风险的后果,其基础建立在严重程度、可能性及可探测性上。
? 判定标准:根据医药生产的特点和便于确切的评定等级,本次评估将严重程度、发生的可能性和可探测性的评定等级均分为十级。
严重程度的评定等级表(S) 严重程度(S)的评定等级表
等级 严重程度
1 由于清洁不彻底导致发生轻微污染及交叉污染,但对产品质量影响不明显可以忽略。
2 由于清洁不彻底导致发生轻微污染及交叉污染,但可能导致成品的一般缺
陷,对产品质量影响不太明显。
3 由于清洁不彻底导致发生轻微污染及交叉污染,但可能使产品质量受到一
定影响,导致患者由于成品质量缺陷或药品不良反应以及副作用而感到不满意。
4 由于清洁不彻底导致发生污染及交叉污染,影响药品质量问题而使患者处
于一定危害之中。
5 由于清洁不彻底导致发生严重污染及交叉污染,影响药品质量问题而使患者健康有很大损害,甚至可能导致死亡。
发生的可能性的评定等级表(P)
发生的可能性的评定等级表(P)
发生的可能性 等级
1 发生可能性极低,如:标准设备进行的自动化操作失败。
2 很少发生,如:需要初始配置或调整的自动化操作失败。
3 偶尔发生,如:简单手工操作中因习惯造成的人为失误。
4 极易发生,如:复杂手工操作中的人为失误。
5 肯定会发生,如:复杂手工操作中的未经培训人员的人为失误。
可探测性的评定等级表(D)
可探测性的评定等级表(D)
等级 发生的可能性
1 潜在的缺陷在抵达下一个过程前肯定可以被发现或被防止
2 潜在缺陷在抵达下一个过程前可能由过程控制发现或防止
3 潜在缺陷在抵达下一个过程前不大可能由过程控制发现或防止 4 潜在缺陷在抵达下一个过程前被发现的可能性非常小
5 目前的控制方法无法检测不出潜在的缺陷
2
RPN是事件发生的可能性、严重程度和可探测性三者乘积,用来衡量可能的工艺缺陷,以便采取可能的预防措施.
RPN = Severity(严重程度)×Possibility(发生的可能性)×Detection(可探测性)
风险优先数量等级判定
测量范围1-125 风险优先数量等级判定
<9
严重性×
发生的可能性×
可探测性 9-36
>37
四.通过因果关系图(鱼骨图)找出影响清洁验证效果的因素
1、清洁验证的要求:目测标准、活性成分残留量、清洁剂残留量、微生物污染水平。
2、现在执行的相关质量控制点参数
3、相关设备及管道系统
4、相关控制系统及环境设施
5、人员操作及培训
6、相关取样标准及残留量测定等检验标准
3
4
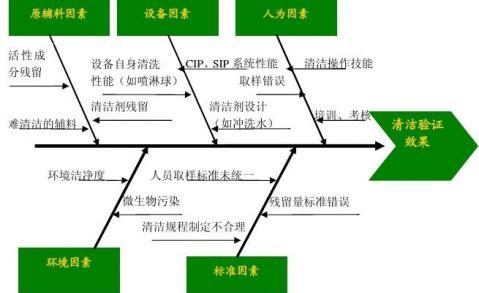
五.失效模式和效果分析(FMEA)
1、对影响清洁验证效果的工艺参数FMEA 分析评估
影响清洁验证效果的工艺参数FMEA 分析评估表
序号 风险项目
潜在失效影响 CIP、SIP系统失效或性能达不到要求。
1
设备
单体设备的自身清洁功能故障或失效。 清洁剂的清洗设计参数不合理。
人员清洁操作失败。
2
人员
人员取样失败。 产品活性成分残留量超标。
3
原辅料
难于清洁的辅料残留量超标。
清洁剂残留量超标。
4
环境
环境洁净度超标导致清洁验证可能失败。 微生物污染导致清洁验证可能失败。 严重程度(S) 5 5 4 5 5 5 5 4 4 4 ①、清洁剂选择不合理;②、人员操作失败。
潜在失效原因
发生的可探可能性测性RPN (P) (D)
2 2 2 2 4 4 4 4 4 4 30 30 24 30 60 60 60 48 48 48 加强员工培训,实行随时监控。 加强员工培训,在文件及方案中明确需在最难清洁部位取样。 ①、事先做好清洁剂选择准备工作,按照ICH“残留溶剂指南”合理选择恰当的清洁剂;
②、加强员工培训,规范SOP操作。
合理选择专属性强、低残留的清洁剂。
加强HVAC、水或者压缩空气、纯蒸汽系统的维护保养工作,验证前予以确认,确保清洁验证的顺利进行。
①、前期介入设备设计工作,做好DQ;
②、做好IQ、OQ、PQ,加强设备维护保养。
CAPA实施措施
系统故障或系统设计缺陷导致死角
3
较多。
单体设备设计缺陷、材质未达要求
或维护保养不力,导致设备清洁不3 能达到要求(如喷淋球设计缺陷)。 清洁剂在极端情况下流速、流型等
3
参数达不到要求,清洁不彻底。 未按SOP操作。 未在最难清洁部位取样。
3 3 3 3
清洁剂的选用不恰当,清洁性能差、
3
残留量高。
HVAC、水或者压缩空气、纯蒸汽系统失效导致清洁验证失败。 3 3 5
清洁之前污染情况过于严重导致无法使用。 在清洁后放置过程中设备被污染。
取样标准不具有代表性。
5
标准
残留量检验标准错误。 5
4 5
时间间隔(待清洁放置时间)太长。 连续生产间歇时,已清洁设备在清
洁后到下一次使用的时间间隔(清3 洁后放置时间)过长,再次被污染。 取样标准未统一。
①、残留量标准制定不合理;②、残留量标准检验方法错误。
3
间的参数,并写入操作SOP。 通过清洁验证确认清洁后放置时间的参数,并写入操作SOP。 取样标准按无菌药品指南制定,加强员工培训。
①、残留量标准按无菌药品指南制定;②、QC需采用经验证的残留量检验方法进行检验,并保持持续的验证状态。
4 2
48 30
3 2 30
2、对中/高风险项目的重新评估
6
改进措施实施后对已经确认的对中/高风险项目的重新评估。见下表:
对影响清洁验证效果的中/高风险项目采取CAPA措施后重新评估表
严重程度(S) 5 5
发生的
可探测
可能性
性(D)
(P) 2
①、前期介入设备设计工作,做好DQ;
2
②、做好IQ、OQ、PQ,加强设备维护保养。
2 加强员工培训,实行随时监控。 2
2 2 2 2 2 2 1 1 1 1 3 2 2 2 2 2 序号 风险项目 潜在失效影响 CIP、SIP系统失效或性
能达不到要求。
潜在失效原因
系统故障或系统设计缺陷导致死角较多。
单体设备设计缺陷、材质未达要求或维护保养不力,导致设备清洁不
能达到要求(如喷淋球设计缺陷)。
清洁剂在极端情况下流速、流型等参数达不到要求,清洁不彻底。 未按SOP操作。 未在最难清洁部位取样。
CAPA实施措施 RPN 10 10 8 10 30 20 20 16 16 16 1 设备
单体设备的自身清洁功能故障或失效。
清洁剂的清洗设计参数
4
不合理。
人员清洁操作失败。 5
2
人员
人员取样失败。 产品活性成分残留量超标。
3
原辅料
难于清洁的辅料残留量超标。
清洁剂残留量超标。
4
环境
环境洁净度超标导致清洁验证可能失败。 微生物污染导致清洁验证可能失败。 5 5 5 4 4 4 加强员工培训,在文件及方案中明确需在最难清洁部位取样。 ①、事先做好清洁剂选择准备工作,按照ICH“残留溶剂指南”
①、清洁剂选择不合理;②、人员
合理选择恰当的清洁剂;
操作失败。
②、加强员工培训,规范SOP操作。
清洁剂的选用不恰当,清洁性能差、合理选择专属性强、低残留的清残留量高。 洁剂。
加强HVAC、水或者压缩空气、
验HVAC、水或者压缩空气、纯蒸汽系纯蒸汽系统的维护保养工作,
统失效导致清洁验证失败。 证前予以确认,确保清洁验证的
顺利进行。 7
清洁之前污染情况过于
严重导致无法使用。
在清洁后放置过程中设
备被污染。
取样标准不具有代表
性。
5 标准
残留量检验标准错误。 5 4 5 时间间隔(待清洁放置时间)太长。 时间的参数,并写入操作SOP。 连续生产间歇时,已清洁设备在清通过清洁验证确认清洁后放置2 洁后到下一次使用的时间间隔(清时间的参数,并写入操作SOP。 洁后放置时间)过长,再次被污染。 取样标准按无菌药品指南制定,取样标准未统一。 2 加强员工培训。 ①、残留量标准按无菌药品指南①、残留量标准制定不合理;②、制定;②、QC需采用经验证的2 残留量检验方法进行检验,并保残留量标准检验方法错误。
持持续的验证状态。 2 2 16 20 2 20
8
六.本次风险评估结论:
影响清洁验证效果的主要中高风险点存在于人员操作、原辅料和清洁剂残留量以及清洁操作时相关的设备控制系统、环境控制系统、辅助设备等。在清洁验证中应作为检查监控的重点,将所有中等风险和高风险点作为质量控制点,在验证方案及报告中检查记录。
对所有已知的风险均应采取针对性的CAPA措施:硬件方面,从DQ方面就实现介入,做好IQ、OQ、PQ,通过设备调试优化、加强维护保养来杜绝风险的发生;软件方面,通过参照相关指南来科学制订检验标准,系统制订相关SMP和SOP、加强人员培训和检查监控,以降低清洁验证中的风险。
9
