分子生物学与基因工程原理实验报告 ----绿色荧光蛋白(GFP)基因的克隆和表达
姓名:张可欣 王跃
学号:201220142012 201220142022
组别:1组
背景知识
绿色荧光蛋白(green fluorescent protein,GFP)是一类存在于包括水母、水螅和珊瑚等腔肠动物体内的生物发光蛋白。当受到紫外或蓝光激发时,GFP发射绿色荧光。它产生荧光无需底物或辅因子发色团是其蛋白质一级序列固有的。GFP基因由3个外显子组成,长2.6kb;GFP是由 238个氨基酸所组成的单体蛋白 ,相对分子质量为27.0 kMr,其蛋白性质十分稳定,能耐受60℃处理。19xx年GFP的晶体结构被解出,蛋白质中央是一个圆柱形水桶样结构,长420 nm,宽 240 nm,由 11个围绕中心α螺旋的反平行β折叠组成,荧光基团的形成就是从这个螺旋开始的,桶的顶部由 3个短的垂直片段覆盖,底部由一个短的垂直片段覆盖,对荧光活性很重要的生色团则位于大空
腔内。发色团是由其蛋白质内部第65-67位的
Ser-Tyr-Gly自身环化和氧化形成。
19xx年GFP的晶体结构被解出,蛋白质中央是一
个圆柱形水桶样结构,长420 nm,宽240 nm,由11
个围绕中心α螺旋的反平行β折叠组成,荧光基团的
形成就是从这个螺旋开始的,桶的顶部由3个短的垂直
片段覆盖,底部由一个短的垂直片段覆盖,对荧光活
性很重要的生色团则位于大空腔内。
实验一 质粒DNA的分离与纯化
一、实验目的
掌握一种最常用的质粒 DNA提取方法:碱裂解法。该法用于从小量培养物中抽提质粒DNA,比较方便、省时,提取的质粒 DNA质量较高,可用于DNA的酶切、PCR甚至测序。
二、基本原理

质粒是一类在细菌细胞内发现的独立于染色体外,能够自主复制的稳定的遗传单位。迄今为止,从细菌中分离得到的质粒都是环型双链DNA分子,分子量范围从1kb到200kb。质粒DNA可持续稳定地处于染色体外的游离状态,但在一定条件下又会可逆地整合到寄主染色体上,随着染色体的复制而复制,并通过细胞分裂传递到后代。在大多数情况下质粒 DNA复制中的酶体系和细菌染色体复制时所用的酶是相同的。有些质粒复制受宿主细胞复制作用的严格限制,因此每个细胞中只含一个或几个拷贝,称为严谨型质粒,有的质粒的复制受宿主细胞的控制不严,称为松弛型质粒,它们在每个细胞中的数目可达 10-200个拷贝。当宿主细胞的蛋白质合成受到抑制时(例如经氯霉素处理),细菌染色体虽不再增加,但松弛型质粒 DNA可继续被复制,以至每个细胞内的拷贝数可以增至一千到几千。
质粒具有一定的生物功能,它们往往带有一些抗药标记,当质粒DNA用人为的方法转化进细菌时,转化后的细菌会表现出质粒基因所具有的新的生物表现型,例如,把一个含有抗药基因的质粒转入细菌后,原来无抗药性的细菌则表现出抗药的新表型。借助转化菌获得的新表型特征,可证实质粒已转入宿主细菌中,这样就可以作为转化菌的选择性标记。
质粒作为基因克隆载体分子的重要的条件是获得批量的纯化的质粒 DNA分子。目前已有许多方法可用于质粒 DNA的提取,它们都包括三个基本的步骤:细菌的生长和质粒的扩增;菌体的收集裂解,质粒DNA的分离;质粒DNA的纯化。
1、细菌的生长和质粒的扩增
从琼脂培养基平板上挑取一个单菌落,接种到含适当抗生素的液体培养基中培养。对于松弛型质粒(如 pUC系列)来说,只要将培养物放到标准的LB或 2YT培养基中生长到对数晚期,就可以大量提取质粒,而不必选择性地扩增质粒 DNA。但对于严谨型质粒(如 pBR322)来说,则需在得到部分生长的细菌培养物中加入氯霉素继续培养若干小时,以便对质粒进行选择性扩增。
2、菌体的收集、裂解和质粒 DNA的分离
质粒分离的基本原理是利用宿主菌(一般是大肠杆菌菌株)DNA与质粒DNA之间的两种主要性质差异:(1)大肠杆菌的染色体较一般的载体质粒 DNA大得多。(2)从细胞中提取得到的大肠杆菌 DNA主体是变性的线性分子,而大多
数质粒 DNA是共价闭合的环状分子。这里主要介绍碱裂解法的基本原理:在细菌悬浮液中加入 SDS(十二烷基硫酸钠)和 NaOH使菌体裂解(有时需要先使用溶菌酶水解细胞壁)。此处理可破坏碱基配对,故可使细菌的线状染色体DNA变性,但闭环质粒 DNA链由于处于拓扑缠绕状态而不能彼此分开。当条件恢复正常时(如加入酸性的 NaAc或 Kac中和碱性 NaOH),质粒 DNA链迅速得到准确配对,重新恢复成天然的超螺旋分子。通过离心,可以使染色体 DNA与变性蛋白质、RNA分子一起沉淀下来,而质粒超螺旋分子仍滞留于上清中。
3、质粒 DNA的提纯
对于小量制备的质粒 DNA,经过苯酚抽提、RNA酶消化和酒精沉淀等简单步骤除去残余蛋白质及 RNA,达到纯化的目的。质粒 DNA分子具有三种构型:共价闭合环形 DNA(cccDNA,SC构型)、开环 DNA(OC构型)和线性分子(L构型)。在细菌体内,质粒 DNA是以负超螺旋构型存在的。在琼脂糖凝胶电泳中不同构型的同一种质粒 DNA,尽管分子量相同,但具有不同的电泳迁移率。其中走在最前沿的是 SC DNA,其后依次是 L DNA和 OC DNA。
三、实验材料、仪器及试剂
1.在含有pEGFP-N3质粒的DH5α平板上菌落上挑取菌种,置于含有5mLLB培养基的试管中。摇晃过夜。
在含有 pET-28a质粒的平板上挑取单菌落于另外一个试管中,同样摇荡培养过夜。
2、使用仪器
恒温培养箱,超净台,恒温摇床,制冰机,台式离心机,小型混合器,冰箱。
3.试剂
①? LB培养基的配制:
组成
蛋白胨(Trypton)
酵母提取物(Yeast Extract)
NaCl
琼脂(Agar)
蒸馏水 液体 10g 5g 10g 定容至1000ml 固体 10g 5g 10g 15g 定容至1000ml
培养基配制完成后要进行两小时的灭菌处理。
②溶液Ⅰ:50ml葡萄糖,25mM Tris-HCl(PH8.0),10mM EDTA。
③溶液Ⅱ(现用现配):0.2N NaOH,1% SDS(先加水,再加 NaOH和 SDS)。 ④溶液Ⅲ(100ml):60ml 5M KAc,60ml 11.5ml冰醋酸。
四、实验步骤
1.分别取N3,28α质粒。取2.0ml DH5α培养液倒入2.0mL圆底离心管中,13000rpm离心1min。
2.在同一离心管中,重复1。离心后弃上清,再离心.
3.弃上清,将管倒置于卫生纸上数分钟,使液体流尽。(沉淀为收集的菌体)
4.菌体沉淀重悬浮于100μL溶液Ⅰ中(需用涡旋仪剧烈振荡混匀),室温下放置10min。(破碎细胞)
5.加入新配制的溶液Ⅱ200μl(SDS与NaOH等量混匀),盖紧管口,快速温和颠倒(手动)离心管5次,以混匀内容物(千万不要振荡),冰浴5min。(使拟核DNA和蛋白质变性)
6.加入150μL预冷的溶液Ⅲ,盖紧管口,并倒置离心管,温和振荡3次,使沉淀混匀,冰浴中15min,13000rpm离心5min。(中和,质粒DNA恢复超螺旋)
7.上清液350μl移入干净离心管中,加入450μl等体积的氯仿/异戊醇(24:1),振荡混匀,13000rpm离心2min。(沉淀蛋白质等)
8.将水相移入干净离心管中,在通风橱中加入450μl等体积的氯仿/异戊醇(24:
1)振荡混匀,13000rpm离心2min。(沉淀蛋白质等)
9.将水相移入干净离心管中,加入2倍体积的无水乙醇,振荡混匀后,置于室温下2min,然后13000rpm离心5min。(洗涤,沉淀质粒DNA)
10.弃上清,将管口敞开倒置于卫生纸上使所有液体流出,加入 1mL 70%乙醇洗沉淀一次,振荡混匀后,13000rpm离心5min。(洗涤,沉淀质粒DNA)
11.吸除上清液,将管倒置于卫生纸上使液体流尽,室温干燥。
12.将沉淀溶于30μL ddH2O中,18μL用于实验二酶切,12μL剩余样品作为参比用于实验三电泳。
注意事项:氯仿/异戊醇是有机溶剂,容易腐蚀移液枪,因此在吸取氯仿时,
要直上直下操作,及时退掉枪头,防止移液枪被腐蚀。
实验二 质粒DNA酶切及浓度的测定
一、实验目的:
学习使用限制型内切酶进行DNA酶切的原理和方法。
学习利用核酸蛋白测定仪测算核酸的浓度和纯度。
二、基本原理:
1.迄今已发现了3000多种限制性内切酶。传统上将限制性内切酶按照亚基组成、
酶切位置、识别位点、辅助因子等因素划分为三大类。II型酶在其识别位点之
中或临近的确定位点特异地切开DNA链。它们产生确定的限制片段,因此是三类
限制性内切酶中唯一用于DNA分析和克隆的一类。
II型限制性内切酶中最普遍的是象EcoRI、HindIII、BamHI和NotI这样在
识别序列中进行切割的酶。这一类酶是构成商业化酶的主要部分。大部分这类酶
都以同二聚体的形式结合到DNA上,因而识别的是对称序列;但有极少的酶作为
单聚体结合到DNA上,识别非对称序列。一些酶识别连续的序列(如EcoRI识别
GAATTC;HindIII识别AAGCTT;BamHI识别G↓GATCC;NotI识别GC↓GGCCGC);
而另一些识别不连续的序列(如BglI识别GCCNNNNNGGC)。限制性内切酶酶切
DNA后形成两种类型的末端:
(i)两条链断裂的位置是交错地,产生粘性末端,如EcoRI酶切后产生 5’-G↓AATTC-3’
3’-CTTAA↓G-5’ 末端;
(ii)两条链的断裂位置处在一个对称结构的中心,产生平末端,如HaeⅠⅠ
Ⅰ酶切后产生5’-GG↓CC-3’
3’-CC↓GG-5’ 末端。
DNA连接酶能够催化在两条DNA链之间形成磷酸二酯键,这种酶需要在一条
DNA链的3’-末端具有一个游离的羟基(-OH),和在另一条DNA链的5’-末端
具有一个磷酸基团(-P)。
5’ 3’
(1)pET-28α质粒全图谱:
3’ 5’
表达EGFP蛋白使用的pET-28α原核载体质粒包含有在多克隆位点两侧的His-tagpolyHis编码序列;用于表达蛋白的T7启动子,T7转录起始物以及T7终止子;选择性筛选使用的lacI编码序列及卡那霉素抗性序列,pBR322启动子,以及为产生单链DNA产物的f1启动子。
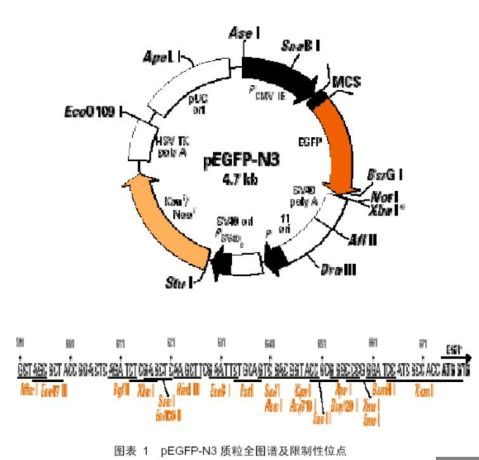
(2)pEGFP-N3质粒全图谱:
实验使用的EGFP蛋白取自原核-真核穿梭质粒pEGFP-N3的蛋白质编码序列。此质粒原本被设计于在原核系统中进行扩增,并可在真核哺乳动物细胞中进行表达。本质粒主要包括位于PCMV真核启动子与SV40真核多聚腺苷酸尾部之间的EGFP编码序列与位于EGFP上游的多克隆位点;一个由SV40早期启动子启动的
卡那霉素/新霉素抗性基因,以及上游的细菌启动子可启动在原核系统中的复制与卡那抗性。在EGFP编码序列上下游,存在特异的BamH I及Not I限制性内切酶位点,可切下整段EGFP编码序列。
2.核酸分子在 260nm下有最大吸光值,因此可以通过260nm下核酸的吸光值计算核酸浓度(mg/ml),并通过测定与 280nm和 230nm的比值,估算 DNA的纯度。
三、实验材料与仪器
1、实验材料
pEGFP-N3,pET-28aDNA。
2.使用仪器
Micro-Spectrophotometer核酸蛋白测定仪,移液枪,冰箱。
3.试剂:
BamHI(10U/μL)(TaKaRa公司),NotI(10U/μL)(TaKaRa公司),T4ligase。
四、实验步骤
(一)酶切:
1.按如下双酶切体系(30μL)混合:
反应物
质粒
BamH Ⅰ Not Ⅰ
10×buffer K
ddH2O
2.离心 10s,混匀。
3.-20℃冰箱酶切 1周。
(二)浓度测定:
1.打开开关。
2.按‘Nucleicacid’键,使用‘Select’键选择屏幕中‘DS-DNA’。
3.在检测基座上加入1μlddH2O,按下Blank键做空白检测。
4.用吸水纸拭去检测基座上的ddH2O。在检测基座上分别加入1μl N3、28α质pEGFP-N3(μL) 18 2 2 3 5 pET-28a(μL) 18 2 2 3 5
粒DNA样品,按下Measure键测定样品浓度和纯度。
DNA的纯度:OD260nm/280nm=1.8±0.1(如果低于1.7,说明样品中蛋白质去除的不完全,或样品中有苯酚的污染;如果高于1.9,说明样品中RNA去除的不完全)。
五、实验结果:
下图数据:①左侧:纯度;②右侧:浓度。
Ⅰ、N3: Ⅱ、 28α:

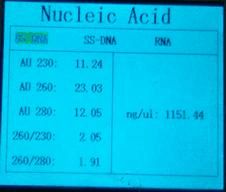
结果分析:N3样品处理成功;28α样品中RNA去除的不完全
实验三 琼脂糖凝胶电泳及连接
一、实验目的
学习掌握一种最常用的分离、鉴定、纯化 DNA片段的比较方便、省时的技术:琼脂糖凝胶电泳的基本原理和操作方法。
二、实验原理
影响DNA在琼脂糖凝胶中迁移速率的因素主要有:(1)DNA分子的大小双链DNA分子在凝胶基质中迁移的速率与其碱基对数的常用对数成反比。分子越大,迁移的越慢,因为摩擦阻力越大,也因为大分子通过凝胶孔径的效率低于较小的分子。(2)琼脂糖浓度给定大小的线状DNA片段在不同浓度的琼脂糖凝胶中迁移速率不同。在DNA电泳迁移速率的对数和凝胶浓度之间存在线性相关。(3)DNA的构象超螺旋环状(Ⅰ型)、切口环状(Ⅱ型)和线状(Ⅲ型)DNA在琼脂糖凝胶中以不同速率迁移。其相对迁移速率主要取决于琼脂糖凝胶的浓度和类
型,其次是电流强度、缓冲液离子强度和Ⅰ型超螺旋绞紧的程度或密度。一些条件下,Ⅰ型DNA比Ⅲ型迁移得快;在另一些条件下,顺序可能相反。(4)所用的电压低电压时,DNA片段迁移率与所用的电压成正比。电场强度升高时,高分子量片段的迁移率遂不成比例的增加。所以,当电压增大时琼脂糖凝胶分离的有效范围反而减小。要获得大于2kbDNA片段的良好分辨率,所用电压不应高于5-8V/cm。(5)电泳缓冲液DNA的泳动受电泳缓冲液的组成和离子强度的影响。缺乏离子则电导率降低,DNA或者不动或者迁移很慢。高离子强度时(如10×buffer),电导率升高,使得应用适中的电压也会产生大量的热能,最严重时凝胶会熔化,DNA变性。
三、实验材料、仪器及试剂
1.实验材料
pEGFP-N3和pET-28a DNA
2.仪器
电泳槽、核酸电泳仪、振荡器、制冰机、蓝盾可见光透射仪、凝胶成像仪,刀片,冰箱。
3.试剂
50×TAE:Tris碱 242g,Na2EDTA.2H2O 37.2g,加入约 800ml的去离子水,充分搅拌溶解。
GeneFinder-溴酚蓝上样缓冲液(6×loadingbuffer):0.25%溴酚兰,0.25%二甲苯青FF,40%(w/v)蔗糖水溶液。配制好后可以按50:1的比例稀释GeneFinder。
四、操作步骤
1.加 100ml 1×TAE缓冲液于三角瓶中,
2.精确称取1g琼脂糖加到三角瓶中,于微波炉中加热至完全熔化,
3.冷却至60℃左右,
4.轻缓倒入封好两端的电泳胶板中,插好梳子静置待凝胶凝固,
5.放入电泳缓冲液(1×TAE)中,使电泳缓冲液刚好没过凝胶约 1mm,轻轻拔除梳子。
6.按下表分别混匀,三孔上样。

7.100v(3-4V/cm)约电泳30min。
8.荧光激发器观察质粒 DNA条带的酶切情况。条带分离适中后,并用凝胶成像系统采集照片。
9.回收酶切产物(采用天为时代DNA回收试剂盒进行回收):
(1)用干净的刀片将需要的DNA条带从凝胶上切下来,放置于离心管中差量法称取重量。
(2)以0.1g凝胶对应300μL的体积加入PN。 (3)50℃水浴放置10min,期间不断温和上下翻动(防止过热)离心管至胶完全融解。
(4)将上一步得到的溶液加入到一个吸附柱中,吸附柱再放入离心管,13000rpm离心60s,弃掉废液。 (5)加入800μL漂洗液PW,13000rpm离心60s,弃掉废液。(洗柱)
(6)加入500μL漂洗液PW,13000rpm离心60s,弃掉废液。(洗柱)
(7)将离心吸附柱放回收集管,13000rpm离心2min。(去掉残留的洗脱液)
(8)取出吸附柱,放入一个干净的离心管中,在吸附膜的中间位置加入适量洗脱缓冲液EB30μL,洗脱缓冲液先在65℃水浴预热,室温放置2min,13000rpm离心1min,然后将离心的溶液重新加回离心吸附柱中,13000rpm离心1min。(两次洗脱后,样品在离心管中)
10.连接:
按照下表中连接体系进行,连接一周。
反应物
回收纯化的pET-28α质粒
GFP基因片段
T4连接酶
缓冲液(10×) 体积/μL 5 12 1 2
五、实验结果:
跑胶方向为自左向右。样品从上向下依次是Marker样品,酶切N3质粒样品,酶切28α质粒样品。

实验四 大肠杆菌感受态细胞的制备及转化
一、实验目的:
了解和掌握大肠杆菌感受态细胞的制备方法的原理和操作要点,以及质粒 DNA转化大肠杆菌细胞的原理和方法。
二、实验原理:
外源 DNA只有转化到大肠杆菌细胞内才能得到扩增。感受态指细菌细胞具有的能够接受外源 DNA的一种特殊生理状态。大肠杆菌的感受态可用 CaCl2处理而诱导产生:将正在生长的大肠杆菌细胞在 0℃下加入到低渗的 CaCl2溶液中,便会使细胞膜的透性发生改变,此时的细胞即呈现为感受态。这一方法可以用于批量制备感受态细胞,其转化效率可达到5×106 -2×107个转化克隆子/μg超螺旋质粒 DNA。制备好的大肠杆菌感受态细胞可在-70℃冻存。
在 0℃下外源 DNA可吸附到感受态细胞表面,短时间的热刺激( 42℃,90s)诱导细胞吸收 DNA。转化了质粒 DNA的大肠杆菌随后在培养基中 37℃培养 1hr,可使质粒 DNA中编码抗生素抗性的基因得以表达,因此,转化了质粒 DNA的大肠杆菌细胞可在含有相应抗生素的培养基上生长,而没有转化的细胞则无法
生长。
三、实验材料、仪器:
1.实验材料
DH5α, pET-28a重组质粒DNA。
2.使用仪器
水浴锅,高压灭菌锅、移液器、超净工作台、离心机、振荡培养箱,制冰机。
四、操作步骤:
1. LB(Luria-Bertain)液体和固体培养基的配制(参考实验一)
培养基配制完成后要进行两小时的灭菌处理。氨苄青霉素和卡那霉素等抗生素不抗热,如果培养基温度过高,容易导致抗生素失效,应使培养基降温至 60℃左右后,再加入抗生素。但也不应使培养基的温度过低,否则容易出现气泡。75mm直径的培养皿约需15ml培养基。
2.感受态细胞的制备(CaCl2法)(超净工作台操作)
(1)挑一大肠杆菌单菌落放入3mlLB液体培养基(不含Kan),37℃培养过夜。
(2)活化大肠杆菌:取3ml新鲜的LB液体培养基加入50-150μl的过夜菌,培养2-3个小时,OD600在0.4-0.6之间。
(3)将活化的DH5α培养液转入离心管中,冰上放置10min,然后于4℃下4000rpm离心5min。(低转速防止细胞的破碎,采用1.5ml同管两次离心沉淀的方法)
(4)弃去上清,用预冷的0.1mol/L的CaCl2溶液600μL轻轻悬浮细胞(吹吸),冰上放置20min,4℃下4000rpm离心5min。(Ca2+与细胞膜作用,冷处理后,使膜表面产生裂缝)
(5)弃去上清,加入300μL预冷的0.1mol/L的CaCl2溶液,轻轻悬浮细胞(吹吸),冰上放置5min,即成感受态细胞悬液,可-80℃长期保存。(Ca2+与细胞膜作用,冷处理后,使膜表面产生裂缝)
3.转化涂板
(1)取2个无菌离心管,分别加入100μL,200μLDH5α感受态细胞悬液,第1管加10μlddH2O(参比),第2管加入质粒DNA溶液20μl,轻轻摇匀,冰上放置30min。
(2)42℃水浴中热激90s,热激后迅速置于冰上冷却5min。(使膜表面产生裂
缝)
(3)分别向管中加入100μLLB液体培养基,混匀后在37℃振荡培养30min。(细胞扩增)
(4)从管1中分别取50μL涂布于含抗生素和不含抗生素的平板上,从管2中取220μL涂布于含抗生素的平板上。正面向上放置约10分钟,待菌液完全被培养基吸收后倒置培养皿,37℃过夜培养。凝胶成像系统采集图片。
管1 管1 管2

50μL 50μL 220μL
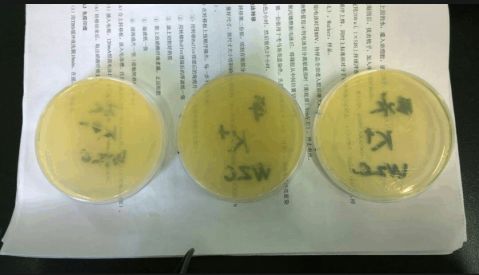
五、实验结果:
下图中,自左向右依次是管1 Kan-,管2 Kan+,管1 Kan+。

实验五 重组质粒DNA的鉴定(菌落PCR法)
一、实验目的
掌握菌落PCR法鉴定重组质粒DNA的基本原理,了解菌落PCR法鉴定菌落及保存的操作方法。
二、基本原理
单菌落或提取的质粒 DNA可以通过PCR方法鉴定正确克隆。聚合酶链式反应(Polymerase Chain Reaction,简称 PCR)是体外酶促合成特异 DNA片段的一种方法。典型的PCR由高温变性、低温退火和适温延伸等三步反应组成一个循环周期,通过多次循环反应,使目的 DNA得以迅速扩增。其主要步骤是:将待扩增的 DNA置于高温下使之解链,人工合成的两个寡核苷酸引物在低温下分别在目的片段两侧与 DNA两条链互补结合;DNA聚合酶在72℃将单核苷酸从引物的 3’端开始掺入,沿模板从 5’→3’方向延伸,合成 DNA的新互补链。
具体地说,PCR反应系统有寡核苷酸引物,反应缓冲液,热稳定 DNA聚合酶(Taq酶),脱氧核苷三磷酸底物和靶序列(即模板)等五部分组成,缺一不可。
PCR技术能在试管中建立反应,经数小时之后,就能将极微量的某一特定的目的DNA片段扩增 106倍以上,而无需经过烦琐的基因克隆程序便可获得足够数量的精确的 DNA拷贝。它操作简单,易于掌握,结果也较为可靠,为基因的分析和研究提供了一种强有力的手段,对整个生命科学的研究与发展都有深远的影响。因此,PCR技术产生的时间虽不长,却以惊人的速广泛地应用于分子生物学的各个领域。它可用于基因的分离、克隆和核苷酸序列分析、突变体和重组体的构建、基因表达调控的研究、基因多态性的分析、遗传病和传染病的诊断、肿瘤机制的探索及法医鉴定等诸多方面。
三、实验材料、仪器及试剂
1.实验材料
pET-28a重组质粒 DNA或菌落
2.使用仪器
PCR仪,掌中宝离心机,冰箱,小型混合器,电泳槽和电泳仪,移液器及吸头,蓝盾可见光透射仪。
3.GFP基因扩增
正向引物:5’-ggg CATATg gTg AgC AAg ggC gAg g-3’,反向引物:5’-ggg CTC gAg TTA CTT gTA CAg CTC g-3’。
四、实验步骤
1.挑取菌落
在管2培养平板上随机挑取5个菌落。首先使用无菌枪头挑取菌落,在已准备好的含有卡那抗菌素,分好区的固体培养基中轻划一下(为保菌种)(实验六中不用这个菌种,故省去这一步),然后将余下菌置于离心管中(作为PCR反应模板)。
2.PCR反应体系(20μl)
反应物
dNTP(10mM) 左引物
右引物
Taq酶(5U/μl) MgCl2(25mM)
10×Buffer ddH2O
3.PCR循环:
(1)95℃5min予变性;(长时间质粒完全变性)
(2)(95℃30s(变性);58℃30s(退火,引物结合);72℃45s(延伸))35cycles;(引物作用下,只扩增GFP片段)
(3)72℃10min延伸。
4.PCR产物的检测
20μl PCR产物加入4μl溴酚蓝-GeneFinder混合液,3μl Marker加入1μl溴酚蓝-GeneFinder混合液,分别按编号加入DNA琼脂糖凝胶电泳的加样孔,体积/μl 2 5 5 2 6 10 69.5
使用1%琼脂糖电泳分离。100V,30min。
5.用荧光激发器看结果,确定阳性克隆的位置。并采集照片。
五、实验结果:
点样孔洞穿,无结果。
实验六 GFP蛋白的诱导表达
一、实验目的
掌握用IPTG诱导GFP基因表达的基本原理及基本操作步骤。
二、实验原理
IPTG(异丙基硫代β-L半乳糖苷)是一种常见的诱导基因表达的诱导剂,结构类似乳糖。
GFP基因连接到pET-28a的多克隆位点(MCS),GFP基因的表达受其上游T7启动子和操纵基因O位点以及结合到这些顺式作用元件的蛋白因子的控制。LacI基因编码调节蛋白,可以四聚体的形式结合到操纵基因O位点上,关闭GFP基因的表达。IPTG可与四聚体调节蛋白结合,从而改变调节蛋白的构象,使调节蛋白不再与O位点结合。接着BL21编码的T7RNA聚合酶结合到T7启动子位点,从而启动GFP基因的表达。
三、实验材料和仪器
1.实验材料
BL21,pET-28a重组质粒DNA(老师连接的)。
2.使用仪器
离心机,冰箱,小型混合器,移液器,恒温培养箱,荧光发射器,超净工作台。
四、实验步骤
1.取阳性克隆质粒DNA转化BL21。(BL21是用于基因表达的菌株)
2.在含有Kan的固体培养基上,37℃培养20h。
3.挑取单菌落,37℃振荡培养过夜。
4.取4支无菌带盖试管,加入新鲜LB液体培养基(含有Kan)5ml,按1:20稀释比例加入过夜菌,37℃培养至生长期,约2-3小时。
5.加入IPTG(1:1000)至终浓度1mmol/L,分别诱导1h,2h,3h。
6.三个时间段分别取1.5ml,10000rpm离心5min,去除上清,收集沉淀,
7.观察蛋白表达:
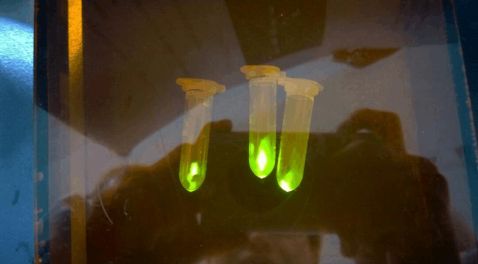
用荧光发射器照射表达蛋白的样品管,照相,保存照片。
五、实验结果
下图从左向右依次是1h,3h,2h。
实验七 Southern杂交
一、目的
进一步筛选出重组质粒DNA。
掌握Southern杂交的基本原理及基本操作步骤。
二、基本原理
DNA印迹杂交法是指利用毛细管作用,将变性DNA从凝胶上转移到硝酸纤维素膜或尼龙膜上,加以固定后用探针杂交的技术。此法是由 Dr.Southern 19xx年建立的,它是分子生物学研究领域中最常用的技术之一,为后来发展的各种生
物大分子杂交技术提供了重要的理论和实践基础。
分子杂交技术是根据两条单链 DNA(或 DNA与 RNA)中互补碱基序列能专一配对的原理进行的。在一定条件下,单链 DNA或 RNA能与另一条单链 DNA互补的碱基形成氢键,从而使两条单链杂交形成双链 DNA分子。
Southern印迹杂交技术是由:电泳,印迹,固定和检测 4个步骤组成。即用一种或几种限制性内切酶消化 DNA分子,通过琼脂糖凝胶电泳按分子量大小分离所得片段,随后使 DNA在原位发生变性,并从凝胶中转移至一固相支持物上(通常为硝酸纤维素膜或尼龙膜)。DNA转至固相支持物的过程中,各个 DNA片段的相对位置保持不变,用放射性标记或非放射性标记的 DNA或 RNA探针与固定于膜上的 DNA分子进行杂交,经放射自显影或显色反应确定所有与探针杂交的片段的位置。
探针很难与琼脂糖凝胶中的 DNA进行杂交,因此必须把 DNA转移至一固相支持物上。DNA在高盐存在下,可以通过毛细作用印迹到膜上(目前又发展了真空转移和电转移等技术)。DNA片段的大小对转移率有很大的影响,大的 DNA片段较难定量转移,一般可用短波长紫外线照射凝胶,将其中的 DNA断裂为较小的片段,以利转移。实验表明,单链 DNA的平均长度在大约 1000个碱基时即可充分转移。
能产生可检测杂交信号所需的 DNA量取决于几个因素:DNA中与探针互补部分所占比例,探针的大小与比活,膜上 DNA的量。在最佳条件下经放射自显影曝光书天后这一方法的灵敏度足以检出不到 0.1pg的与高比活32P标记的探针(109 cpm/)互补的DNA。Southern印迹杂交方法通常需要10?g基因组DNA。
杂交所用探针一般多采用放射性同位素标记,但由于非放射性探针标记对人体无害,无同位素污染及其后处理等优点,此外,标记的探针可长期保存,随时可用,所以非放射性探针标记越来越受到重视。
本试验采用非放射性地高辛标记技术。
非放射性 DIG系统利用地高辛(digoxigenin, DIG)标记 DNA、RNA或寡核苷酸作探针,以便进行杂交及随后的显色或化学发光检测。
非放射性探针标记方法之一是采用由间壁连接有类固醇半抗原的异羟基泽地黄毒苷配基标记的 dUTP(缩写 DIG-dUTP)作为 DNA合成的底物,经随机标
记法掺入新合成的DNA中,形成非放射性同位素标记探针,杂交后,用相应的碱性磷酸酶酶联抗体检测 DIG标记DNA的存在。在X-磷酸盐和硝基蓝四锉盐(NBT)存在下,碱性磷酸酶催化生色反应。显示出所检测的目标 DNA所在。
对 DNA标记来说,DIG通过一个不耐碱的酯键与dUTP相联。使用不耐碱的DIG-11dUTP可以更容易和有效地除去膜上的探针,利用第二种 DIG标记的探针进行再杂交。不耐碱的 DIG-11dUTP标记的 DNA探针不能用碱(NaOH)变性。必须在沸水中保温变性。
DNA标记:DIG-High Prime系统是以随机引物标记的原理标记 DNA探针。在 5×反应缓冲液中预先混合了随机引物标记的所有试剂,即可节省步骤又可以提高产量和可重复性,十分方便。DIG-High Prime系统可以用小到200bp的 DNA片段、线性化的质粒、粘粒或λDNA甚至超螺旋的质粒作为标记的模板。
DIG-High Prime标记反应的产量:在标准反应中37℃保温 1小时,由 1μg的对照DNA可以产生 800ng的DIG标记的DNA。标记片段的长度为200-1000bp。
杂交:有别于同位素标记的杂交反应,我们推荐使用 DIG Easy Hyb(一种可以立即使用的无毒的杂交液),它可以将杂交的时间降到低于 4小时。
免疫检测:杂交后的探针与偶联有碱性磷酸酶的抗体(anti-DIG-AP)结合,然后用显色底物 NBT/BCIP(见 DIG DNA Labeling and Detection kit)或化学发光底物 CSPD(见DIG Luminescent Detection Kit for Nucleic Acid)检测与 DIG结合的抗体。
步骤
DNA标记
杂交
免疫检测
显色反应
反应时间 10分钟-过夜 6小时或过夜 1.5小时 0.5-16小时
三、试剂配制
1.美莱博(Mylab)公司DIG High Primer Labelling and Dection Sterter Kit I成分。
这些试剂按下面的配方配制:
(1)缓冲液1.马来酸缓冲液(maleicacidbuffer)[含有组分:0.1Mmaleicacid,0.15MNaCl;用固体NaOH将pH调到7.5(20℃)]
配制方法:将马来酸缓冲液(干粉)用800ml水溶解,反复冲洗干净瓶内干粉。
检查pH是否为7.5。定容至1L。
(2)缓冲液2.洗涤缓冲液(Washing buffer)
马来酸缓冲液加入0.3%Tween20(v/v)。
(3)缓冲液3.阻断液
将10×阻断液母液用马来酸缓冲液稀释10倍,制备成1×阻断液。
(4)缓冲液4.检测缓冲液
0.1MTris-HCl,0.1MNaCl,pH9.5(20℃)。
(5)缓冲液5.TE缓冲液
10mMTris-HCl,1mMEDTApH8.0。
(6)溶液6.抗体溶液
每次使用前,需10,000rpm离心抗DIG-AP酶结合物5分钟,从表面小心 吸取所需的量。用阻断液按1:5000稀释抗体。
2.显色溶液
必须新鲜配制:在10ml缓冲液4中加入200μlNBT/BCIP浓贮备液。
3.采用公司“primer-a-gene”labelingkit和DIG-dUTP进行探针标记。
四、使用仪器
稳压电泳仪;电泳槽;紫外检测仪;电热恒温水浴锅;杂交炉;恒温振荡器等。
用品及器具:保险膜,杂交管,吸水纸,解剖刀,增感屏,瓷盘,镊子,塑料手套,滤纸,尼龙膜等。
五、实验材料
1、样品DNA;
2、DIG-DNA探针
六、实验操作
(一)Southern转移
1、将 PCR样品按下表混匀并点样,在1%琼脂糖凝胶中电泳1小时,取出凝胶。(来源菌株为pEGFP-N3,是老师提取质粒后PCR得到的GFP片段)

2、把凝胶浸在 0.25mol/L HCl中,室温轻轻晃动,直到溴酚蓝从蓝变黄。(解链)
3.将凝胶放入塑料盒中,在变性液(0.5mol/L NaOH,1.5mol/L NaCl)中,室温2×15分钟,轻轻晃动。(中和HCl)
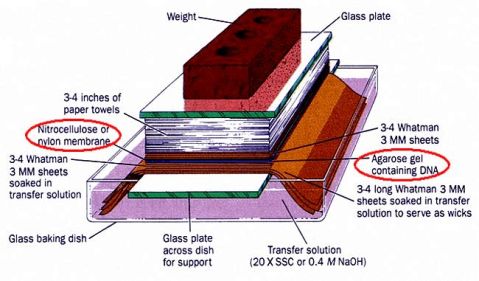
4.在塑料盒中换入转移液(3M NaCl,8mM NaOH,pH7.2),自下至上按照玻璃板、两层长滤纸条、三层小滤纸、凝胶(四周覆盖绝缘塑料膜)、比凝胶略大的尼龙杂交膜、三层小滤纸、10cm厚度的纸塔的顺序叠放转移系统,用胶条固定,水平静置过夜,完成转移。(小滤纸比凝胶略大;杂交膜不可用手触碰,盖在凝胶上后不可移动;纸塔起吸取液体的作用)
下图为转移示意图,实验中将玻璃盒换成塑料盒,将上层玻璃板及其上重物换成胶条,用力固定在塑料盒上。
5.取掉吸水纸塔,在滤膜上用铅笔标记电泳胶加样孔的位置,放在玻璃板上紫外交联数秒,使DNA牢固结合在膜上,即使在沸水中煮也不会脱离。(铅笔芯为惰性物质,不会影响实验结果)
(二)DNA探针的制备
反应物
dNTP(10mM) 左引物
右引物
Taq酶(5U/μl) MgCl2(25mM),10×Buffer
ddH2O
1.随机引物末端标记目的片段(Promega公司Primer-a-Gene Labeling system)。 注:
(1)每个标准反应可标记10ng-3μgDNA,要标记更多的DNA必须将所有的成分和体积放大。
(2)线性化的DNA应用酚/氯仿抽提并用乙醇沉淀,这样可以显著提高标记 效率。
(3)37℃下延伸保温时间(至20小时),可以提高DIG标记DNA的产量。
(4)用DIG-HighPrime标记的探针的长度为200-1000bp。
(三)DNA分子杂交
1、将适当体积(20ml/100cm2)的预热到杂交温度的预杂交缓冲液加入到有膜的杂交管中,预杂交 1-2小时。(利用缓冲液中其它DNA覆盖富含正电荷的杂交膜,为探针与目标片段的杂交提供便利)
2、将 DIG标记的探针(5-25ng/ml杂交液)在沸水中变性10分钟,在冰水上迅速冷却 10分钟。(解链) 体积/μl 0.5 1 1 0.5 3 12
4、倒去预杂交液,换上探针和缓冲液的混合物,温和摇动,保温至少2小时。(杂交时,探针与预杂交时覆盖的其它DNA竞争,探针的特异性更强,竞争力更大)
(四)杂交后洗膜:
1.在室温下用2×SSC,0.1%SDS双组分溶液洗,1次10分钟。
2.在室温下用0.1×SSC,0.1%SDS双组分溶液洗两次,每次15分钟,不停搅动。
(五)免疫检验
1、在 20ml阻断液(1×)中孵育30分钟。(即牛奶,起类似于预杂交液的覆盖作用)
2、在 10ml抗体液中孵育30分钟。(抗体与抗原特异性反应)
3、用 20ml洗涤液洗涤2×15分钟。(洗去杂交膜上多余的物质)
4、在 15ml检测缓冲液中平衡5分钟。
5、在避光条件下,于 10ml新鲜制备的显色底物液中反应显色。在显色过程中勿摇动。(显蓝褐色)
6、当点或带显色到合适的深度后,将湿膜照相记录。
七、实验结果

放大图:

八、注意事项
1.杂交温度不可太高,时间不宜过长;杂交温度应比杂交分子的解链温度低20-25℃,一般同源探针的杂交温度在 65℃,异源探针的杂交温度应适当调低,一般可在 50℃下进行杂交,如是不匹配程度较高的异源探针可以加入 50%甲酰胺在 42℃杂交。
2.洗膜的严紧性:应尽量控制洗膜的严禁性以降低背景,如用放射性标记应在洗膜的过程中密切检测放射性强度,以防过高的严紧度致使探针脱落。
3.杂交膜不立即进行杂交,可保鲜膜包被,放到密封的杂交袋中长期保存。
4.尼龙膜的再生(回收)
当用同位素标记时,可将膜至于煮沸的0.1×SSC/0.1%SDS溶液中5-10min,并用盖革计数器检测残留的放射强度为零,取出膜,滤纸吸干,用保鲜膜包好保存。
