物理化学实验报告
实验名称: 燃烧含的测定
一、实验目的
1、用氧弹式量热计测定萘的燃烧焓。
2、了解热量计中主要部分的作用,掌握氧弹量热计的实验技术。
二、实验原理
反应为理想气体则: Qp =Qv +△ nRT
△rHm = △rUm + RT∑Vb(g)
△U可表示为: △U = △cUb + △cU引燃丝 + △U量热计
MbQv.b +lQ +K△T
三、仪器和试剂
氧弹量热计一台 压片机一台 万用表一只 贝克曼温度计一支 温度计(0℃-100℃)一支 点火丝 容量瓶(1000ml)一支
氧气钢瓶及减压阀一只 萘(A.R.) 苯甲酸(A.R.)
四、实验步骤
1、热容量K的测定
(1)截取15cm引燃丝,将其中部绕成环状。
(2)称取苯甲酸约0.8-10g,压成片状,并放桌上敲击2次,去除没压紧的部分,再次称量。
(3)拧开氧弹盖放在专用支架上,引燃丝两端固定在两电极柱上,药片放于坩埚中,使引燃丝与药片表面接触,盖上氧弹盖。
(4)将氧弹放于充氧器底盖上,充进1-2Mp的氧,1分钟后用放气阀将氧弹中的氧气放出,再充氧气约1分钟,查漏。
(5)量取3000ml的水倒入内桶,氧弹放于内桶底座上,点火插头插在氧弹电极上,将贝克曼温度计的传感器竖直插入量热计盖上的孔中。打开电源,按“搅拌”。
(6)约5-10分钟后,开始初期的读数,隔半分钟读数一次,读第10次的同时按“点火”,仍半分钟读一次,直至两温差小于0.002℃时,再读数10次。
(7)停止搅拌,取出传感器,拔掉引火导线,取出氧弹并擦干外壳,用放气阀放掉氧气,打开氧弹盖,检查燃烧是否完全。取出引燃丝,量其剩余长度。
(8)洗净并擦干氧弹内外壁,将水倒入储水桶,擦干全部设备。等待设备和室温平衡做下一步实验。
2、萘的燃烧焓测定
称取萘0.6g左右,实验步骤同上。
五、数据记录与处理
室温:19.1℃ 大气压强:102.57KPa
5-1、苯甲酸燃烧的记录
苯甲酸的质量:0.8267 g 引燃丝初始长度:15.0cm
引燃丝剩余长度: 0 cm

5-2、萘燃烧的记录
萘的质量:0.6028 g 引燃丝初始长度:15.0cm
引燃丝剩余长度:0 cm
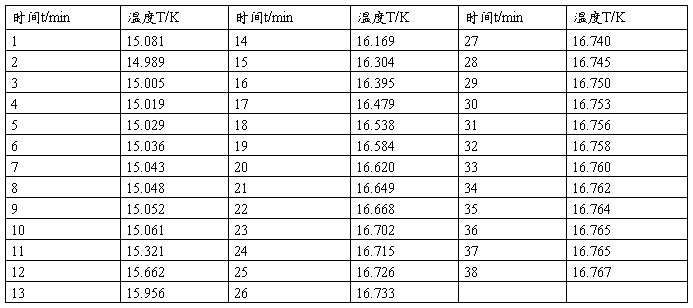
计算k的值:
△cHm(苯甲酸)= -3226.7kj/mol Ql = -6.699j/cm
△cUm(苯甲酸)=△cHm(苯甲酸)- △nRT=-3225.46KJ/mol
△T=15.54-14.18= 1.36K
K=-( mBQv,b+lQl)/ △ T=-(0.8267/122* (-3226.7)+(15*( -6.699)/1000)/1.36
=16.150k j/k
(2)计算萘的燃烧焓:
△T=16.66-15.09=1.57 K
Qv,B=-(lQl+K△T)/mB=-(15*( -6.699)/1000+16.150*1.57)/(0.6028/128)
=-5362.71kj/mol
Qp=Qv+△nRT=-5362.71-2*8.314*(19.1+273.15)/1000=-5367.56kj/mol
六、注意事项
1、压片时应不松不紧,以保证完全燃烧,且不会散开。
2、点火丝不要插到药片的小孔,以免燃烧时药品溶化,会影响点火质量。
3、如果实验失败应把氧弹从水桶中提出,排清里面的氧气才能重做。
4、往水桶内添水时,应注意避免把水溅到电极上。
七、思考与讨论
1、本次实验测得的萘的燃烧焓偏高,主要的误差在于药品称量时电子天平的读数,实验温度的读取,数据拟合时的读数等。
3、本实验中,哪些为体系?哪些为环境?系统和环境间有无热交换,如何矫正?答:氧弹内部空间为体系,氧弹以外为环境,实验过程中有热损耗,可增加氧弹壁的厚度来降低热损耗。
第二篇:物理化学实验报告-电池电动势的测定及其应用
电池电动势的测定及其应用
摘要: 在本实验中,我们利用对消法测量电池电动势并计算相关热力学常数。首先我们通
过测量电池Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) 的电动势,得到AgCl的溶度积Ksp,AgCl ;然后测量不同温度下Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) 的电动势,作E-T图拟合进而求该反应的热力学常数ΔrGm ,ΔrSm ,ΔrHm 。
关键词: 对消法 可逆电池 电动势
The Measurement and the Application of the Battery
Electromotive Force
Abstract: In this experiment, we measure the electromotive force of cells (Using
compensation method) and apply these results to calculate some related hermodynamic constants.Firsr,we determine EMF of cell Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) to get Ksp,AgCl ;Then we determine EMF of cell Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) in different temperature to get ΔrGm ,ΔrSm andΔrHm .
Key words: Compensation method, Reversible cell, Electromotive force (EMF),
第 1 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
1. 序言
化学电池由两个“半电池”组成,在电池反应过程中正极物质发生还原反应,负极物质发生氧化反应,电池反应是这两个电极反应的总和,其电动势为组成该电池的两个“半电池”电极电位的代数和。本实验采用对消法,以银-氯化银电极为参比电极,使测量回路中基本无电流通过,很大程度上减小了误差。
将化学反应设计成可逆电池,使测量电池电动势成为获得热力学常数的一种有力手段。而且电化学测量比一般的化学测量方法快速、精确、简便,因此电池电动势的测定对化学研究有着重要的意义。利用电化学方法测算物理化学参数的需要将所测反应设计成原电池,本
—实验设计Cu(s) | CuSO4(m1) || Cl(m2) | Ag(s),AgCl(s) 可逆电池,用于求标准铜电极电动势
E°Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) 可逆电池,用于求AgCl的溶度积常数 ,(Cu2+/Cu) ;
以及反应的热力学常数ΔrGm 、ΔrSm 、ΔrHm 。
2. 实验部分
2.1 实验仪器
UJ25型高电势直流电位差计 上海精密科学仪器有限公司
501型超级恒温器 上海市实验仪器厂
2010双通道色谱工作站
标准电池,银-氯化银参比电极
移液管,容量瓶,半电池管,KCl盐桥
铂电极,铜电极,电阻箱,电流计
0.1mol /L AgNO3溶液(电镀液)
0.1mol /L CuSO4溶液(电镀液)
0.1000mol /L AgNO3 & 0.1mol /L HNO3溶液
0.1000mol /L CuSO4溶液
2.2 实验步骤
1)制备银电极:将浸泡于浓硝酸中的铂电极取出用蒸馏水冲洗,再用细晶相砂纸打磨光亮,用蒸馏水冲洗干净后插入盛0.1mol /L AgNO3溶液的烧杯中,按Figure 1.接好线路,调节可变电阻,使电流在3mA、电压在6V电镀Ag 20min 。取出,用0.1 mol /L 的HNO3溶液冲洗,用滤纸吸干迅速放入盛有0.1000mol /L AgNO3 + 0.1 mol /L HNO3溶液的半电池管中。
2)制备铜电极:将两支铜电极在稀硫酸中浸洗,用蒸馏水冲洗,再用细晶相砂纸打磨光亮,用蒸馏水冲洗干净后插入盛有镀铜溶液的烧杯中,控制电流在3mA、电压在6V电镀Cu 20min 。取出后用蒸馏水冲洗,放入实验用的CuSO4溶液中。
3)将参比电极与铜电极组合成电池,在室温条件下选用CuSO4溶液与铜丝组成原电池,测量其电动势。
4)在室温条件下,测量银电极与参比电极组成的原电池的电动势,计算Ksp,AgCl。
第 2 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
5)连续将恒温增加在5~7℃左右,测量银电极与参比电极组成的原电池的电动势。由所得数据计算该电池反应的ΔrGm , ΔrSm , ΔrHm 并进行误差计算。
2.3 注意事项
1) 连接线路时,切勿将标准电池、工作电源、待测电池的正负极接错;
2) 应先将半电池管中的溶液先恒温后,再测定电动势;
3) 使用检流计时,按按钮的时间要短,以防止过多的电量通过标准电池或被测电池,造成严重的极化现象,破坏被测电池的可逆状态。
3. 结果与讨论
3.1 实验结果
铜电极和参比电极电动势E1=0.095528V,相对误差为82.0%;
电极和参比电极电动势E2=0.095528V,相对误差为5.5%;
AgCl的溶解Ksp(AgCl)= 6.6*10-11,相对误差为63.3%;
ΔrG?m= -50.59 kJ/mol ,相对误差为9.11%;
ΔrS?m= -25.30 J/(mol·K) ,相对误差为23.9%;
ΔrH?m= -58.17 kJ/mol ,相对误差为11.2%。
3.2 误差分析
1)仪器的不稳定带来较大误差:
调节电桥平衡的操作时间应尽可能的短,否则电极上较长时间的有电流通过,会发生电池反应使得溶液浓度下降、电极表面极化,这样可逆电极变成不可逆的,会给实验带来较大误差。而实验中所用仪器不稳定,需要较长的时间才能大致调节到平衡,即使是同一个电动势值,在很短的时间内测得的数据都有较大波动,所以不能很快调节到平衡是实验的误差主要来源。
2)电流无限小的情况下测量,才能达到可逆电池的要求,但在实验过程中电流无法达到无限小仍存在一定值的电流,于是产生的极化作用破坏了电池的可逆性,使电动势偏离可逆值。
3)对E ~ T曲线作线性拟合可能不合适:
Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) 的Nernst方程:
KspRTRTaAg?aCl-E?0?ln?lnFaAg?aCl-FKsp
R?E?[lnF
??Ag??cAg???Ksp?Cl??cCl? ]?T其中?Ag? ,?Cl? ,Ksp 项显然会随温度T改变,因此对E ~ T曲线作线性拟合可能并不合适。
第 3 页 共 7 页 物理化学实验NO.8 PB07007303 王璐 ?
4)恒温槽温度存在波动,电镀不均匀,会造成不稳定,此外实验中采用盐桥来消除液接电位,但实际实验中不能保证盐桥能够完全消除液接电位。
3.3 讨论与思考
本次实验是对物化中电池电动势相关知识的一个复习,通过实验我了解了电池电动势的测量方法以及热力学常数的测定原理。这是一个综合性很强的实验,在实验操作过程中我知道了如何制作盐桥、如何用对消法测定电池的电动势,并熟悉了标准电池、可逆电池、电位差计、检流计等仪器的使用方法,可谓收获颇丰。
参考文献:
[1] 崔献英,柯燕雄,单绍纯.物理化学实验[M].中国科技大学出版社,2000: 29~32.
[2] 付献彩,沈文霞,姚天扬,侯文华.《物理化学》(第五版)上册[M].南京大学化学化工学院,高等教育出版社,2005.
附件:实验数据处理
1. 数据记录
饱和标准电池电动势:1.01864V(20℃)
—Cu(s) | CuSO4(m1) || Cl(m2) | Ag(s),AgCl(s) 部分:
Table A1.
水浴温度 E (V)
(℃) 1 2 3
26.15 0.095900 0.095170 0.095514
Ag(s),AgCl(s) | KCl(m1) || AgNO3(m2) | Ag(s) 部分:
Table A2. 平均 0.095528
水浴温度
(℃) 26.15
34.50
40.15
46.45
E (V) 1 0.524193 0.523871 0.521913 0.519122 2 0.524092 0.523421 0.522133 0.518812 3 0.524581 0.523221 0.521401 0.518732 平均 0.524289 0.523504 0.521816 0.518889
2. 数据处理
2.1 铜电极和参比电极电动势理论值的计算
-电池:Cu│CuSO4(0.1000m)║Cl(1.000mKCl)│AgCl-Ag
各电极电位为:
?右???Ag?,AgClRTaAgCl??ln2??Ag2FaCl?,AgCl?RT1ln2 2FaCl-
第 4 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
?? 左??Cu2?,Cu?RTaCu2?RT?ln??Cu?lnaCu2?2?,Cu2FaCu2F
E?E??
已知:?Ag?RT1 ln22FaCl-aCu2??=0.22233V,=0.3419V,aCu2?=0.0150,aCl?=0.606 ?,AgClZn2?,Zn
理论电动势E=0.3419- 0.22233-8.314*(273.15+26.15)/(2*96485)ln(1/0.015/0.6062)=0.052496V 实验测得电动势Ea=0.095528V
相对误差为(0.095528-0.052496)/ 0.052496=82.0%
2.2银电极和参比电极电动势理论值的计算
-电池:Ag│AgNO3(0.1000m)║Cl(1.000mKCl)│AgCl-Ag
-负极反应:Ag(s)+Cl(1.000m) ? AgCl(s)+e-
+正极反应:Ag(0.1000m)+e- ? Ag(s)
E=[?Ag?/Ag?
??RT1RTRT1?= lnaAg?]?[?Ag?ln]E??ln/AgClFaAg?aCl?FFaCl??已知:?Ag,AgCl=0.22233V,?Ag?,Ag=0.7996V,aAg?=0.0734,aCl?=0.606
理论电动势E=0.7996-0.22233-(273.15+26.15)/96485*ln(1/0.0734/0.606)=0.496992V
实验测得电动势Ea=0.524289V
相对误差为(0.524289-0.496992)/ 0.496992=5.5%
2.3计算 AgCl的Ksp
E?RT1RTln?lnaAg??aCl? FKspF
RTaAg??aCl?RT??Ag??CAg????Cl??CCl?ln?ln(C?)?2 =FKspFKsp
CAgNO3 = 0.1000 mol/L,γ±Ag+ = 0.734,CKCl = 1.000 mol/L,γ±Cl- = 0.606
Ksp(AgCl)=0.734*0.1*0.606/exp(0.524289*96485/8.314/299.3)=6.6*10-11
pKsp,AgCl = 10.18
文献的Ksp(AgCl)=1.8*10-10
相对误差为(1.8*10-10-6.6*10-11)/ 1.8*10-10=63.3%
2.4 计算银电极与参比电极组成的电池电动势相关热力学数据及误差
Table A3.
水浴温度
(℃)
26.15 E/V 0.524289 T/K 299.30
第 5 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
34.50
40.15
46.45 0.523504 0.521816 0.518889 307.65 313.30 319.60
Fig A1.温度T与电池电动势E的线性拟合曲线
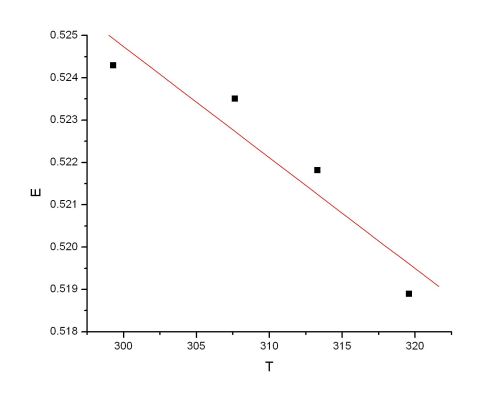
Y = A + B * X
Parameter Value Error
------------------------------------------------------------
A 0.60339 0.0198
B -2.62179E-4 6.38595E-5
------------------------------------------------------------ R SD N P
------------------------------------------------------------ -0.94548 9.53748E-4 4 0.05452
------------------------------------------------------------ ?E)p=-2.62179×10-4 故(?T
???G???E??rSm???rm??nF????T?P ??T?P
?rGm??nFE
第 6 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
??E??rHm??nFE?nFT????T?P
n=1,F = 96487 C/mol,E=0.524289V
得:
ΔrGm =-1×96500×0.524289=-50.59kJ/mol
-ΔrSm =1×96500×(-2.62179×104)= -25.30J/(mol?K)
-ΔrHm =-50593 + 1×96500×299.30× (-2.62179×104) =-58.17 kJ/mol
查参考文献得Ag+(aq)、Cl-(aq)、AgCl(c) 各自的的标准生成焓变ΔfH?m、标准生成自由能变ΔfG?m及标准熵S?m,由此计算出电池反应的ΔfH?m、ΔfG?m、ΔfS?m如下所示.
Table A4. Ag+(aq)、Cl-(aq)、AgCl(c) 的ΔfH?m、ΔfG?m及S?m
Ag+(aq)
Cl—(aq)
AgCl(c)
电池反应
Δ
Δ
Δ
Δ
Δ
Δ
ΔfH?m 105.90 -167.44 -127.03 -65.49 ΔfG?m 77.11 -131.17 -109.72 -55.66 S?m 73.93 55.20 96.11 -33.02 rG?m= -55.66 kJ/mol rS?m= -33.02 J/(mol·K) rH?m= -65.49 kJ/mol (33.2-25.30)/ 33.02 = 23.9% 。 rS?m 相对误差:(55.66-50.59)/ 55.66 = 9.11% 。 rG?m 相对误差:(65.49-58.17)/ 65.49 = 11.2% 。 rH?m 相对误差:
第 7 页 共 7 页 物理化学实验NO.8 PB07007303 王璐
