物理化学实验报告
院系 XX学院
班级 XX系XX班
学号 XXXXXXXX
姓名 XXX
实验一 计算机联用测定无机盐溶解热
日期 2012/X/X 同组者姓名 XX XXX
成绩
一、 实验目的
(1) 用量热计测定KNO3的积分溶解热。
(2) 掌握量热实验中温差校正方法以及与计算机联用测量溶解过程动态曲线的方法。
二、 实验原理
盐类的溶解过程通常包含着两个同时进行的过程:晶格的破坏和离子的溶剂化。前者为吸热过程,后者为放热过程。溶解热是这两种热效应的总和。因此,盐溶解过程最终是吸热或放热,是由这两个热效应的相对大小决定的。常用的积分溶解热是指等温等压下,将1摩尔溶质溶解于一定量溶剂中形成一定浓度溶液的热效应。溶解热的测定可以在具有良好绝热层的量热计中进行的。在恒压条件下,由于量热计为绝热系统,溶解过程所吸收的热或放出的热全部由系统温度的变化放映出来。为求溶解过程的热效应,进而求得积分溶解热(即焓变△H),可以根据盖斯定律将实际溶解过程设计成两步进行,如图2-1.

△H
 △H
1=0
△H
1=0
 绝热
绝热

由图2-1可知,恒压下焓变△H为两个过程焓变△H1和△H2之和,即:
△H=△H1+△H2 (2-1)
因为,量热计为绝热系统,Qp=△H1
所以,在t1温度下溶解的恒压热效应△H为:
△H=△H2=K(t1-t2)=-K(t2-t1) (2-2)
式中K是量热计与KNO3水溶液所组成的系统的总热容量,(t2-t1)为KNO3溶解前后系统温度的变化值△t溶解。
设将质量为m的KNO3溶解于一定体积的水中,KNO3的摩尔质量为M,则在此浓度下KNO3的积分溶解热为:
△solHm=△HM/m=-KM/m·△t溶解 (2-3)
K值可由电热法求取。即在同一实验中用电加热提供一定的热量Q,测得温升为△t加热,则K·△t加热=Q。若加热电压为U,通过电热丝的电流强度为I,通电时间为τ则:
K·△t加热=IUτ(2-4)
所以K =IUτ/△t加热 (2-5)
由于实验中搅拌操作提供了一定热量,而且系统也并不是严格绝热的,因此在盐溶解的过程或电加热过程中都会引入微小的额外温差。为了消除这些影响,真实的△t溶解与△t加热应用图2-2所示的外推法求取。图2-2表示电加热过程的温度-时间(t-τ)曲线。AB线和CD线的斜率分别表示在电加热前后因搅拌和散热等热交换而引起的温度变化速率。tB和tC分别为通电开始时温度和通电后的直线段的最初温度。真实的△t加热必须在tB和tC间进行校正,去掉由于搅拌和散热等所引起的温度变化值。为简便起见,设加热集中在加热前后的平均温度tE(即tB和tC的中点)下瞬间完成,在tE前后由于搅拌或散热而引起的温度变化率即为AB线和CD线的斜率。所以将AB、CD直线分别外推到与tE对应的时间的垂直线上,得到G、H两交点。显然GN与pH所对应的温度差即为tE前后因搅拌和散热所引起的温度变化的校正值。真实的△t加热应为H与G两点所对应的温度tH与tG之差。
三、 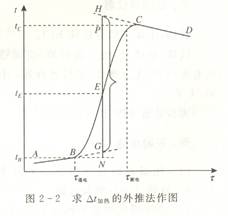 试剂与仪器
试剂与仪器
试剂:干燥过的分析纯KNO3。
仪器:量热计,磁力搅拌器,直流稳压电源,半导体温度计,信号处理器,电脑,天平。
四、 实验步骤
1用量筒量取100mL去离子水,倒入量热计中并测量水温。
2在干燥的试管中称取2.7~2.9g干燥过的KNO3(精确到±0.01g)。
3先打开信号处理器、直流稳压器,再打开电脑。自动进入实验测试软件,在“项目管理”中点击“打开项目”,选择“溶解热测定”,再点击“打开项目”,输入自己学号和称取的样品重量。
4系统提示装入试样的后,立即装入待测试样;
5等待测试结果,注意数据变化。测试完毕,系统自动保存。读取
五、数据处理
(1)作盐溶解过程和电加热过程温度一时间图,用外推法求得真实的△t溶解与△t加热。
图如下。
解:外推法求得△t溶解=1.873℃ △t加热=2.047℃ 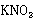 质量:2.82g
质量:2.82g
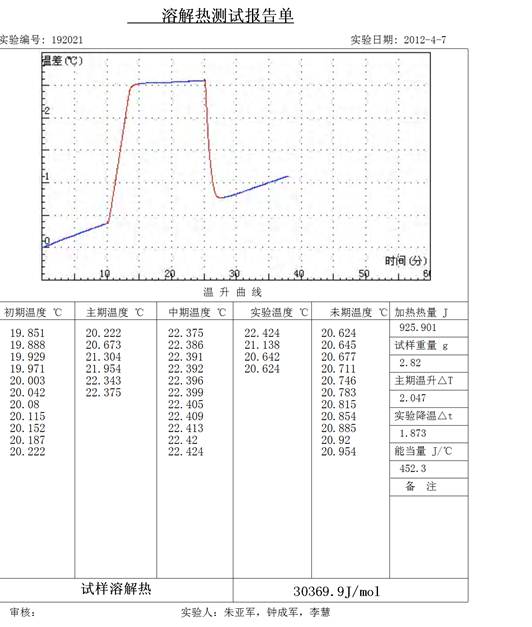
(2)按式(2-5)计算系统总热容量K。
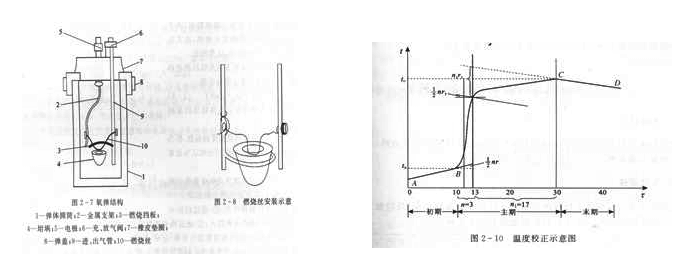
解: K=UIT/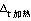 =925.901J/2.047℃=452.32J/℃
=925.901J/2.047℃=452.32J/℃
(3)按式(2-3)计算KNO3的积分溶解热△solHm?
解:△solHm=△HM/m=-KM/m·△t溶解=452.32*101/(2.82*1.873)=8649.29 J/mol
六、思考题
(1)溶解热与哪些因素有关?本实验求得的KNO3溶解热所对应的温度如何
确定?是否为溶解前后系统温度的平均值?
答:与溶质,溶剂,溶解温度及浓度有关,本实验中对应的溶解温度即盐溶解前的水温。
(2)为什么要用作图法求得△t溶解与△t加热?如何求得?
答:由于实验搅拌操作中提供了一些热量,而且系统也不是严格绝热的,因此在盐溶解的过程或电加热的过程中都会引入微小的额外温差,为了消除影响,真实的△t溶解与△t加热应用上图2-2外推法求得。
(3)本实验如何测定系统的总热容量K?若用先加热后加盐的方法是否可以?
答:用电热法测定系统总热容量K;不可以,因为要求的是量热计与盐溶液的热容量,而不是盐和水的热容量。
(4)在标定系统热容过程中,如果加热电压过大或加热时间过长,是否会影响实验结果的准确性?为什么?
答:不会;H是状态量,与过程无关。
实验二 有机物燃烧热测定
日期 2012/4/7 同组者姓名 XX XXX
成绩
一、实验目的
(1)用氧弹式量热计测定奈的恒容燃烧热。
(2)掌握氧弹式量热计的构造、原理和使用方法。
(3)掌握有关热化学实验中总热容量标定与温差校正的方法。
二、实验原理
物质的燃烧热是指1摩尔物质在氧气中完全燃烧时释放出的热量。若燃烧在恒容下进行称恒容燃烧热(Qv),在恒压下进行称恒压燃烧热(Qp)。用氧弹式量热计测得的燃烧热是恒容燃烧热,Qv= -CM△t/m,式中,△t=t2-t1是燃烧前后系统温度的变化;m、M分别是被测物质的质量与摩尔质量,C是系统的总热容。加负号是因为燃烧是一个放热过程,物质的燃烧热为负值。应该指出,由于实验装置难以做到完全绝热,故实际测定时,需对测得的上△t作校正。实际使用中更多的是恒压燃烧热Qp,Qp可用式Qp=Qv+△nRT方便地求得。式中△n为燃烧前后气体物质的量的变化。物质的燃烧热是温度的函数,但当温度变化不是很大时,可近似认为是常数。本实验采用数显式氧弹量热计测量燃烧热,它通过控制双向可控硅自动点火和熄火;通过测量控制接口对燃烧初期、主期、末期(其含义见数据处理部分)的温度进行采集、记录、打印。经过数据处理得到初期温度变化率r、末期温度变化率r1以及温度校正值△t’,并得到实验的最后结果,这些数据也能通过打印机打印出来。
三、试剂与仪器
试剂:苯甲酸、萘、镍铬丝、氧气等;仪器:HR-15数显氧弹式量热计。
图2-5和图2-7分别是氧弹式量热计和氧弹的结构简图。
四、实验步骤
1.用标准苯甲酸标定量热计的热容量C
(1)截取10cm镍铬丝,将其两端分别接在氧弹内的两个电极上。
(2)将预先压成片状干燥的苯甲酸样品(1g左右)放人坩埚内,然后将坩埚放在氧弹金属支架的环上,如图2-7所示。注意镍铬丝应与样品尽量接近,但切不可触及坩埚。
(3)拧紧氧弹盖及放气孔,接上充氧器,往氧弹中缓缓充人氧气,充氧时间不少于30 S,直到氧弹内压力到达2.5~3 MPa。完成后将氧弹浸没在水中,检查是否漏气。
(4)往内筒中加人4000ml去离子水,调节内筒水温,使内筒水温比外筒水温低0.7℃~1.0℃.将内筒平稳地放在外筒的绝缘架上。
(5)把氧弹放人内筒的固定座上(注意每次实验应保持相同位置)。然后接上点火电极插头,观察面板上点火指示灯应微亮,否则表示点火线未接通。盖上筒盖,点火线应压在筒盖边缘的线槽内。插入温度传感器。开动搅拌器,面板搅拌指示灯亮。
(6)打开电脑,HR-15型氧弹式量热计测试软件,进行测试内容设置。设置方法为:(1)选择实验内容 “热容测定”,并输入苯甲酸标准燃烧热发热量值26480.5(26446),输入试样编号及试样重量。
(7)然后点击“开始”键进行实验测量。实验分三个阶段:初期、主期、末期。注意记录温度的变化,值得注意的是,点火成功,主期温度明显升高,否则,点火不成功。
(8)测量完毕,停止搅拌,取出温度传感器插人外简内,打开筒盖,拔下点火电极插头,取出氧弹,用放气帽按下放气阀,使气体缓缓放出至常压。
(9)实验完毕,氧弹筒体及所有的内件必须冲洗干净,并且用干毛巾擦干。
2.测定萘的恒容燃烧热
(1)将预先压好片的试样品放入坩埚,准确称量(0.7g 左右)(精确到士0.00029)。按上述热容量C的测定完成实验步骤(1)~(8)。
(2)键盘操作:
①输人样品质量(g)。
②输人仪器热容量C,进行测试内容设置。设置方法为:选择实验内容 “发热量测定”。
五、数据处理
前已述及,恒容燃烧热Qv= -CM△t/m。但这个计算式没有考虑以下各项的影响:系统与环境间的热交换、生成HNO3。水溶液的热量和燃烧丝燃烧放出的热量。因此,精确的计算应用下式:
Qv=[-C(tn-t0+△t’)-gb-(-5.98) VOH-]×M/m
式中tn为主期的最高温度,t0为主期的最初温度,g为燃烧丝的燃烧热(镍铬丝为-1400 J·g-1),b为燃烧掉的燃烧丝质量,VOH-为滴定洗弹液所消耗的0.lmol·L-1NaOH溶液体积(mL),-5.98为相当于被 lmL 0.lmol·L NaOH溶液所中和的HNO3水溶液的生成热(J·mL),△t’为由于系统与环境热交换引起温差的校正值,由下式计算:
△t’=-0.5(r+r1)n- r1n1
式中r为初期温度变化率(以初期结束温度减去初期开始温度所得温差除以初期时间间隔数),r1为末期温度变化率(以末期结束温度减去末期开始温度所得温差除以末期时间间隔数),n为主期内每半分钟温度上升不小于0.3℃的时间间隔数(点火后的第一个时间间隔不管温度升高多少,都计入n中),nl为主期内每半分钟温度升高小于0.3℃的时间间隔数。
关于系统温升△t的校正可参照图2-10温度-时间(t-τ)曲线加以说明。由图中可知,主期时间间隔数为20,其中n为3,n1为17。这两部分分别称为温度跃升区和高温区。在高温区,即n1部分,温升平稳。因为此时系统温度已高于环境温度,系统散热是主要的,其温度变化率由CD线的斜率r1决定,所以由散热引起温度变化为n1r1。而在温度跃升区,即n部分,由开始低于环境温度到后来高于环境温度。因此这个区域包括了开始吸热及后来散热的综合影响,引起系统的温度变化可以看作由两部分造成,即 nr/2和 nr1/2,所以整个主期由于热交换引起的温度变化为以上两个区域的综合。
按式(2-7)、式(2-8)和式(2-9)计算下列内容:
(1) 已知苯甲酸的恒容燃烧热为-26446 J·g-1,计算本实验量热计的总热容量C。
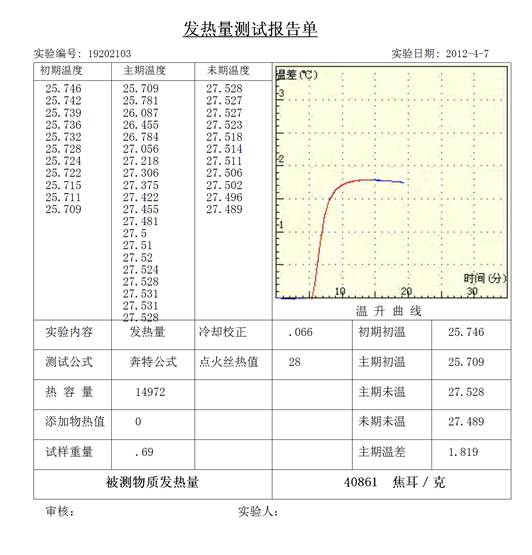
解:由下图可知n=3,n1=18,r =0.048/10,r1=0.034/10;
Qv=[-C(tn-t0+△t’)-gb-(-5.98)Voh]*M/m
并且tn=26.443, t0=24.565, △t’=0.0735 Qv=-26446 J·g-1
由上式得:C=15579J/mol
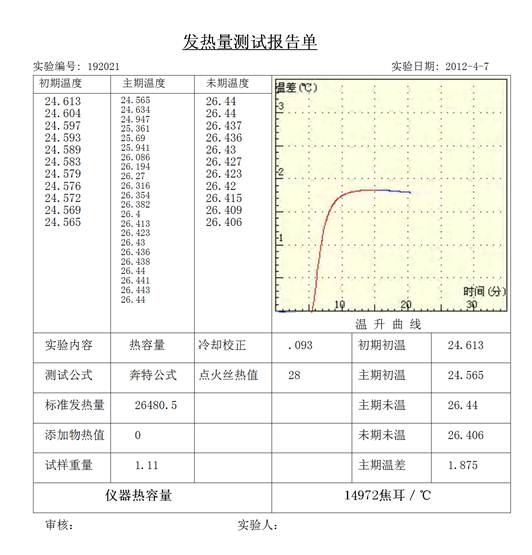
(2) 计算萘的恒容燃烧热Qv和恒压燃烧热Qp.
(3)  =346.6KJ/mol
=346.6KJ/mol
(4)  =513.56KJ/mol
=513.56KJ/mol
六、思 考 题
(1)为什么量热计中内筒的水温应调节得略低于外筒的水温?
答:保持环境温度
(5) 在标定热容量和测定条燃烧热时,量热计内筒的水量是否可以改变?为什么?
答:不可以,水当量的求法是用已知燃烧热的物质(本实验中用苯甲酸)放在量热器中燃烧,测其始终态温度,一般来说对不同样品,只要每次水量相同,水当量就是定值。
(3)为什么在数据处理时要计算温度校正值上△t’?怎样计算?
答:由于实验装置难以做到完全绝热,由下式公式: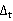 =-0.5(
=-0.5(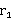 +r)n-
+r)n-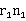 得出(r初期温度变化率,
得出(r初期温度变化率,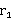 末期温度变化率,n为主期内半分钟上升不小于0.3℃时间间隔
末期温度变化率,n为主期内半分钟上升不小于0.3℃时间间隔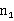 为主期内半分钟上升小于0.3℃时间间隔数。
为主期内半分钟上升小于0.3℃时间间隔数。
实验三 差热分析
日期 2012/4/7 同组者姓名 XXX XX
成绩
一、 实验目的
了解热分析的基本原理及差热曲线的分析方法,测定CuSO4·5H2O脱水过程的差热曲线及各特征温度;测定KNO3的晶型转变过程的热效应。
二、 实验原理
(1)热分析是在程序控制温度下测量物质的物理性质与温度的关系的一类技术。差热分析(D.T.A)是热分析方法的一种。其根据是当物质发生化学变化或物理变化(如脱水、晶型转变、热分解等)时,都有其特征的温度,并往往伴随着热效应,从而造成研究物质与周围环境的温差。此温差及相应的特征温度,可用以鉴定物质或研究其有关的物理化学性质。
为对其待测样品进行差热分析,则将其与热稳定性良好的参考物一同置于温度均匀的电炉中以一定的速率升温。这种参考物如SiO2、Al2O3,它们在整个实验温度范围内不发生任何物理化学变化,因而不产生任何热效应。所以,当样品没有热效应产生时,它和参考物温度相同,两者的温差△T=0;当样品产生吸热(或放热)效应时,由于传热速率的限制,就会使样品与参考物温度不一样,即两者的温差△T≠0。若以温差△T对参考物温度T作图,可得差热曲线图(如图2-15所示)。当△T=0时是一条水平线(基线);当样品放热时,出现峰状曲线,吸热时则出现方向相反的峰状曲线。热效应结束后温差消失,又重新出现水平线。这些峰的起始温度与物质的热性质有关。峰状曲线与基线围起来的面积大小则对应于过程热效应的大小。
差热峰的面积与过程的热效应成正比,即:
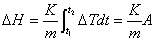
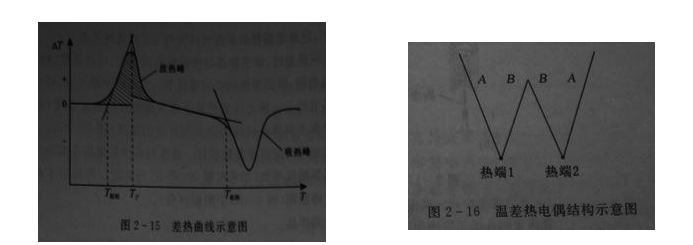
式中m为样品的质量;△T为温差;t1,t2为峰的起始时刻与终止时刻;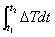 为差热峰的面积A。K为仪器参数,与仪器特征及测定条件有关。同一仪器测定条件相同时K为常数,所以可用标定法求得。即用一定量已知热效应的标准物质,在相同的实验条件下测得其差热峰的面积,由式(2-20)求得K值。本实验用已知熔化焓的Sn(△Hm=60.67J.g-1).峰面积可用图解积分法计算或直接用求积仪求得。
为差热峰的面积A。K为仪器参数,与仪器特征及测定条件有关。同一仪器测定条件相同时K为常数,所以可用标定法求得。即用一定量已知热效应的标准物质,在相同的实验条件下测得其差热峰的面积,由式(2-20)求得K值。本实验用已知熔化焓的Sn(△Hm=60.67J.g-1).峰面积可用图解积分法计算或直接用求积仪求得。
(2)温差△T的测量,是用两对相同型号的热电偶同极串联组成一个温差热电偶,如图2-16所示,其中A、B表示组成热电偶的两种不同金属材料。实验时,将其中一热端插入装有参考物的样品管中,将另一热端插入装有样品的样品管中,引出的两端接在自动记录仪(或电位差计)上。当两端温度相同时,由于两对热电偶热电势方向相反、大小相等,所以输出电势为零,记录仪的记录笔走在基线上。在样品产生热效应时,两管中出现温差而产生电势差,使记录笔发生偏转。在实验的温度变化范围有限的情况下,记录笔偏移的距离可认为与△T呈线形关系。
(3)在实际测量时,由于样品与参比物的比热容、导热系数、粒度、装填情况等不可能完全相同,因而差热曲线的基线不一定与时间轴平行,峰前后基线也不一定在同一条直线上。因此峰起始温度通常是指外推起始温度,即以基线延长线与峰的前沿最大斜率点切线的交点所对应的温度如图(2-15)。实践证明,用外推法确定的此特征温度重复性较好。温度的具体数值应在实验条件下用国际热分析协会推荐的标准物(如苯甲酸、Sn等)进行标定。在确定了峰的起点和终点后。再确定峰面积(图2-15中阴影部分)。
三、 试剂与仪器
试剂:CuSO4·5H2O,参考物Al2O3,标准物Sn。
仪器:热分析电炉,CKW-1000系列温度控制仪,XWT系列台式自动平衡双笔记录仪。
实验步骤
(1)熟悉综合热分析仪的基本结构和操作使用方法,熟悉操作软件的使用方法。
(2)根据教师指定的实验样品,设计控温程序,包括开始温度、升温速率、终止温度、保温时间、气体流速等。
(3)按照设计的控温程序运行控温程序,对样品进行热分析操作,实时采集数据。在微机上观察有关参数及绘出的曲线。
(4)控温程序结束后,让加热炉降温。处理数据,打印图谱和有关数据。
四、 数据处理
(1) 记录实验条件,用外推法从各差热曲线上确定起始反应温度。
实验四 热重分析实验
日期 2012/4/7 同组者姓名 XX XXX
成绩
一、 实验目的
了解热重分析的基本原理及热重曲线的分析方法,测绘NaHCO3、BaCl2·2H2O的脱水热谱图并予以定量解释。
二、 实验原理
热重法(TG)是在程序控制温度的条件下测量物质的质量与温度的关系的一种技术。当样品在程序升温过程中发生脱水、氧化或分解时,其质量就会发生相应的变化。通过热电偶和热天平,记录样品在程序升温过程中的温度t和与之相对应的质量m,并将此对应关系绘制成图,即得到该物质的热重谱线图(图2-29)。
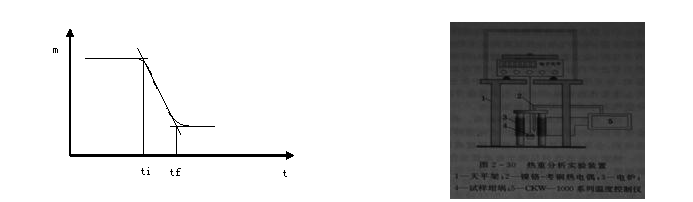
图2-29 热重谱线示意图
在理想的实验情况下.图中ti应该是样品的质量变化达到天平开始感应的最初温度.同样tf是样品质量变化达到最大值时的温度。图线的形状、ti和tf的值主要由物质的性质所决定.但也与设备及操作条件(如升温速率等)有关。在实验中由于样品的预处理状况、热分析炉的结构、炉内外气氛对流等因素的影响.ti、tf往往不易确定.故采用如图2-29所示外排法得到。根据质量变化的百分率及相应温度,可以得到物质在一定温度区间内反应特性以及热稳定性等信息.以至于可推测其组成等。因此,热重法与差热分析一样,也是热分析的有力工具之一。
本实验分别测试NaHCO3、BaCl2·2H2O在加热过程中发生分解反应时质量的变化,测求其分解反应温度和两个脱水温度并验证如下反应步骤:
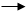 NaHCO3 Na2CO3+ CO2+ H2O
NaHCO3 Na2CO3+ CO2+ H2O
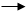 BaCl2·2H2O BaCl2·H2O+ H2O
BaCl2·2H2O BaCl2·H2O+ H2O
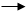 BaCl2·H2O BaCl2+H2O
BaCl2·H2O BaCl2+H2O
需要注意的是,热重谱图上的温度应该用国际热分析协会推荐的标准物质相变温度进行标定。
三、 试剂与仪器
试剂:BaCl2·2H2O(AR),NaHCO3(AR)。
仪器:电子天平(精度0.1mg),热分析炉,CKW-1000系列温度控制仪。仪器组装如图2-30所示。
四、 实验步骤
(1)如图2-30装好设备,在天平右臂挂好坩埚,调节天平到平衡位置,并记下读数。
(2)取下空坩埚,称取0.15g左右的NaHCO3放在其中,轻轻振动,使之自然堆积。然后将坩埚仍挂回天平右臂上,使其垂直地置于电炉的恒温区域之中。
(3)把测温热电偶插入电炉,热电偶的热端应尽量接近坩埚,并接好温度控制仪。
(4)设置好控制程序,控制温度升高速度为每分钟3度。
(5)每隔1度记录天平的读数与相应温度,直到200度为止。
(6)按上述步骤测量BaCl2·2H2O的两次脱水温度与失重量。
五、 数据处理
(1)记录实验条件,列表记录测定数据(测得的温度应考虑用标准物质草酸分解温度118度进行标定后的温度校正值)。
(2)以天平读数为纵坐标、温度为横坐标分别作NaHCO3、BaCl2·2H2O的失重热谱图。
(3)用外推法求出NaHCO3的分解反应以及BaCl2·2H2O的两次脱水的起始温度ti和结束温度tf.
(4)试将BaCl2·2H2O两次失重的量与化学反应式中的计量关系相验证。
六、 思考题
(1) 热重分析中升温速率过快或过慢对实验有什么影响?
答:升温速率是对热重分析(TG)曲线影响最大的因素。
升温速率越大,测试测得的温度滞后现象越严重,起始失重温度和终止温度测定值变得越高,分解温度范围也会变得更宽。对于对分解失重不太敏感的样品的TG测试,如果升温速率太快,样品来不及作出充分响应,失重台阶就会测不准或测不出。
热重分析中升温速率缓慢能够使实验的温度记录更准确。但会使某些化学反应或物理变化的反应速率也变得缓慢,导致出现失重台阶钝化,从而又影响到解析时读取失重温度和失重量的准确读值。
再过分缓慢,其实也没有必要,过分缓慢增加了许多倍的测试占机时间、也就增加了测试成本、增加了测试费用!
(2) 简述热重分析的特点及局限性。
答:特点,是样品处于程序控制的温度下,观察样品质量随温度或时间的函数,从而得出物质在一定温度区间内的反应特性以及热稳定等信息。局限性,测量过程中由于有可能进行多个反应,还是有些不准确。
实验五 溶液表面张力测定
日期 2012/4/7 同组者姓名 XX XXX
成绩
一、实验目的
(1) 掌握气泡的最大压力法测定溶液表面张力原理和技术。
(2) 测定不同浓度正丁醇水溶液的表面张力,计算表面吸附量。
二、实验原理
处于液体表面的分子由于受到液体内部分子与表面层外介质分子的不平衡的作用,具有表面张力。定义单位长度上沿着表面的切线方向垂直作用于表面的收缩力为表面张力δ,单位N·M-1。气泡的最大压力法(或最大泡压法)是测定液体表面张力的方法之一。它的基本原理如下:当玻璃毛细管一端与液体接触,并往毛细管内加压时,可以在液体的毛细管口处形成气泡。设气泡在形成过程中始终保持球形,则气泡内外的压力差Δp(即施加于气泡的附加压力)与气泡的半径r、液体表面张力δ之间的关系可由拉普拉斯(Laplace)公式表示,即△p=2δ/r。显然,在气泡形成过程中,气泡半径由大变小,再由小变大;而压力差Δp则由小变大,然后再由大变小。当气泡半径r等于毛细管半径R时,压力差达到最大值Δpmax,因此Δpmax=2δ/R。由此可见,通过测定R和Δpmax,即可求得液体的表面张力。
本实验中用数字式微压差测量计测量压力差Δp。
在同一温度下,如测定不同浓度c的溶液表面张力,按吉布斯(Gibbs)吸附等温式可计算溶质在单位界面过剩量,即吸附量。
三、仪器与试剂
仪器:表面张力测定实验装置,。
试剂:正丁醇溶液(0.20mol·L-1、0.40 mol.L-1、0.60 mol·L-1、0.80 mol·L-1)。
四、实验步骤
(1)通过活塞调节水滴滴入增压瓶中的速度,使气泡从毛细管口逸出,速度控制在每分钟5~15个。记录微压差仪读数,得Δpmax。(要求至少测定三次,然后取平均值。)
(3)同上测定0.20mol.L-1,0.40 mol.L-1,0.60 mol.L-1与0.80 mol.L-1正丁醇溶液的Δpmax。
注意 在每次调换溶液时,测定管和毛细管均须用待测液淋洗。毛细管管口应保持干净,一旦污染,则得不到均匀而间歇的气泡。
五、数据记录与处理
(1)计算不同浓度的正丁醇水溶液的表面张力。

(2)绘出δ-c曲线图,在δ-c曲线图上求出各浓度值的相应斜率,即dδ/dc.
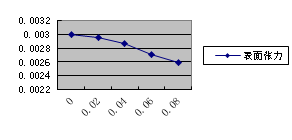
(3) 计算溶液各浓度所对应的单位表面吸附量。

六、思考题
(1)实验时,为什么毛细管口处于刚好接触溶液表面的位置?如果插入一定浓度将对实验带来什么影响?
答:减少测量Δpmax误差,因为Δpmax是气泡内外的压力差,在气泡形成过程中,由于表面张力作用,凹液面产生一个指向液面外的附加压力Δp, =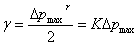 ,如果插入一定深度,p外还要考虑插入这段深度的静压力,使得Δpmax的绝对值变大,表面张力也变大。
,如果插入一定深度,p外还要考虑插入这段深度的静压力,使得Δpmax的绝对值变大,表面张力也变大。
(2)在毛细管口所形成的气泡什么时候其半径最小?
答:测量时Δpmax最大。
(3)为什么要求从毛细管中逸出的气泡必须均匀而间断?如何控制出泡速度?
答:如果气泡逸出的很快,或几个气泡一齐出,即气泡形成的时间太短,则吸附平衡就来不及在气泡表面建立起来,测得的表面张力也不能反映该浓度之真正的表面张力值。通过控制滴液漏斗的放液速度调节。
实验八 电导法测量弱电解质的电离常数
日期 2012/4/7 同组者姓名 XX XXX
成绩
一、实验目的
1.学会电导(率)仪的使用方法。
2.掌握溶液电导的测定。
二、实验原理
1.弱电解质电离常数的测定
AB型弱电解质在溶液中电离达到平衡时,电离平衡常数KC与原始浓度C和电离度α有以下关系(1):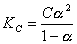 ,在一定温度下KC是常数,因此可以通过测定AB型弱电解质在不同浓度时的α代入式(1)求出KC。醋酸溶液的电离度可用电导法来测定,将电解质溶液放入电导池内,溶液电导(G)的大小与两电极之间的距离(l)成反比,与电极的面积(A)成正比即式(2):
,在一定温度下KC是常数,因此可以通过测定AB型弱电解质在不同浓度时的α代入式(1)求出KC。醋酸溶液的电离度可用电导法来测定,将电解质溶液放入电导池内,溶液电导(G)的大小与两电极之间的距离(l)成反比,与电极的面积(A)成正比即式(2):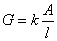 ,式中
,式中 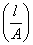 为电导池常数,以Kcell表示;κ为电导率。由于电极的l和A不易精确测量,因此在实验中是用一种已知电导率值的溶液先求出电导池常数Kcell,然后把欲测溶液放入该电导池测出其电导值,再根据(2)式求出其电导率。溶液的摩尔电导率是指把含有1mol电解质的溶液置于相距为1m的两平行板电极之间的电导。以Λm表示,其单位以SI单位制表示为S·m2·mol-1(以c·g·s单位制表示为S·cm2·mol-1)。摩尔电导率与电导率的关系:
为电导池常数,以Kcell表示;κ为电导率。由于电极的l和A不易精确测量,因此在实验中是用一种已知电导率值的溶液先求出电导池常数Kcell,然后把欲测溶液放入该电导池测出其电导值,再根据(2)式求出其电导率。溶液的摩尔电导率是指把含有1mol电解质的溶液置于相距为1m的两平行板电极之间的电导。以Λm表示,其单位以SI单位制表示为S·m2·mol-1(以c·g·s单位制表示为S·cm2·mol-1)。摩尔电导率与电导率的关系: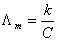 ,式中,C为该溶液的浓度,其单位以SI单位制表示为mol·m-3。对于弱电解质溶液来说,可以认为:
,式中,C为该溶液的浓度,其单位以SI单位制表示为mol·m-3。对于弱电解质溶液来说,可以认为: 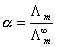 ,
,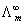 是溶液在无限稀释时的摩尔电导率。对于强电解质溶液(如KCl、NaAc),其Λm和C的关系为
是溶液在无限稀释时的摩尔电导率。对于强电解质溶液(如KCl、NaAc),其Λm和C的关系为 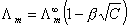 。对于弱电解质(如HAc等),Λm和C则不是线性关系,故它不能像强电解质溶液那样,从
。对于弱电解质(如HAc等),Λm和C则不是线性关系,故它不能像强电解质溶液那样,从 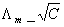 的图外推至C=0处求得
的图外推至C=0处求得 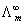 。但我们知道,在无限稀释的溶液中,每种离子对电解质的摩尔电导率都有一定的贡献,是独立移动的,不受其它离子的影响,对电解质
。但我们知道,在无限稀释的溶液中,每种离子对电解质的摩尔电导率都有一定的贡献,是独立移动的,不受其它离子的影响,对电解质 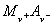 来说,即
来说,即 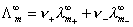 。弱电解质HAc的
。弱电解质HAc的 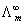 可由强电解质HCl、NaAc和NaCl的
可由强电解质HCl、NaAc和NaCl的 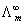 的代数和求得:
的代数和求得: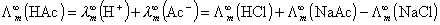 ,因此有
,因此有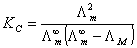 或
或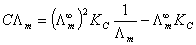 ,以CΛm对
,以CΛm对 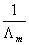 作图,其直线的斜率为
作图,其直线的斜率为 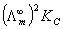 ,如知道
,如知道 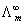 值,就可算出KC。
值,就可算出KC。
三、仪器药品
电导率仪1台; 恒温槽1套; 电导池1只; 电导电极1只; 容量瓶(100mL)5只;移液管(25mL、50mL)各1只; 洗瓶1只; 洗耳球1只。各种不同浓度的醋酸溶液。
四、实验步骤
(1)将恒温槽温度调至(25.0±0.1)℃或(30.0±0.1)℃;
(2)测定电导池常数Kcell
倾去电导池中蒸馏水,将电导池和铂电极用少量的10.00mol·m-3KCl溶液洗涤2~3次后,装入10.00mol·m-3KCl溶液,恒温后,用电导仪测其电导,重复测定三次。
(3)测定电导水的电导(率)
倾去电导池中的KCl溶液,用电导水洗净电导池和铂电极,然后注入电导水,恒温后测其电导(率)值,重复测定三次。
(4)测定HAc溶液的电导(率)
倾去电导池中电导水,将电导池和铂电极用少量待测HAc溶液洗涤2~3次,最后注入待测HAc溶液。恒温后,用电导(率)仪测其电导(率),每种浓度重复测定三次。按照浓度由小到大的顺序,测定各种不同浓度HAc溶液的电导(率)。 每次测定前,都必须将电导电极及电导池洗涤干净,以免影响测定结果。
五、数据处理
1.电导池常数Kcell
25℃或(30℃)时,10.00mol·m-3KCl溶液电导率: 0.140877s/m 。

2.醋酸溶液的电离常数
HAc原始浓度: 。

3.按公式(6)以CΛm对 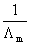 作图应得一直线,直线的斜率为
作图应得一直线,直线的斜率为 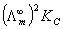 ,由此求得KC,并与上述结果进行比较。
,由此求得KC,并与上述结果进行比较。
【思考问题】
1. 为什么要测电导池常数?如何得到该常数?
答:醋酸溶液的电离度可用电导法来测定 用一种已知电导率值的溶液先求出电导池常数Kcell
2. 测电导时为什么要恒温?实验中测电导池常数和溶液电导,温度是否要一致?
答:减少误差,控制变量 不需要
