一、实验目的
1、测定在常压下环己烷-乙醇系统的气液平衡数据,绘制系统的沸点-组成图
2、确定系统的恒沸温度及恒沸混合物组成
3、了解阿贝折射仪的测量原理,掌握阿贝折射仪的使用方法
二、实验原理
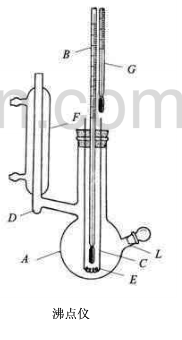
用沸点仪直接测定一系列不同组成液体混合物的气液平衡温度,并收集少量馏出物和馏出液,分别用阿贝折射仪测定折射率,利用折射率-组成工作曲线,查出对应于样品折射率的组成
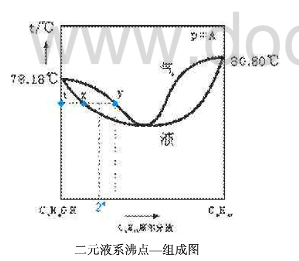
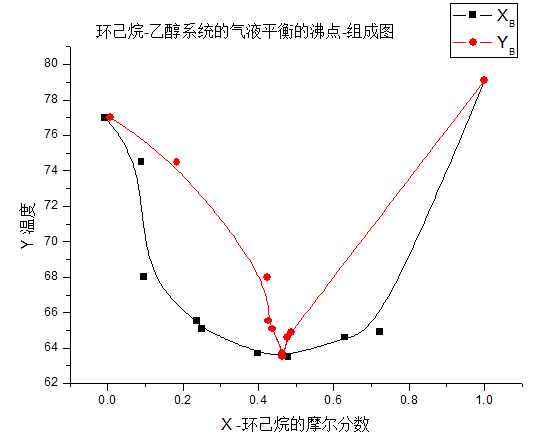
实验采用环己烷-乙醇系统,其沸点-组成图属于具有最低恒沸点的类型(如图所示)
三、实验仪器、试剂
仪器:沸点仪一套,NTY-2A型数字式温度计一套,YP-2B精密稳流电源一套,阿贝折射仪一套,HK-1D型恒温水槽一套
试剂:无水乙醇(A,R),环己烷(A,R),不同组成环己烷-乙醇的混合物
四、实验步骤
1、开启恒温水槽,设定水温为30℃,供阿贝折射仪使用;
2、加入试剂,盖好加料口塞子,使电热丝及温度传感器浸入液体中;
3、开冷凝水,温度传感器连接NTY-2A数字式温度计,加热丝连接YP-2B精密稳流电源。调节稳流电源电流,加热至沸腾。液体沸腾后,蒸气逸出,经冷凝后流入球形小室。最初在冷凝管下端球形小室的液体不能代表平衡时气相组成,为加速达到平衡可将球形小室内最初冷凝的液体倾回沸点仪内,反复2-3次,待温度读数恒定后记下沸点并停止加热
4、长吸液管吸取气相冷凝管,迅速测其折光率;用短吸液管,吸取蒸馏液迅速测其折光率
4、同法完成1、2、3、4、5、6、7、8,乙醇以及纯环己烷实验。
5、实验结束,关闭电源及水源。
五、数据记录与处理
室温: 21.7 ℃;
大气压(实验前) 101.45 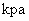 ,大气压(实验后) 101.45
,大气压(实验后) 101.45 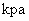 ,
,
大气压(平均值) 101.45  。
。
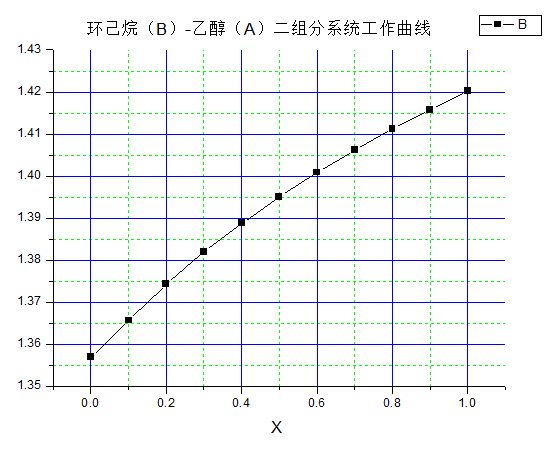
1、30℃时,已知组成的环己烷(B)-乙醇(A)二组分系统的折射率(温度:30.0℃+0.1℃)


六、结果与讨论
由图所示,得出,系统的最低恒沸点为63.5℃,最低恒沸混合物的组成为xB=0.4793.与书中所告诉我们的最低恒沸点为64.8,最低恒沸点混合物的组成(摩尔分数)为xB=0.55相比,相对偏小。
造成这种误差的可能原因:
1、 在给试剂加热的过程中,沸腾后,应将冷凝回流到球形小室的液体倾倒回沸点仪内,并反复3次,
而在实验时,可能忘记倾倒或者少了几次,导致所测得气相和液相的折射率有少许误差。
2、 在用阿贝折射仪测定折射仪时,毕竟是人肉眼所看,不能保证阴暗正好过中点。这样所测得数据就会有偏差。
3、 在取得液相或者气相测定的时候因为不够快而导致无法精准的测定。
4、 测定时,也没法保证前一次的测定对后一次的测定完全没有干扰。
5、 仪器本身存在误差
注意事项:
1、 检查沸点仪在是否干燥、清洁、是否有异物
2、 沸点仪在没有加入被测溶液时,不得调压加热
3、 测定折射率时,速度要快。
第二篇:物化实验报告3-液体饱和蒸气压的测定
一、实验目的
1.掌握用等位计测定乙醇在不同温度下的饱和蒸气压。
2.学会用图解法求乙醇在实验温度范围内的平均摩尔蒸气焓与正常沸点。
二、实验原理
一定温度下,液体纯物质与其气相达平衡时的压力,称为该温度下该纯物质的饱和蒸气压简称蒸气压。
纯物质的蒸气压随温度的变化可用克拉佩龙方程表示:
dP/dT = ΔvapHm/(TΔVm)
设蒸气为理想气体,在实验温度范围内摩尔蒸气焓ΔvapHm可视为常数。并略去液体的体积,积分得:
ln(P/pa) = -ΔvapHm/R*(1/T) +C
本实验采用静态法直接测定乙醇在一定温度下的蒸气压。
三、仪器与试剂
仪器: DPCY-2C型饱和蒸气压教学实验仪1套,HK-1D型恒温水槽1套,WYB-1型真空稳
压包1个,稳压瓶1个,安全瓶1个。
试剂: 无水乙醇。
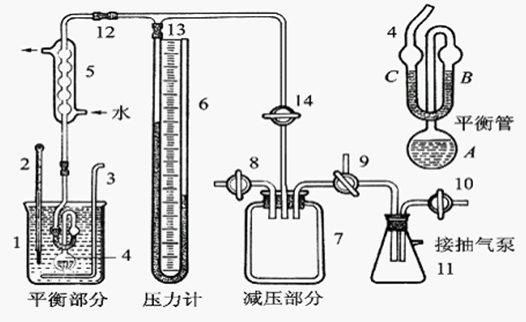
四、实验装置图
五、实验步骤
1.读取室温及大气压。
2.装样。
将等位计内装入适量待测液体乙醇,A球管约2/3体积,U形管两边各1/2体积,然后
按图装好各部分。
3.教学实验仪置零。
打开教学实验仪装置,预热5分钟,选择开关打到KPa,按下面板上的置零键,显示值
为00.00数值(大气压视为0看待)。
4.系统气密性检查
除了真空泵前的安全瓶活塞通大气外,其余活塞都关上,接通真空泵电源关闭与真空
连接的安全瓶活塞,开始抽真空。抽气减压至压力显示-40~-53KPa时,关闭三通活塞,
使系统与真空泵,大气都不相通,观察压力示数。
5.排除球管上方空间内的空气。
打开HK-1D型恒温电源,设定温度为25℃,接通冷凝水,同时调节搅拌器匀速搅拌,其目的是使等位计内外温度平衡,用WYB-1型真空稳压包控制抽气速度,抽气减压气泡逸出的速度以一个一个地逸出为宜至液体轻微沸腾,此时AB弯管内的空气不断随蒸气径C管逸出,如此沸腾3-5min可认为空气被排出、除干净(压力显示约-94KPa)。抽气结束后,先关闭真空稳压包上与稳压瓶相连的阀门,再关闭另一侧门,打开与真空泵连接的安全瓶活塞,使其通大气,最后关电源。
6.饱和蒸气压的测定
当空气被排除干净,且体系温度恒定后,旋转稳压瓶上的直通活塞H,缓缓放入空气,直至B、C管中液面平齐,关闭直通活塞H,记录温度与压力。然后,将恒温槽温度升高5℃,当待测液体再次沸腾,体系温度恒定后,再次放入空气B、C管液面再次平齐,记录温度和压力,依次测定,共测5个值,升高温度间隔为5℃。
7.结束实验
实验结束后,再读一次,关闭电源,打开真空稳压包上中间的阀门将体系放入空气,待等位计内乙醇冷却后,关掉冷凝管的冷却水,整理好仪器装置但不要拆装置。
六、注意事项
1、抽真空前后,与真空泵连接的安全瓶,都要通大气。
2、严格控制抽真空速度,不可过快。观察U型管气泡不要成串。
3、实验结束后,一定要用真空稳压包上中间的阀门缓慢通大气,防止封闭液过多流入球内。
七、数据记录及处理
室温:18.5 ℃
大气压(实验前):101.68 KPa 大气压(实验前):101.64 KPa
大气压(平均值):101.66 KPa
1.不同温度时,乙醇的蒸气压
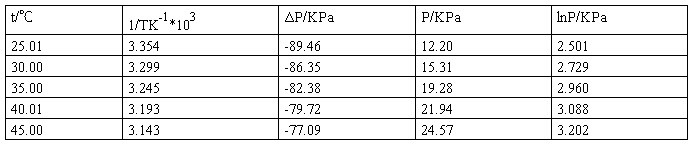
2.以lnP/KPa~1/TK-1*103作图

从图中可以看出,第2个数据点和第4个数据点在这条直线上。则直线斜率:
m= ( 3.088—2.729)÷(3.193—3.299)=—3.38679Kpa*K
直线截距C=13.884kpa, 所以直线方程为:
ln(P/pa)=—3.38679(103/(t+273.15))+13.884
从而得到 ΔvapHm= -m×R= -(-3.38679)×8.314=28.16kJ/mol.
将P=101.325代入直线方程,得到沸点Tb =92.4℃
3.计算实验的相对误差。
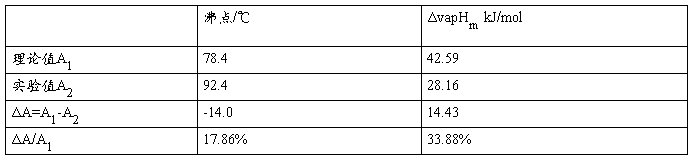
本实验的实验误差很大,可能有以下几个原因造成:
1) 由于等压计放置有点倾斜,造成视觉误差,判断平衡是出现较大的误差;
2) 读数时间间隔短,没有等等压计平衡就进行读数,造成的误差。
