职高高二化工期末试卷
用到的相对原子质量:N:14 H:1 O:16 C:12 Cl:35.5
一、选择题(每题4分,共120分)
1.少量金属钠应保存在( )
A.密闭容器中 B.水中 C.煤油中 D.浓NaOH溶液中
2.在常温下,不溶于浓硫酸、浓硝酸,也不溶于氢氧化钠溶液的金属是( )
A.铝 B.铁 C.钠 D.铜
3.物质所含分子数最多的是( )
A.34gNH3 B.18gH2O C.6.02×1023个CO2分子 D.2.5molH2
4.同温同压下,1LCH4和1LH2的质量比是( )
A.1 :1 B.16:1 C.1:8 D.8:1
5.下列物质中,硫元素既能被氧化,也能被还原的是( )
A.H2SO4 B.H2S C.SO2 D.SO3
6.下列气体中,有颜色且有刺激性气味的是( )
A.O2 B.CO2 C.CH4 D.Cl2
7.下列气体的水溶液有漂白性的是( )
A.HCl B.CO2 C.H2 D. Cl2
8.下列物质能使红墨水变蓝的是( )
A.碘 B.碘化钾 C.液溴 D.氯气
9.下列物质中,能使湿润的淀粉碘化钾试纸变蓝的是( )
A.KBr B.Cl2 C.NaCl D.CO
10.下列物质的水溶液中,滴加硝酸银溶液有白色沉淀生成的是( )
A.KCl B.KNO3 C.KI D.KBr
11.在集气瓶里,将硫化氢和二氧化硫两种气体充分混合后,可观察到的现象是( )
A.有黄色粉末产生 B.有棕色烟产生
C.有红色沉淀生成 D.有黑色沉淀生成
12.下列气体中,能造成环境污染的是( )
A.N2 B.SO2 C.CO2 D.N2
13.下列物质中,能用铝制容器贮存的是( )
A.冷的稀盐酸 B.冷的浓硫酸
C.冷的稀硫酸 D.冷的稀硝酸
14.浓硝酸跟铜反应,其氧化剂与还原剂物质的量之比为( )
A.4:1 B.2:1 C.8:3 D.2:3
15.某二价阴离子的电子层结构与18号元素的原子电子层结构相同,该元素是( )
A.Ca B.Mg C.S D.H2O
16.下列分子中,有3个原子核和10个电子的是( )
A.NH3 B.SO2 C.HF D.H2O
17.下列元素中,金属性最强的是( )
A.Na B.K C.Ca D.Al
18.下列各元素的原子半径最小的是( )
A.Na B.Cl C.Mg D.S
19.下列各组原子序数中,化学性质相似的一组是( )
A.2和9 B.9和17 C.14和20 D.8和12
20.下列元素中最高正化合价数值最大的是( )
A.Ca B.N C.Cl D.Ar
21.下列物质中,既含有离子键有含有共价键是的( )
A.NaOH B.CaO C.NH3 D.NaCl
22.比钠原子多一个质子有少一个电子的粒子是( )
A.Na B.Na+ C.Mg2+ D.Mg
23.下列物质中属于强电解质的是( )
A.SO3 B.铜 C.HF D. NaCl
24.将pH=4的醋酸和pH=10的氢氧化钠溶液等体积混合后,溶液呈(
A.酸性 B.中性 C.碱性 D.不能确定
25.有两种溶液,其PH分别是3和5,则两种溶液中OH-浓度比是(
A.3:5 B.5:3 C.100:1 D.1:100
26.下列溶液中酸性最强的是( )
) )
A.pH=4 B.pH=10 C.[ H+]=10-5mol·L-1 D.[OH-]=10-9mol·L-1
27.在NaAc水溶液中加入紫色石蕊溶液呈( )
A.红色 B.紫色 C.黄色 D.蓝色
28.下列物质的水溶液中[H+]大于[OH-]的是( )
A.K2CO3 B.KNO3 C.NH4Cl D.NH4Ac
29.pH=0的溶液是( )
A.没有OH-,只有H+ B.[ H+]=0 C. [H+]=1mol·L-1 D.[OH-]=10-14mol·L-1
30.体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时,两者
消耗NaOH的物质的量为( )
A.相同 B.HCl C.CH3COOH多 D.无法比较
二、填空题(每空2分,共56分。)
1.在新制的氯水中,含有含有 等分子,其中有杀菌、漂白能力的是下会发生化学反应,方程式是 。
2.漂白粉的有效成分是。制取漂白粉的化学方程式为 。
3..通常情况下,氨气是颜色、具有液称之为 。
4.具有相同的数,而有不同的子称为同位素。
5.第三周期的主族元素,从Na到Cl,原子半径逐渐,失电子能力逐渐 ,非金属性逐渐 ,金属性逐渐 ,非金属性逐渐 。
6.R2-离子的M电子层与L电子层电子数相等,元素R应处于周期表中第 周期,第 族。
7.4个CO2中所含的氧原子与个H2SO4中所含的氧原子数相同。
8.写出下列物质在水中的解离方程式。
(1) 氢氧化钠
(2) 醋酸
(3) 氨水
9.含有NaCO3的盐碱地不利于作物生长。用化学方程式表示产生碱性的原因
通过施加适量石膏(CaSO4·2H2O)可以降低土壤的碱性。用化学方程式表示石膏降低土壤碱性的原因。
三、计算题(共26分)
1.5g氢气和142g氯气混合点燃,将生成的气体用水完全吸收得到溶液500ml,求溶液中生成物的物质的量浓度。(16分)
2.已知某溶液[OH-]=10-4mol·L-1,计算溶液的[H+]和pH。(10分)
第二篇:职高二年级期末试卷
20##—2011年度上学期期末考试数学试卷
(时间:100分钟 总分:100分 答案写到答题卡上)
一、判断题(每小题2分,共20分)
1. 1、4、7、10是等差数列。
2. 1与16的等比中项是4.
3. 若 与
与 是相反向量,则它们的模相等。
是相反向量,则它们的模相等。
4. 差向量的方向由被减向量的终点指向减向量的终点。
5. 若直线的倾斜角为 =
= ,则k=
,则k=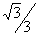
6. 3x+4y+5=0的一个法向量为(4,3)
7. (x-1)2+y2=4表示圆心为(1,0)半径为4的圆。
8. 过三点有且只有一个平面。
9. 过直线外一点有且只有一条直线与这条直线平行。
10. 过直线外一点有且只有一条直线与已知直线垂直。
二、选择题(每小题2分)
1. 已知等差数列的前三项为a-1,a+2,2a+3,则此数列的通项公式为( )
A、3n+1 B、3n-1 C、3n-5 D、3n-2
2. 在等比数列 中,
中,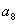 是
是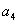 与( )的等比中项。
与( )的等比中项。
A、 B、
B、 C、
C、 D、
D、
3. 向量 等于( )
等于( )
A、 B、
B、 C、
C、 D、
D、
4. 已知 =2,向量
=2,向量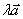 是单位向量,则实数
是单位向量,则实数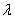 等于( )
等于( )
A、2 B、 C、
C、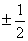 D、
D、
5. 直线 的倾斜角为( )
的倾斜角为( )
A、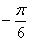 B、
B、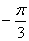 C、
C、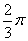 D、
D、
6. 以点(2,-1)为圆心,且与直线3x-4y+5=0相切的圆的方程为( )
A、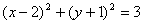 B、
B、
C、 D、
D、
7. 已知圆 的圆心在(3,4),则r=( )
的圆心在(3,4),则r=( )
A、 B、
B、 C、
C、 D、5
D、5
8. 点P在直线 上,直线
上,直线 在平面
在平面 内,可记为( )
内,可记为( )
A、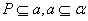
 B、
B、 C、
C、 D、
D、
9. 已知直线n // 平面 ,直线m
,直线m ,那么直线n与m的位置关系是( )
,那么直线n与m的位置关系是( )
A、平行 B相交 C、异面 D、平行或异面
10. 下列命题中
(1)平行于同一条直线的两条不重合的直线平行
(2)平行于同一条直线的两个不重合的平面平行
(3)平行于同一个平面的两条不重合的直线平行
(4)平行于同一平面的两个不重合的平面平行
正确的是( )
A、(1)(2) B(1)(4) C、(2)(3) D(2)(4)
三、填空题(每小题3分)
1. 已知 ,则
,则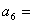
2. 等比数列 中,
中, 是方程7x2-18x+7=0的两根,则
是方程7x2-18x+7=0的两根,则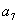 =
=
3. 已知A(-1,2),B(-2,1),则 =
=
4. 已知 则
则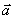 与
与 的夹角为
的夹角为
5. 已知直线上L上两点A(2,1),B(-1,3),则直线的斜率为
6. 圆心为(-1,-3)且过点(2,1)的圆的方程为
7. 已知直线L的倾斜角的正弦为 ,则直线的斜率为
,则直线的斜率为
8. 在空间四边形ABCD中,E、F、G、H分别为AB、AD、BC、DC的中点,则四边形EFHG为 四边形,若AC=BD,则四边形EFHG为
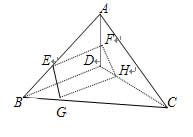

在正方体ABCD-A1B1C1D1中
9. 直线A1D与BC1是 直线,所成角为 度。
10. 与直线AB平行的平面有
答题卡
一、判断题(2分*10)
1—5 6—10
二、选择题(2分*10)
1—5 6—10
三、填空题(3分*10)
1、 2、 3、 4、
5、 6、 7、 8、
9、 10、
四、解答题(每小题6分,共30分)
1、已知等差数列 中,
中, 求
求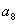 和d
和d
2、已知 ,求
,求 及
及
3、求两条平行线 与
与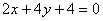 间的距离
间的距离
4、求圆心在直线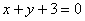 上,且过点A(6,0)B(1,5)的圆的方程
上,且过点A(6,0)B(1,5)的圆的方程
5、长方体AC1中,AB=BC= cm,AA1=2cm求
cm,AA1=2cm求
(1) BC与A1C1所成的角
(2) AA1与BC1所成的角
