有机物化学反应方程式汇总

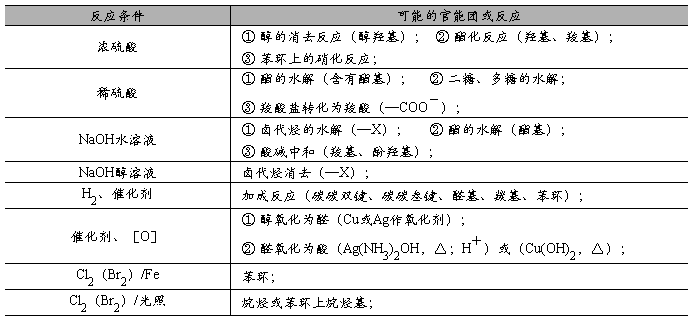
从反应试剂归纳有机反应

从反应条件归纳有机反应
第二篇:必修I 化学反应及离子反应方程式汇总
必修I 化学反应及离子反应
方程式汇总
一、钠及其化合物的反应
1、钠块在空气中变暗
4Na+O2=2Na

2O
钠在空气中燃烧(黄色的火焰)
2Na + O2 Na2O2
Na2O在空气中加热(变黄)
2Na2O+O2=2Na2O2
2、钠与水反应
(浮、熔、游、响、红)
2Na + 2H2O = 2NaOH+ H2 ↑
2Na +2H2O=2Na++2OH -+H2 ↑
钠与硫酸铜溶液的反应:
2Na+2H2O+CuSO4=Cu(OH)2↓+ H2↑+Na2SO4
钠与氯化铁溶液的反应:
6Na+6H2O+2FeCl3=2Fe(OH)3↓+ 3H2↑+6NaCl
3、过氧化钠与水的反应
2Na2O2 + 2H2O = 4NaOH + O2 ↑
2Na2O2 + 2H+2O = 4Na+4OH -+O2↑
(放热反应、Na2O2是强氧化剂,用于漂白)
碱性氧化物Na2O与水的反应
Na2O+H2O=2NaOH
4、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是: 2Na2O2 + 2CO2 = 2Na2CO3 + O2
5、苏打(纯碱)与盐酸反应
①盐酸中滴加纯碱溶液
Na2CO3 + 2HCl = 2NaCl + H2O+CO2↑
CO2-
3 + 2H+ = H2O + CO2↑
②纯碱溶液中滴加盐酸,至过量
Na2CO3 + HCl =NaHCO3 + NaCl
CO2-
3 + H+ = HCO-3
NaHCO3+HCl=NaCl+H2O+CO2↑
HCO-+
3+H= H2O +CO2↑
6、小苏打受热分解
2NaHCO△
3 Na 2CO3 + H2O +CO2 ↑
7、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热
NaHCO △ Na
3 + NaOH 2CO3 + H2O
HCO-+ OH - = H2-
32O + CO3(若是溶液中反应有离子方程式)
8、NaHCO3与Ca(OH)2反应:
1
①NaHCO3不足的离子反应方程式:
HCO3+OH+Ca= H2O+CaCO3↓
②NaHCO3过量的离子反应方程式
2HCO3-+2OH-+Ca2+= 2H2O+CaCO3↓+ CO32-
9、氯化钙与碳酸钠溶液反应:
CO32-+Ca2+= CaCO3↓
10、金属锂在空气中燃烧
4Li+O2 △ --2+2O 11、碳酸钠的电离方程式
Na2CO3 = 2Na+ + CO32-
二、镁、铝及其化合物的反应
1. 铝箔在氧气中剧烈燃烧
4Al + 3O2 点燃 2Al2O3
2. 铝片与稀盐酸反应
2Al + 6HCl = 2AlCl3 + 3H2↑
2Al + 6H+ = 2Al3+ +3H2↑
3. 铝与氢氧化钠溶液反应
2Al+2NaOH +2H2O = 2NaAlO2 +3H2↑
-- 2Al+2OH +2H2O = 2AlO2 + 3H2↑
4. 铝与三氧化二铁高温下反应(铝热反应)
2Al + Fe2O3 高温 2Fe + Al2O3
5. 氧化铝溶于盐酸溶液
Al2O3 + 6HCl 2AlCl3 +3H2O
++ Al2O3 + 6H=2Al+3H2O
氧化铝溶于氢氧化钠溶液
Al2O3 + 2NaOH 2NaAlO2 +H2O
Al2O3 + 2OH-=2AlO2-+H2O
6. 硫酸铝溶液中滴过量氨水
Al2(SO4)3 +6NH3·H2O=2Al(OH)3↓+3(NH4)2SO4 Al3++3NH3·H2O = Al(OH)3↓+ 3NH4+
铝盐与过量的强碱反应
Al3+ + 4OH- =AlO2- + 2H2O
7. ①氢氧化铝溶液中加盐酸
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3 + 3H+ = Al3+ + 3H2O
②Al(OH)3与NaOH溶液反应
Al(OH)3 + NaOH NaAlO2 +2 H2O
--Al(OH)3 + OH = AlO2 +2 H2O
8、用氢氧化钡与明矾溶液的反应
①铝离子恰好沉淀完的离子反应
3Ba2++3SO42-+2Al3++6OH-=3BaSO4↓+2Al(OH)3↓ ②使硫酸根离子沉淀完全的离子反应
2Ba2++2SO42-+Al3++4OH-=2BaSO4↓+AlO2-+2H2O
2
9、氢氧化铝加热分解
2Al(OH)3 △ 2O3 + 3H2O
10、偏铝酸钠与二氧化碳的反应 ①二氧化碳少量的反应: 2NaAlO2+3H2O+CO2= 2Al(OH)3 ↓+Na2CO3 2AlO2-+3H2O+CO2= 2Al(OH)3 ↓+CO32- ②二氧化碳足量的反应: 2NaAlO2+3H2O+CO2= 2Al(OH)3 ↓+Na2CO3 AlO2+2H2O+CO2= Al(OH)3 ↓+HCO3
11. 镁在空气中燃烧 : ①镁与空气中的氧气反应: 2Mg + O2 点燃 -- 2MgO
②镁与空气中的二氧化碳反应: 2Mg + CO2
点燃 2MgO + C ③镁与空气中的氮气的反应: 3Mg + N2 点燃 Mg3N2
12. 镁与盐酸的反应:
Mg+ 2HCl = MgCl2 +H2↑ Mg +2H+ = Mg2+ + H2↑
三、铁、铜及其化合物的反应
1、铁与硫加热反应
Fe +

S FeS
铁与氧气加热反应 3Fe+2O2 Fe

3O4
铁在氯气中加热反应 2Fe+3Cl2 2FeCl3
高温
2. 高温下铁与水反应 3Fe+4H2O(g) Fe3O4+4H2
3. 铁与盐酸反应
Fe + 2HCl = FeCl2 + H2↑ Fe + 2H+ = Fe2+ + H2↑
4. 铁与硫酸铜溶液反应 Fe + CuSO4 = FeSO4 + Cu
Fe + Cu2+ = Fe2+ + Cu
5. 氧化亚铁溶于盐酸中 FeO + 2HCl = FeCl2 + H2O
FeO + 2H = Fe + H2O 氧化铁溶于盐酸中
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 6H+ = 2Fe3+ + 3H2O
3
+2+
四氧化三铁溶于盐酸中
Fe3O4 + 8HCl = 2FeCl3 +FeCl2+4H2O
Fe3O4+8H+ = 2Fe3+ +Fe2++ 4H2O
6. 氯化铁中滴入氢氧化钠溶液(红褐色沉淀) FeCl3+3NaOH = Fe(OH)3↓+3NaCl
Fe3++3OH - = Fe(OH)3 ↓
7. 氢氧化亚铁在空气中被氧化
(白色沉淀迅速变成灰绿色最后变为红褐色沉淀) 4Fe (OH)2+O2+2H2O =4Fe (OH)3
8. 氯化亚铁溶液中通入氯气
2FeCl2 +Cl2 =2FeCl3
2 Fe2+ +Cl2 =2 Fe3++2Cl-
9. 氯化铁溶液中加入铁粉
2FeCl3+Fe = 3FeCl2
2Fe+ Fe = 3Fe
10. 用KSCN检验的存在离子方程式 3+2+
Fe+3SCN-= Fe (SCN)3
11. 氯化铁溶液中加入铜片的反应
2FeCl3 + Cu = 2FeCl2+CuCl2
3+ + Cu = 2Fe2++Cu2+
2Fe
12. 氢氧化铁加热分解
2Fe(OH)3 △ 3+2O3 + 3H2O
13.硫酸亚铁与氢氧化钠溶液反应
FeSO4+2NaOH = Fe(OH)2↓+Na2SO4
Fe+2OH = Fe(OH)2 ↓ 四、碳、硅及其化合物的反应
1、Si 与F2 的反应
Si+2F2 =SiF4
2、Si与HF的反应: Si+4HF SiF4+2H2
3、Si 与NaOH溶液的离子反应:
Si+2NaOH+H2O
Si+2OH +H2O -2+-Na2SiO3 +2H2↑ SiO3+2H2↑

2-
SiO2+2NaOH = Na2SiO3 + H2O
SiO2+2OH -= SiO32- + H2O
7、硅酸钠与HCl的反应:
Na2SiO3+2HCl=2NaCl+H2SiO3↓
4
SiO3+2H=H

2SiO3↓
8、硅酸的受热分解:
H2SiO3SiO2+H2O
9、工业制单质硅(碳在高温下还原二氧化硅) SiO2 + 2C 高温

2-+ Si + 2CO↑
铜丝在氯气中剧烈燃烧(棕色烟)
Cu + Cl2 点燃 CuCl2
之后加水,可由绿色溶液(浓)得到蓝色溶液(稀)
2、Na在氯气中剧烈燃烧(棕色烟)
2Na + Cl2 点燃 2NaCl 3、铁在氯气中剧烈燃烧 2Fe+3Cl2 点燃 3FeCl3(棕褐色烟)
4、氢气在氯气中燃烧(苍白色火焰)
H2 + Cl2 点燃 2HCl
氟气与氢气反应(黑暗处即可爆炸)
H2+F2=2HF
5、氯气溶于水
Cl2+H2O = HCl + HClO
Cl2+H2O = H++Cl-+HClO
新制氯水中含有的微粒:
(H+ 、Cl -、ClO -、OH-、Cl2、HClO、H2O)
6、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂) 2HClO 2HCl + O2↑
7、工业制漂白粉的原理及漂白粉的失效
2Ca(OH)2 + 2Cl2 =Ca(ClO)2 + CaCl2 + 2H2O
2Ca(OH)2 +2Cl2 =2Ca2++2ClO-+2Cl -+2H2O Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HclO
Ca(ClO)2+2CO2+2H2O=Ca(HCO3)2+2HClO
2+-- Ca+2ClO+2CO2+2H2O =2HCO3+ 2HclO
8、工业制漂白液的原理
2NaOH+ Cl2 =NaClO+NaCl+H2O
2OH-
+Cl2 =ClO-+Cl -+2H2O
9、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶) MnO2 +4HCl(浓)
MnCl2+Cl2↑+2H2O 5
MnO2 +4H++2Cl-Mn2++Cl2↑+2H2O
10、新制氯水注入盛NaBr溶液的试管中
Cl2 + 2NaBr = Br2 + 2NaCl
Cl2 + 2Br- = Br2 + 2Cl-
新制氯水注入盛FeCl2溶液的试管中
Cl2 +2FeCl2 =2FeCl3
新制氯水注入盛NaI溶液的试管中
Cl2 +2NaI =2NaCl+I2
11、氯气与二氧化硫同时通入水中
Cl2+SO2 +2H2O=H2SO4 +2HCl 六、硫及其化合物的反应
1、硫粉与氧气的反应:在空气中燃烧产生淡蓝色火焰,在纯氧中产生蓝紫色火焰
点燃

S+O2SO2 Cu+2H2SO4 (浓) CuSO4 +2H2O+SO2 ↑
6、碳与浓硫酸反应:
C+2H2SO4(浓) 2H2O+CO2↑+2SO2↑
7、硫酸根离子的检验
8、硫酸的电离方程式
6
七、氮及其化合物的反应
1、氮气和氢气反应(工业合成氨)
N 催化剂
2 + 3H2 高温高压 2NH3
2、
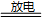
氮气和氧气放电下反应(雷雨发庄稼)
N2+O2 2NO
2NO + O2 2NO2
二氧化氮溶于水 3NO2 + H2O 2HNO3 + NO 3NO+-
2 + H2O 2H+ 2NO3+NO
3、HNO3与Cu的反应
①Cu与浓HNO3
Cu+4HNO3 = Cu(NO3)2+2NO2↑+2H2O Cu+4H+ +2NO-
3=Cu2++2NO2↑+2H2O
②Cu与稀HNO3反应
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 3Cu+8H+ +2NO-
3=3Cu2++2NO↑+4H2O
4、HNO3与Fe的反应
Al、Fe遇浓HNO3、浓硫酸钝化(常温)
①Fe与浓HNO3加热 Fe+6HNO△
3 3)3+3NO2↑+3H2O
②Fe与稀HNO3反应
Fe+4HNO3=Fe(NO3)3+NO↑+2H2O 3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O(铁粉过量) 5、 C与浓HNO3加热
C+4HNO
3(浓) △ CO2↑+4NO2↑+2H2O
6、 S与浓HNO3加热
S+6HNO3(浓) △ H2SO4+6NO2↑+4H2O
7、NO2 、O2 的混合气通入水中无剩余气体
4NO2+O2 +2H2O = 4HNO3
8、NO 、O2 的混合气通入水中无剩余气体
4NO+3O2+2H2O =4HNO3
9. 碳酸氢铵受热分解 NH4HCO3 △ NH3 ↑+ H2O↑ + CO2↑
10. 氯化铵受热分解 NH△
4Cl 3 ↑+ HCl↑
11、 用浓盐酸检验氨气(白烟生成)
HCl + NH3 = NH4Cl
12、硫酸铵溶液与氢氧化钠溶液混合加 7
(NH △
4)2SO4 +2NaOH 3↑+Na2SO4 +2H2O
NH+ △
4 + OH - NH3 ↑+ H2O
13、 硝酸铵溶液与氢氧化钠溶液混合(不加热) NH4NO3 + NaOH = NH3·H2O + NaNO3
NH+-
4 + OH = NH3·H2O
14、氨水显碱性:
NH3+H2O NH3·H2O NH+- 4+OH
氨水受热分解:
NH NH
3·H2O △ 3↑+H2O
15、实验室制氨常用加热铵盐和碱的混合物: 2NHCl+Ca(OH) △
42 3↑+CaCl2+2H2O
16、氨的催化氧化
4NH3 +
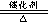
5O2 4NO+6H2O
17、氨气与氯气反应
①氯气过量:
2NH3 +3Cl2= N2+6HCl
②氨气过量:
8NH3 +3Cl2= N2+6NH4Cl(用于检验氯气管道是否漏气)
8
