�л���ѧ��ĩ��ϰ�ܽ�
һ���л������������
������ѧϰ�л���ѧ�ġ����ԡ�����ˣ�Ҫ��ѧϰ�߱������ա��л��������������������ϰ��������ϵͳ�����ȷ�����Ҫ���ܶԳ����л�������д����ȷ�����ƻ��������д���ṹʽ����ʽ��
1�� ��������д �� Ҫ������һЩ���������������Ļ�����Ľṹʽ���磺ľ�����ʴ���
���͡�ʯ̿�ᡢ���ᡢˮ��ȩ��ˮ���ᡢ�ȷ¡����ᡢ��ζ�ᡢ����ᡢ�������ʰ��ᡢ�����ᡢ�Ȱ��ᡢ�Ͷ�ȩ�������ǡ����ǵȡ���Ӧ��ϤһЩ��������д����Ʒ�����������Ļ�����磺RNA��DNA����˾ƥ�֡��������֡���Ŷ��ȡ�
2��ϰ����������Ҫ�����ա������졢�¡����������١��塢��������ͷ�ĺ��弰�÷���
���ճ��������Ľṹ���磺ϩ��������ϩ��������������������춡�����嶡�����л��ȡ�
3��ϵͳ��������ϵͳ���������л��������������ص㣬�����������ո�����������ԭ����������������ǻ����������칹�塢��ѧ�칹��Ͷ�����Ż�������������ѵ㣬Ӧ�������ӡ�Ҫ�μ�����������ѭ�ġ��������
4�����������������Ǹ���ȡ������������˳�����еĹ���
������1��ԭ�ӣ�ԭ�������������ǰ�棬ͬλ��������������ȡ����ֳ���ԭ�ӵ����ȴ���Ϊ��I>Br>Cl>S>P>O>N>C>H
������2�����ͻ��ţ������һ��ԭ��������ͬ����Ƚϵڶ���ԭ�ӵ�ԭ���������������ơ��������������ȴ���Ϊ��(CH3)3C->(CH3)2CH->CH3CH2->CH3-
������3�������ͻ��ţ��ɿ�������������������ͬ��ԭ�����������������������ȴ���Ϊ: -C��CH>-CH=CH2>(CH3)2CH-
�������������ҪӦ����������ϵͳ������ϩ���м����칹�������
����������ϵͳ��������������������м�����ͬ��ȡ��������ȡ�������ա��������һ���г������Ȼ��ź��г���
�������մ��������������ȴ���Ϊ���嶡��>�춡��>����� >����>����>�һ�>����
��1�� �������칹�������:ϩ�������칹�����������˳������Z��E���ַ�����
�Ļ����������˳����ʾ��Ҳ������Z��E��ʾ����˳����ʾʱ����ͬ��ԭ�ӻ������˫��̼ԭ��ͬ���Ϊ˳ʽ����֮Ϊ��ʽ�����˫��̼ԭ���������ĸ����Ŷ�����ͬʱ��������˳����ʾ��ֻ����Z��E��ʾ�����ա�������Ƚ����Ի��ŵ�����˳���Ż�����˫��̼ԭ��ͬ���ΪZ�ͣ���֮ΪE�͡�����ע�⣬˳������Z��E�����ֲ�ͬ�ı�ʾ�����������ڱ�Ȼ��������ϵ���еĻ����������˳����ʾ��Ҳ������Z��E��ʾ��˳ʽ�IJ�һ����Z�ͣ���ʽ�IJ�һ����E�͡����磺
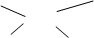 CH3-CH2 Br
CH3-CH2 Br
C=C ����ʽ��Z�ͣ�
H CH2-CH3
 CH3-CH2 CH3
CH3-CH2 CH3
C=C (��ʽ��E��)
H CH2-CH3
֬��������Ҳ����˳���칹�壬����ȡ�����ڻ�ƽ���ͬ��Ϊ˳ʽ����֮Ϊ��ʽ��
˫�����Ż������������˫�����źͶ�����Ż�����������ؼ���ȷ��
ĸ�塣�����������¼��������
�� ��±�غ����������������Ų���ʱ����±�غ�������Ϊȡ����������������Ϊĸ�塣
�� ��˫�����ǻ����ʻ����Ȼ�����ʱ������ϩ��Ϊĸ�壬�����Դ���ȩ��ͪ������Ϊĸ�塣
�� ���ǻ����ʻ�����ʱ����ȩ��ͪΪĸ�塣
�� ���ʻ����Ȼ�����ʱ��������Ϊĸ�塣
�� ��˫������������ʱ��Ӧѡ��Ⱥ���˫���ֺ����������̼��Ϊ���������ʱ��˫���������Ծ����ܵ͵����֣����˫����������λ������ͬ����Ӧ��˫������ͱ�š�
�����ŵ�����˳��:-COOH���Ȼ���>-SO3H��������� > -COOR��������>-COX��±���������� > -CONH2 (����������) > -CN (�����> -CHO��ȩ����> -CO- ���ʻ���> -OH(���ǻ�)> -OH (���ǻ�) >-SH ���ϻ���> -NH���������� > -O- ���ѻ���> ˫�� > ����
(4)���ӻ������������ ���ڴ��ӻ�ĸ��������������������������ԣ�һ��������뷨��Ҫע��ȡ�����ı�š�
�����л�������Ļ�����Ӧ
1���ӳɷ�Ӧ�����ݷ�Ӧ���̲�ͬ��Ϊ��ӳɡ��˼ӳɺ�������ӳɡ�
��1�� ����ӳɣ������Լ��Ľ��������еļӳɷ�Ӧ��Ҫ�����ղ��Գ�ϩ������
��ӳɷ�Ӧʱ����ѭ�����Ϲ����Լ��д�����˵IJ��ּӵ�����϶��˫��̼ԭ���ϣ������Բ��ּӵ�������ٵ�˫��̼ԭ���ϡ�ϩ����±�ء�±���⡢���ᡢ��±�ᡢˮ��Ȳ����±�ء�±���⡢ˮ�Լ�����˫ϩ��1��2��1��4�ӳɶ�����ӳɷ�Ӧ��ϩ��������ӳɷ�Ӧʱ��˫���ϵ������ܶ�Խ��ӦԽ�����С�
��2�����˼ӳɣ������Լ����������еļӳɷ�Ӧ��Ҫ�������Լ��ĸ���˼ӳɷ�Ӧ�����̣��ӳɼ��ӳɩ�����������ͬ�ṹ���ʻ�����������˼ӳɷ�Ӧ�Ļ���˳��Ӱ�췴Ӧ���Ե����ء��ʻ��������������ᡢ���������ơ����������Լ���������������ļӳɶ����˼ӳɷ�Ӧ�� �ʻ�����������˼ӳɷ�Ӧ�Ļ���˳��Ϊ��
HCHO>CH3CHO>RCHO>C6H5CHO>CH3COCH3>RCOCH3>C6H5COCH3>C6H5COC6H5
��3�������ɻ��ӳɣ������ɻ����������еļӳɷ�Ӧ��ϩ���ڹ���������������廯����еļӳ������ɻ��ӳɡ����Գ�ϩ�����廯��������ɻ��ӳ�ʱ�õ������Ϲ���IJ������ӵ�������ٵ�˫��̼ԭ���ϡ�
�ӳɷ�Ӧ��������������֮�⣬���в��������Ĵ��⻯�������ϩ��˫ϩ�ϳɵȡ�
2��������Ӧ ��һ���������������ȥ��С���ӣ���H2O��HX��NH3�� ���γ� ˫���������ķ�Ӧ��������Ӧ��±������±����ʹ���ˮ����Ҫ��������Ӧ��
��1����±������±���⣺±������������Ӧ����ǿ���������½��С���ͬ�ṹ��±��������������Ӧ�Ļ���˳��Ϊ������>����>һ����Ҫ����±��������������Ӧʱ����ѭ�IJ����ɷ����±�����в�ֻ����һ����̼ʱ������ʱ��ȥ�����ٵ���̼�ϵ���ԭ�ӣ�����˵��������˫��̼�����������϶��ϩ�����༴��±����Ͳ�±���鷢����ȥ��Ӧʱ, ��Ҫ����˫����������������ϩ����Ҫע�⣬±������������ˮ���Ǿ�����Ӧ��
��2������������������������Ӧ��ǿ���������½��У���������Ҳ��ѭ�����ɷ����Ҫ���ղ�ͬ�ṹ�Ĵ�����������Ӧ�Ļ���˳���崼>�ٴ�>������
3��ȡ����Ӧ ���ݷ�Ӧ���̵IJ�ͬ�ɷ�Ϊ��ȡ������ȡ���������ȡ����
�š���ȡ�����������Լ��Ľ�����������ȡ����Ӧ����ȡ����Ӧ�������ϵ�±�����������ǻ���������������������Լ��ص��ε�ż�Ϸ�Ӧ�ȣ�������ȡ����Ӧ�������ͷ����ӻ���Ҳ�ܷ�����ȡ����Ӧ��Ҫע�ⱽ�������¶ۻ���ʱ���ܽ��и��Ϸ�Ӧ�������Ͻ��������ʱ�ᷢ���칹���������������Ͻ�����ȡ����Ӧ�Ĺ��ɣ���һ��ȡ������Ҫ�����λ���ڶ���ȡ�����ǽ���ͬ�������컷��ԭȡ�����Ķ�λЧӦ������������Ա����Ա�����ӻ����������ȡ����Ӧ�Լ������뱽���ȽϽ�����ȡ����Ӧ���ԵIJ��죬ૡ���ԡ�����������ȡ����Ӧ�Ļ��Աȱ�����ऱȱ�С��
�ơ���ȡ�� �����Լ��Ľ����������ȡ����Ӧ����ȡ����Ӧ��±������ˮ�⡢���⡢��⡢���⣬������±��ķ�Ӧ���Ѽ��Ķ��ѣ������������ˮ�⡢���⡢����ȶ�����ȡ����Ӧ��±��������ȡ����Ӧ�ɰ��������̽��У����������̣�SN1����˫�������̣�SN2������±�����װ�SN2���̷�Ӧ����±����һ�㰴SN1���̷�Ӧ����±�������������֮��Ҫ�����ⷴӦ���̵Ļ��������ղ�ͬ±����������ȡ����Ӧ�Ļ��ԣ�SN1��Ӧ֧��Խ�����Խǿ����Ӧ����Խ�죬SN2��Ӧ֧��Խ�࣬��Ӧ����Խ������Ӧ����Խ�����磺���л����ﰴSN1���̷�Ӧ�Ļ����ɴ�С����Ϊ��(CH3)3CI > (CH3)3CBr > (CH3)2CHBr�� Ҫע�⣬�ڼ���������±������ȡ���������ǻ��ྺ���ķ�Ӧ����±������������������±��������ȡ����ǿ�����ܼ�����ˮ��������ȡ�������������ܼ����紼����ǿ��紼�ƣ�����������������������������
�ǡ����ɻ�ȡ���������ɻ������������е�ȡ�������ɻ�ȡ����������±����ϩ����������Ħ�±�������ɻ�ȡ����Ӧ����Ӧ�����Ǹ��¡����ջ����������ڡ����ɻ����ȶ��Ժ�����̼ԭ���������������Ŀ�йأ����Խ�࣬�ȶ���Խ�����ɻ����ȶ�����Ϊ��
����>����>һ��>·CH3
4��������ԭ��Ӧ ����������Ӧ�ͻ�ԭ��Ӧ�������͡�
�š�������Ӧ ϩ��Ȳ�����������Լ������ӡ�ȩ��ͪ�ȶ�����������ӦҪ���ռ��ֳ��õ����������������ء��ظ���ص�������Һ���������������������Լ������Լ�������Լ�����±���Ƶȡ�����������Ӧ��ʵ���е�Ӧ�ã�����������������Ʋ�ϩ���Ľṹ�������Լ�������Լ�����������������ȩ��ͪ�ȡ�
�ơ���ԭ��Ӧ ���������Ĵ��⻯��ȩ��ͪ�����ἰ����ԭΪ������������ԭΪ�����ȶ��ǻ�ԭ��Ӧ��Ҫ���ռ��ֳ��õĻ�ԭ������H2/Ni�� Na+C2H5OH��Fe+HCl��NaBH4���� ��LiAlH4�������/��������ȣ�ע������������ṩ�������ӵĻ�ԭ����ֻ���ʻ�ѡ����⣬��˫�����������������á���Ҫ�����ʻ���ԭΪ�Ǽ������ַ�����ע�⣬���п�����ɭ��ԭʱ��Ӧ������в��ܴ��ڶ������еĻ��ţ��紼�ǻ���˫���ȣ����������������ԭ���������Ľ���ʱ����Ӧ������в��ܴ��жԼ����еĻ��ţ���±�صȡ�
5�����Ϸ�Ӧ ��Ҫ������ȩ���Ϻ������ϡ�
��1����ȩ���� ���Ц����ȩ��ϡ�����������������ǻ�ȩ���˻����ﲻ�ȶ�
����������ˮ������������������ȩ����ˣ��˷�Ӧ����������̼���Ʊ�������������ȩ��Ҫ��������ȩ���ϵķ�Ӧ������
��2������ɭ������ ���Ц��������ǿ�������·�������ɭ�����ϣ���������֮����ȥһ���Ӵ����ɦ�ͪ������Ҫ���շ�Ӧ��������ʵ���е�Ӧ�ã��л��ϳ��й㷺Ӧ�õ�����������������ͨ���˷�Ӧ�Ʊ��ġ�
���������������͵ķ�Ӧ֮�⣬��Ҫ�������ص�����Ӧ�������ص��ε�ȡ����Ӧ�����ȷ�Ӧ�ȣ�ע�ⷴӦ���������P����ʵ���е�Ӧ�á�
�����л��������ת�����ϳɷ���
Ҫ�������л���������������֮���ת����ϵ������������̼�ķ������ڴ˻�������Ƽ��л�������ĺϳ�·�ߡ��������ձ����и������������������Ȳ�������������ȩ���ϡ������Լ����ȶ���������̼����Ȳ����������������Լ����������ص��ε����л��ϳ���Ӧ�÷dz��㷺��
1��Ȳ��������� ����Ȳ���Ȳ���백�������õ�Ȳ�ƣ�Ȳ���벮±������Ӧ�õ����ȡ����Ȳ�����˷�Ӧ������̼�����Ʊ���Ȳ����
2�������Լ��� �����Լ����л��ϳ���Ӧ�ü�Ϊ�㷺�����뻷�����顢ȩ��ͪ������Ӧ�������Ʊ���ͬ�ṹ�Ĵ��ȡ���Щ��Ӧ�ȿ�����̼�����ֿ��γ�����Ĺ����š�
3���ص���ȡ���� �����ص��ε��ص����ɱ���ԭ�ӡ�±�ء��ǻ������ȡ�������ڱ�����ԭ��ȡ������λЧӦ��Ӱ���ʹijЩ���Ų���ֱ�����뱽��ʱ���ɲ����ص���ȡ���ķ�����Ҫע�ⱻ��ͬ����ȡ��ʱ�ķ�Ӧ������
�ġ��л���ѧ��֪ʶ��
1�����ඨλ����
�ڶ�λ��λ����ʹ�½����ȡ������Ҫ����������λ�Ͷ�λ����λ�Ͷ�λ�칹��֮�ʹ���60%����ͬʱһ��ʹ�������±�ص����⣩�����硪O-,��N(CH3)2,��NH2,��OH,OCH3,��NHCOCH3,��OCOCH3,��R,��X(Cl��Br��I),��C6H5�ȡ�
��λ��λ����ʹ�½����ȡ������Ҫ�������ļ�λ����λ�칹�����40%����ͬʱʹ�����ۻ������硪N(CH3)3,��NO2,��CN,��SO3H,��CHO,��COCH3����COOH,��COOCH3,��CONH2,��NH3�ȡ�
2��������ӻ���
�����ӻ���ʹ�������ܶȼ�С�Ļ���,��-COOH,-COOR,-NO2,-X,-HSO3,-CHO,-CO-R�ȡ�
�����ӻ���ʹ�������ܶ�����Ļ���,��-R,-OH,-OR,-NH2,-NHCOR�ȡ�
3����ͬCԭ���л�����۷е㣺֧��Խ��е�Խ�ͣ��Գ���Խ�ߣ��۵�Խ�ߣ������л�����е��ɵ͵�������Ϊ�������� < 3,3-�������� < 2-������ <������ < 2-�����顣
�塢�л�������ļ���
ϩ������ϩ��Ȳ����������Ԫ��֬������������Ȼ�̼��Һ������ɫ
����Ȳ���Ȳ�������������Ȼ���ͭ�İ���Һ������Ȳ������ɫ������Ȳ����ͭ��ɫ������
±�������������Ĵ���Һ������±������������ͬ�ṹ��±�������ɳ������ٶȲ�ͬ����±������ϩ��ʽ±������죬��±������֮����±��������Ȳų��ֳ�����
����������Ʒ�Ӧ�ų�����������6��̼ԭ�����µĴ�������¬��˹�Լ������١��崼���崼���̱���ǣ��ٴ����ú����ǣ��������ú�Ҳ�ޱ仯��
�ӻ�ϩ�����������Ȼ�����Һ������ɫ����������ˮ�������屽�Ӱ�ɫ������
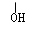 �ʻ������2��4-���������£�������ɫ��Ⱥ�ɫ����������ȩ��ͪ�������Լ���ȩ��������������ͪ���ܣ�������ȩ��֬��ȩ��ͪ��֬��ȩ��������Լ���֬��ȩ����ש��ɫ��������ͪ�ͷ���ȩ���ܣ������ͪ�;���CH3��CH���ṹ�Ĵ��õ������������Һ��
�ʻ������2��4-���������£�������ɫ��Ⱥ�ɫ����������ȩ��ͪ�������Լ���ȩ��������������ͪ���ܣ�������ȩ��֬��ȩ��ͪ��֬��ȩ��������Լ���֬��ȩ����ש��ɫ��������ͪ�ͷ���ȩ���ܣ������ͪ�;���CH3��CH���ṹ�Ĵ��õ������������Һ��
���ɻ�ɫ�ĵ�³�����
����������Լ���������������������������ܡ�
���������١��尷�����ٷ���
1�� �ñ������Ȼ�Լױ������ȣ���NaOH��Һ�з�Ӧ���������ɵIJ�������NaOH���ٰ����ɵIJ��ﲻ����NaOH��Һ���尷��������Ӧ��
2�� ��NaNO2+HCl��
֬�����������ų��������ٰ����ɻ�ɫ��״��尷����Ӧ��
���㰷�����������ص��Σ��ٰ����ɻ�ɫ��״��尷������ɫ���塣
�ǣ�����������ǣ�����ˮ����������ʹ��ˮ��ɫ�������Dz��ܡ�
��ѿ�������ǣ��������Լ�������Լ�����ѿ�ǿ�����������ש��ɫ�����������Dz��ܡ�
�ڶ�ƪ���л���ѧ����ʽ�ܽ�
�����л���ѧ����ʽ�ܽ�
һ����
1.����
����ͨʽ��CnH2n-2
��1��������Ӧ
�����ȼ�գ�CH��ȼ
4+2O2���鲻��ʹ���Ը��������Һ����ˮ��ɫ��
2+2H2O
��2��ȡ����Ӧ
һ�ȼ��飺CH��
4+Cl2���ȼ��飺CHCl+Cl ��
CH3Cl+HCl
32
���ȼ��飺CH ��
CH2Cl2+HCl
2Cl2+Cl2 CHCl3+HCl��CHCl3�ֽ��ȷ£����Ȼ�̼��CHCl ��
3+ClCCl42.��ϩ
+HCl
��ϩ����ȡ��CHCHŨ����
32OH 170��H2C=CH2��+H2O
ϩ��ͨʽ��C
nH2n
��1��������Ӧ
����
��ϩ��ȼ�գ�H2C=CH2+3O22CO2+2H2��ϩ����ʹ���Ը��������Һ��ɫ������������Ӧ��
O
��2���ӳɷ�Ӧ
����ˮ�ӳɣ�H
2C=CH2+Br�������ӳɣ�H ��
���� CH2Br��CH2Br
2C=CH2+H2CH3CH3
���Ȼ���ӳɣ�H��
2C=CH2CH3CH2Cl
��ˮ�ӳɣ�H
2C=CH2+H2CH3CH2OH
��3���ۺϷ�Ӧ
��ϩ�Ӿۣ����ɾ���ϩ��n H2C=CH 2 �� CH 3.��Ȳ
n ��Ȳ����ȡ��CaC
2+2H2
HC?CH��+Ca(OH)2��1��������Ӧ
��Ȳ��ȼ�գ�HC��ȼ
?CH+5O2 4CO2+2H2O
��Ȳ����ʹ���Ը��������Һ��ɫ������������Ӧ��
��2���ӳɷ�Ӧ
����ˮ�ӳɣ�HC?CH+Br
2
Br Br
CHBr=CHBr+Br
2CHBr2��CHBr2
�������ӳɣ�HC?CH+H
2���Ȼ���ӳɣ�HC H2C=CH2
����
?�� CH2=CHCl
��3���ۺϷ�Ӧ
����ϩ�Ӿۣ��õ�������ϩ��nCH2 2 �� n
��Ȳ�Ӿۣ��õ�����Ȳ��n HC?4.��
n
����ͬϵ��ͨʽ��CnH2n-6
��1��������Ӧ
����ȼ�գ�2C+15O��ȼ
6H62
12CO2+6H2O
ͼ1 ��ϩ����ȡ
ͼ2 ��Ȳ����ȡ
- 1 -
������ʹ��ˮ�����Ը��������Һ��ɫ�� ��2��ȡ����Ӧ �ٱ����巴Ӧ
Br
+Br +HBr
���屽��
��������Ӧ
ŨH2SO4 NO2
+HO��NO2 60
+H2O ��
���������� ��3���ӳɷ�Ӧ
+3H �������飩��
��������������
�������������Ҫ������Ҫ��ѧ���ʣ� 5.�ױ�
- 2 -
��1��������Ӧ
�ױ���ȼ�գ�C��ȼ
7H8+9O2
7CO2+4H2�ױ�����ʹ��ˮ��ɫ��������ʹ���Ը��������Һ��ɫ��
O
��2��ȡ����Ӧ
CH 3
CH3 Ũ���� N +3HNO��NO32
2
+3H2O
NO2
�ױ�������Ӧ����2��4��6-�������ױ�������������ױ����ֽ��ݶ��ݣ�TNT������һ�ֵ���ɫ���壬������ˮ������һ������ըҩ���㷺���ڹ���������ȡ� 6.������
��1��ȡ����Ӧ
�������ˮ�⣺CBr+H
2H5��2C2H5����2����ȥ��Ӧ
OH+HBr
��������NaOH��Һ��Ӧ��CH��
3CH2�� CH2=CH2��+NaBr+H2O 7.�Ҵ�
��1�����Ʒ�Ӧ
�Ҵ����Ʒ�Ӧ��2CH
3CH22CH3CH2ONa+H2�����Ҵ��ƣ�
��2��������Ӧ
�Ҵ���ȼ�գ�2CH������
3CH2OH+O22CH3CHO+2H2O ����ȩ�� ��3����ȥ��Ӧ
�Ҵ���Ũ�����������������£����ȵ�170��������ϩ��
ע�⣺�÷�Ӧ���ȵ�140��ʱ���Ҵ�������һ����ˮ��ʽ���������ѡ� 2C2H5OH Ũ����
C2H5��O��C2H5+H2O �����ѣ�
8.����
��������ɫ���壬¶���ڿ����л��������Էۺ�ɫ�����Ӿ����������ζ���۵�140��
43�棬ˮ���ܽ�Ȳ����������л��ܼ��������ж�����һ����Ҫ�Ļ���ԭ�ϡ� ��1�����ӵ����� OH ONa
+H2O
�������ƣ�
��������CO2��Ӧ��
ONa +CO+H �� OH
22 +NaHCO3
��2��ȡ����Ӧ OH
OH +3Br Br��Br
2 ��+3HBr
�����屽�ӣ�
Br
��3����ɫ��Ӧ
�����ܺ�FeCl3��Һ��Ӧ��ʹ��Һ����ɫ��
- 3 -
9.��ȩ
��ȩ����ɫ��ζ�����д̼�����ζ��Һ�壬�е�20.8�棬�ܶȱ�ˮС���ӷ���
O ��1���ӳɷ�Ӧ || ����
��ȩ��������Ӧ��CH3��C��H+H2CH3CH2OH
��
O ��2��������Ӧ || ��ȩ��������Ӧ��2CH3��C��H+O22CH3COOH �����ᣩ
��
��ȩ��������Ӧ��
��
����
CH3CHO +2Ag(NH3)2CH3COONH4+2Ag+3NH3+H2O ������泥�
ע�⣺�������백ˮ���ƶ��ɵ�������Һ�к���Ag(NH3)2OH�������������������� ����һ����������������������ȩ������Ag���й��Ʊ��ķ���ʽ��
Ag+NH3��H2O===AgOH��+NH+ 4
AgOH+2NH3��H2O===[Ag(NH3)2]++OH-+2H2O ��
��ȩ��ԭ������ͭ��CH3CHO+2Cu(OH)2CH3COOH+Cu2O��+2H2O
10.����
��1����������� ����ĵ��룺CH3COOH��2��������Ӧ
CH3COO+H
-
+
+
O
||
Ũ����
CH3��C��OH+C2H5��OH CH3��C��OC2H5+H2O ������������
��
ע�⣺��ʹ������ã���������ˮ�ķ�Ӧ����������Ӧ�� 11.��������
����������һ�ִ�����ζ����ɫ��״Һ�塣 ��1��ˮ�ⷴӦ
����
CH3COOC2H5+H2CH3COOH+C2H5OH
��2���кͷ�Ӧ
CH3COOC2H5CH3COONa+C2H5OH
���ӣ������������ת��
- 4 -
��1����ʵ��������ϩ��170�棩 ��2�������� ��3���������ܽ�ȵIJⶨ ��4��������������ˮ�⣨70��80�棩 ��5�����к��ȵIJⶨ ��6������������50��60�棩
��˵��������1������Ҫȷ�����¶��߾������¶ȼơ���2��ע���¶ȼ�ˮ�����λ�á� 3������Na��Ӧ���л����У� �����ӡ�����ȡ��������ǻ��Ļ���� 4���ܷ���������Ӧ�������У�
ȩ�����ᡢ�����Ρ��������������ǡ���ѿ�ǡ�������ȩ�������ʡ� 5����ʹ�������������Һ��ɫ�������У�
��1������̼̼˫����̼̼�����������������������ͬϵ�� ��2�������ǻ��Ļ������紼�ͷ������� ��3������ȩ���Ļ�����
��4�����л�ԭ�Ե������SO2��FeSO4��KI��HCl��H2O2�ȣ� 6����ʹ��ˮ��ɫ�������У�
��1������̼̼˫����̼̼��������������������ӳɣ� ��2�����ӵȷ������ʣ�ȡ���� ��3����ȩ�����ʣ�������
��4���������ʣ���NaOH��Na2CO3����������ԭ�D�D�绯��Ӧ�� ��5����ǿ������ԭ������SO2��KI��FeSO4�ȣ���������
��6���л��ܼ����籽�ͱ���ͬϵ����ȼ��顢���͡�����ȣ�������ȡ��ʹˮ����ɫ���л���ʳȺ�ɫ����
7���ܶȱ�ˮ���Һ���л����У������顢�屽�������������Ȼ�̼�ȡ� 8���ܶȱ�ˮС��Һ���л����У��������������һ�������� 9���ܷ���ˮ�ⷴӦ��������
±������������֬�������ǡ����ǡ������ʣ��ģ����Ρ� 10��������ˮ���л����У� ����±�������������ۡ���ά�� 11��������Ϊ������л����У�
�����к���̼ԭ����С�ڻ����4���������������⣩��һ�ȼ��顢��ȩ�� 12��Ũ���ᡢ���������·����ķ�Ӧ�У�
��������ͬϵ����������ǻ���������ˮ��Ӧ��������Ӧ����ά�ص�ˮ�� 13���ܱ������������У�
����̼̼˫����̼̼�����IJ����ͻ����KMnO4��������ͬϵ�����ȩ���ӡ� ������л��ﶼ����ȼ�գ�ȼ�ն��DZ����������� 14�������Ե��л����У����з��ǻ����Ȼ��Ļ����
15����ʹ�����ʱ��Ե������У�ǿ�ᡢǿ��ؽ����Ρ���ȩ�����ӡ�ǿ��������Ũ�ľƾ���˫��ˮ����ơ���������ȡ�
16����������������Ӧ���л�������ᡢ��˫�����ŵ��л�������ᡢ�����ʵȣ� 17������NaOH��Һ������Ӧ���л�� ��1���ӣ� ��2�����
��3��±������ˮ��Һ��ˮ�⣻����Һ����ȥ�� ��4��������ˮ�⣬�����ȷ�Ӧ�������ȷ�Ӧ�죩
- 5 -
��5�������ʣ�ˮ�⣩
18����������ɫ�仯���л���Ӧ�� 1�����������Ȼ�����Һ��Ӧ����ɫ�� 2��KMnO4������Һ����ɫ�� 3����ˮ����ɫ��
4���������ⵥ�ʱ���ɫ��
5����������Ũ����ʻ�ɫ ��ɫ��Ӧ
- 6 -
