һ��������ԭ��������
1�� ������Ҫ�����Ĺ�ϵ
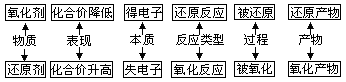
(1) ������ԭ��Ӧ�����Ƿ�Ӧ��������Ԫ�ػ��ϼ۱仯(�����ת��)�Ļ�ѧ�仯��������ԭ��Ӧ��
������ԭ��Ӧ��������Ԫ�ػ��ϼ۵�������������ԭ��Ӧ��ʵ�ʣ�����ת�ơ�
(2) ������Ӧ�ͻ�ԭ��Ӧ����������ԭ��Ӧ�У���Ӧ������Ԫ�ػ��ϼ�����(����˵����ʧȥ)���ӵķ�Ӧ��Ϊ������Ӧ����Ӧ������Ԫ�ػ��ϼ۽���(����˵�����ʵõ�����)�ķ�Ӧ��Ϊ��ԭ��Ӧ��
(3) ����������ԭ����ָ��Ӧ�����Ԫ�ػ��ϼ۽��͵����ʽ���������������Ԫ�ػ��ϼ����ߵ����ʽ�����ԭ����
(4) ���������ԭ������ָ���������Ԫ�ػ��ϼ����߱����������ò�����������������Ԫ�ػ��ϼ۽��ͱ���ԭ�����ò��������ԭ���
��ϵ��
2�� ������ԭ��Ӧ�����ֻ�����Ӧ����
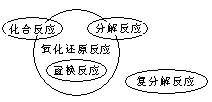
ע�⣺�е��ʲμӵĻ��Ϸ�Ӧ���е������ɵķֽⷴӦ��Ϊ������ԭ��Ӧ��
����������ԭ��Ӧ���йؼ���
1�� ������ԭ�еĵ���ת�Ʊ�ʾ��
(1) ˫���ȷ����ڷ�Ӧ���������֮���ʾ����ת�ƽ�����÷������ڱ�ʾͬһԪ�ص�ԭ�ӻ����Ӽ�ĵ���ת���������
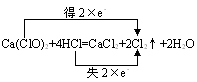
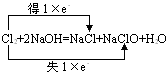
ע�⣺
1���Ŵӷ���ʽ�����ָ���Ҳࣻ
2��ͷ����ʾ��ʧ��ֻ��ʾ�仯������һ��Ҫ�������á���ʧ����
(2) �����ŷ����ڷ�Ӧ���еĻ�ԭ����������֮���ͷָ�������������彲�Ǽ�ͷ��ʧ���ӵ�Ԫ�س���ָ��õ��ӵ�Ԫ�ء���
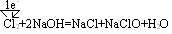
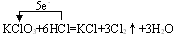

����������ԭ��Ӧ������
1����ԭ��+��������������+��ԭ����
���෴Ӧ���ص��ǻ�ԭ�����������ֱ�Ϊ��ͬ�����ʣ��μӷ�Ӧ����������ԭ��ȫ������ԭ���������й�Ԫ�صĻ��ϼ�ȫ�������仯�����磺
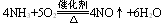
2�� ����������ԭ��Ӧ
���෴Ӧ���ص��ǻ�ԭ����������ֻ�в��ֱ�������ԭ���й�Ԫ�صĻ��ϼ�ֻ�в��ַ����仯����������ԭ��Ӧ�⣬�������������ԭ��Ӧ������
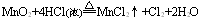
3�� ����������ԭ��Ӧ
����������ԭ��Ӧ���Է�����ͬһ���ʵIJ�ͬԪ��֮�䣬��ͬһ�������е�һ��Ԫ�ر���������һ��Ԫ�ر���ԭ�������ʼ������������ǻ�ԭ����Ҳ���Է�����ͬһ���ʵ�ͬ��Ԫ��֮�䣬��ͬһ�����е�ͬһ��Ԫ�ؼȱ������ֱ���ԭ�����磺
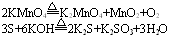
4�� ���з�Ӧ
���෴Ӧ���ص���ͬһ��Ԫ���ڲ�ͬ�ķ�Ӧ���������ּ�̬����Ӧ��ת�����м��̬����Ӧע�����ͬһ��Ԫ�ط�Ӧʱ���仯�ϼ�ֻ��£�����档����
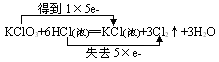
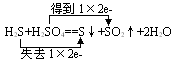
�ġ������ԡ���ԭ��ǿ�����ж�
1�������ԡ���ԭ�Ե�ǿ��ȡ���ڵ�ʧ���ӵ����׳̶ȣ����ʧ���ӵ���Ŀ�����ء���K - e-��K+��Al - 3e-��Al3+�������ݽ������˳�����Na��Al���ã�����ʧȥ���ӣ�����Na��Al�Ļ�ԭ�Ը�ǿ��
��Ԫ�صļ�̬���������̬��ֻ�������ԣ���Fe3+��H2SO4��KMnO4�ȣ���ͼ�̬��ֻ�л�ԭ�ԣ���������ʡ�Cl-��S2-�ȣ��м��̬���������������л�ԭ�ԣ���Fe2+��S��SO2�ȡ�
2�������жϷ���
(1)����Ԫ�ػ��˳���ж�
1�������˳��
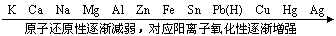
2�ǽ������˳��(����Ԫ��)
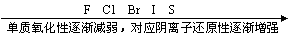
(2) ����Ԫ�������ڱ��е�λ���ж�
1ͬ����Ԫ��(���ϵ���)
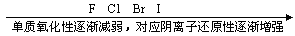
2ͬ��������Ԫ��(������)

(3)����Ԫ������������ˮ���������ǿ���ж�
���磺�����ԣ�HClO4>H2SO4>H3PO4>H2CO3�����ж������ԣ�Cl2>S>P>C��
(4)����������ԭ��Ӧ�ķ����ж�
������(������)+��ԭ��(��ԭ��)=��ԭ����+��������
�����ԣ�������>�������� ��ԭ�ԣ���ԭ��>��ԭ����
(5)������������ļ�̬�ж�
����۵Ļ�ԭ�������������������ڲ�ͬ��������ʱ�ɸ������������̬�øߵ����ж������������Ե�ǿ����
�磺��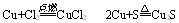 �����ж������ԣ�Cl2>S
�����ж������ԣ�Cl2>S
(6)���ݷ�Ӧ�����ж�
����ͬ����������ͬһ��ԭ����Ӧʱ��������������̬��ͬ���ɸ��ݷ�Ӧ�����ĸߵ��������жϡ����磺
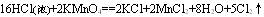
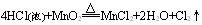
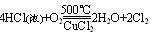
����������Ӧ�У���ԭ������Ũ���ᣬ�������ﶼ��Cl2�����������ֱ���KMnO4��MnO2��O2����һ��ʽ����KMnO4�����¼��ɰ�Ũ�����е���������������ԭ�ӣ��ڶ���ʽ����MnO2��Ҫ�ټ��������²�����ɣ�������ʽ����O2������Ҫ���ȣ����һ���ҪCuCl2��Ϊ����������ɡ��ɴ����ǿ��Եó��Ľ��ۣ�
�����ԣ�KMnO4 >MnO2>O2
(7)�������ʵ�Ũ�ȴ�С�ж�
���������Ի�ԭ�Ե���һֵŨ��Խ���������Ի�ԭ��Խǿ����֮���������Ի�ԭ��Խ�����������ԣ�
1Ũ�������ϡ����
2MnO2����Ũ���ᷴӦ��������ϡ���ᷴӦ��
����ǿ������
�� �ʣ�O3��±�ص��ʣ�X2��
�� �� �H2O2��NO2��Na2O2
�������Σ�KMnO4��K2Cr2O7(�ظ����)��NaClO��KClO3��NaNO3����������ǿ�������£���FeCl3����ǿ����
�����ŨH2SO4��ϡŨHNO3��HClO��
����ǿ��ԭ��
���ý������ʣ�H��ǰ��
SO32-��S2->I->Fe2+>Br-��H2S>H2SO3>HI>HBr�� C��H2��CO�����������£���
�塢������ԭ��Ӧ���йع���
1.�غ����
���ϼ��������н��������еñ���ʧ������һ��������������ԭ��Ӧ�����ϼ�����������ȣ���ʧ����������ȡ�
Ӧ�ã��й�������ԭ��Ӧ�ļ��㼼�ɼ���ƽ������ԭ��Ӧ����ʽ�ĸ������ݡ�
2.ǿ������
��ǿ�����Ե�����������ǿ��ԭ�ԵĻ�ԭ����Ӧ����������ԭ�ԵĻ�ԭ������������Ե��������
Ӧ�ã������������£��������Խ�ǿ�������Ʊ������Խ��������ʻ��û�ԭ�Խ�ǿ�������Ʊ���ԭ�Խ��������ʣ����ܱȽ�����֮��������Ի�ԭ�Ե�ǿ����
3.��̬����
Ԫ�ش������̬��ֻ�������ԣ�������ͼ�̬��ֻ�л�ԭ�ԣ��������м��̬���������������л�ԭ�ԣ�����һ����Ӧ�У���Ҫ����һ�����ʡ�
Ӧ�ã��ж�Ԫ�ػ����������Ի�ԭ�Ե����ޡ�
4.ת������
������ԭ��Ӧ�У���Ԫ�����ڼ�̬���ת�����ף�ͬ��Ԫ�ز�ͬ��̬֮����������Ӧ��Ԫ�صĻ��ϼ�ֻ�����������棻ͬ��Ԫ�����ڼ�̬�䲻����������ԭ��Ӧ��
Ӧ�ã������ж�������ԭ��Ӧ�е����ʱ仯���Ʋ�仯���
5.������
Խ��ʧ���ӵ����ʣ�ʧ���Ӻ��Խ�ѵõ��ӣ�Խ�õ��ӵ����ʣ��õ��Ӻ��Խ��ʧ���ӣ�һ��������ͬʱ�ͼ��ֻ�ԭ������ʱ�������뻹ԭ����ǿ�Ļ�ԭ��������Ӧ��ͬ����һ�ֻ�ԭ��ͬʱ�ͼ�������������ʱ����������������ǿ��������������Ӧ��
Ӧ�ã��ж����ʵ��ȶ��Լ���Ӧ˳��
�ڶ�ƪ��������ԭ��Ӧ�е�֪ʶ��������ϰ
��һ�� ������ԭ��Ӧ�е�֪ʶ�㡢������ϰ
һ��������ԭ��Ӧ����
1�������й�������ԭ��Ӧ����������ȷ���� ( )
A���ڷ�Ӧ�в�һ������Ԫ�صĻ��ϼ۶������仯
B���϶���һ��Ԫ�ر���������һ��Ԫ�ر���ԭ
C����������ԭ��Ӧ�У�ʧȥ���ӵ����ʣ�����Ԫ�ػ��ϼ۽���
D��������ԭ��Ӧ�ı����ǵ��ӵ�ת��
2��������ԭ��Ӧ��ʵ���� ( )
A��������ʧ�� B�����ϼ۵����� C���������������ɡ�D�����ӵ�ת��
3������������ȷ���� �� ��
A����������ԭ��Ӧ�У��������������ʲ�������ԭ��
B���ֽⷴӦ����������ԭ��Ӧ
C����Ӧ��ijԪ�ص�ԭ�ӱ�Ϊ�����ӣ����Ԫ�صĵ����ڷ�Ӧ��һ���ǻ�ԭ��
D������û�е���ת��Ҳ��û�л��ϼ������ķ�Ӧ���Ͳ�����������ԭ��Ӧ
4�����з�Ӧ�У�����������ԭ��Ӧ����( )
A��CaCO3+2HCl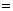 CaCl2+CO2��+H2O B��CaO+H2O
CaCl2+CO2��+H2O B��CaO+H2O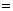 Ca(OH)2
Ca(OH)2
C��Fe+CuSO4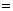 FeSO4+Cu D��
FeSO4+Cu D�� 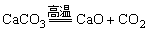
5�����з�Ӧ���ڷ�������ԭ��Ӧ����( )


A.Fe2O3+3CO====2Fe+3CO2 B.NH4NO3====N2O��+2H2O


C.2NaHCO3==Na2CO3+CO2��+H2O D.Cu2(OH)2CO3==2CuO+CO2��+H2O
6��ʵ��������������ԭ��Ӧ��ȡ�������ǣ����� ��
A��O2 H2��CO2����B��O2 CO2������C��CO2���� D��H2 O2
����������ԭ��Ӧ���Ĵ������Ӧ���͵Ĺ�ϵ
7�����з�Ӧһ������������ԭ��Ӧ���ǣ� ��
A�����Ϸ�Ӧʽ B���ֽⷴӦ C���û���Ӧ D�����ֽⷴӦ
8������˵���д������( )
A������������ԭ��Ӧ�����������Ǹ��ֽⷴӦ
B�����Ϸ�Ӧ��������������ԭ��Ӧ
C���û���Ӧһ����������ԭ��Ӧ
D���ֽⷴӦ������������ԭ��Ӧ
9����ͼ18-1����������ȷ��ʾ���ֻ������ͷ�Ӧ��������ԭ��Ӧ��ϵ��ʾ��ͼ�ǣ����� ��
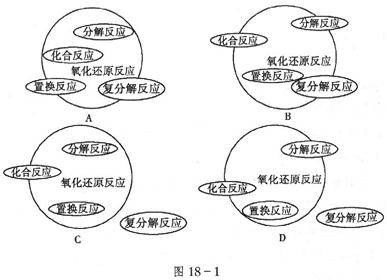
��������������ԭ��
��һ������������ԭ���������ԡ���ԭ�ԣ����������ԭ�����ж�
����һ������������ԭ�������������ԭ�����ж�
10�������з�Ӧ�У�ˮ����ԭ������( )
A��SO3+H2O=H2SO4 B��2Na+2H2O=2NaOH+H2��
C��2H2+O2 2H2O D��2F2+2H2O=4HF+O2
2H2O D��2F2+2H2O=4HF+O2
11��CaH2�����������������Ԫ���ǣ�1�ۣ���ѧ����ʽΪ��
CaH2��2H2O��Ca(OH)2��2H2��������ˮ�� ���� ��
A����ԭ�� B�����������������ǻ�ԭ��
C�������� D���Ȳ������������ֲ��ǻ�ԭ��
12����2KMnO4==2K2MnO4 + MnO2 + O2���У�KMnO4����������ǣ��� ��
A�������� B���Ȳ����������ֲ��ǻ�ԭ��
C����ԭ�� D���������������ǻ�ԭ��
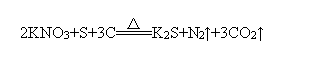
13���ڻ�ҩ�ı�ը��ӦΪ�� �����б���ԭ��Ԫ���� ( )
A��N B��C C��N��S D��N��C
14�����б�ʾSO2����ԭ�ķ�Ӧ�� �� ��
A��SO2+2H2O+Cl2==H2SO4+2HCl
B��SO2+2H2S==3S��+2H2O
C��SO2+H2O==H2SO3
D��2SO2 + O2 ===2SO3
15����05���գ����������ɶ�������ķ�Ӧ�У���Ӧ���еĺ������ʱ���������
A�� ���ڿ�����ȼ�� B�� ͭƬ��Ũ���Ṳ��
C�� ���ȵ�ľ̿��Ũ���ᷴӦ D�� ����������ϡ���ᷴӦ
16�������з�Ӧ�У����������뻹ԭ������ͬһ�����ʵ��� �� ��
A��������̼ͨ�����ȵ�̿��
B������ͭ��ľ̿�ڸ����·�Ӧ
C������ͨ�����ȵ�����ͭ
D��һ����̼ͨ�����µij�����
17��ijԪ���ڻ�ѧ��Ӧ���ɻ���̬��Ϊ����̬�����Ԫ�� �� ��
A�����ܱ����� B��һ������ԭ
C���ȿ��ܱ������ֿ��ܱ���ԭ D�����϶�����
18����K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2��+7H2O��Ӧ�У�______����������______�ǻ�ԭ����______Ԫ�ر�������______Ԫ�ر���ԭ��______���������______�ǻ�ԭ����
19��K2Cr2O7��һ�ֳȺ�ɫ����ǿ�����ԵĻ�������������������±���ԭ�����۸�ʱ����ɫ��Ϊ��ɫ���ݴˣ�����������������ʻ������ʱ���Ϳ���ǰ����������˾���������������K2Cr2O7�Ĺ轺������װ�ô����������ֹ轺��ɫ�ﵽһ���̶ȣ�����֤��˾���Ǿƺ�ݳ�����ʱ�ƾ�(CH3CH2OH)��K2Cr2O7����Ϊ����(CH3COOH)����������ԭ��Ӧ�ķ���ʽ�ɱ�ʾΪ��
2K2Cr2O7+3CH3CH2OH+8H2SO4 = 2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
����һ��Ӧ�У���������___________����ԭ����________������������________����ԭ������____________________��
���Ͷ��������ԡ���ԭ���ж�
20����������Al3+ ��Cl- ��N2 ��MnO4- ��CO2 ��H2O2 ��Fe2+ ��MnO42-
�Ⱦ����������־��л�ԭ�Ե��� ����
A���٢ܢݢ� B���ۢޢߢ� C���ܢݢޢ� D���٢ڢۢ�
21���������������������ӵ��ǣ� ��
A��Cl�� B��Cu2+ C��Fe2+ D��F��
22������Ѫ�쵰���к���Fe2+���ӣ������ʳ�������Σ���ʹ���ж�����Ϊ�������λ�ʹFe2+����ת��ΪFe3+���ӣ����ɸ���Ѫ�쵰��ɥʧ��O2�Ľ�ϵ�����������ά����C�ɻ����������ε��ж�����˵��ά����C���У� ��
A������ B������ C�������� D����ԭ��
23���Ķ����в��Ϻش���Ӧ����
һ������50Kg�Ľ����ˣ�����2g����2g���������в����Ե��ʽ�������ʽ���ڵģ�������Fe2+��Fe3+�͡�����ʽ���ڡ������������ױ����գ���ƶѪ�߲�����ʱ��Ӧ���躬���������ӵĶ������Σ�������������FeSO4��������ά����C����ʹʳ���е����������ӻ�ԭ�ɶ��������ӣ��������������ա�
��1���������о�������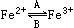 ��ת����A��Fe2+�� ����B��Fe3+�� ����
��ת����A��Fe2+�� ����B��Fe3+�� ����
��2����������ά����C����ʹʳ���е����������ӻ�ԭ�ɶ��������ӡ�����仰ָ��ά����C����һ��Ӧ���� �������� �ԡ�
24����Fe��Fe2+��Fe3+��Cl2��Cl-��Na+���������У�ֻ�������Ե��� ��ֻ�л�ԭ�Ե��� ���������������л�ԭ�Ե��� ��
25�������з�Ӧ��A��Na2O2��HCl �� H2O2��NaCl
B��Ag2O��H2O2��Ag��O2����H2O
C��H2O2 �� H2O��O2��
D��H2O2��Cr2(SO4)3��KOH �� K2SO4��H2O��K2CrO4
��1��H2O2�����������Եķ�ӦΪ������ţ�
��2��H2O2�ȱ��������ԣ��ֱ��ֻ�ԭ�Ե�Ϊ
��3��H2O2���ֳ����Ե��� ��Ϊ
��������
26�����б仯�У�һ����ӻ�ԭ������ʵ�ֵ���( )
A.Cl2��Cl- B.FeCl3��FeCl2 C.C��CO2 D.KMnO4��MnO2
27�����б仯�����������������ʵ�ֵ���
A�� CuO��CuSO4 B��CO2��CO C��Fe��Fe3O4 D��KClO3��O2
28�����б仯���������������ʵ�ֵ��� �� ��
A��CuO��Cu B��CaCO3��CaO
C��Fe��FeCl2 D��HCl��Cl2
�����������ԡ���ԭ��ǿ���Ƚ�
����һ�����ݽ������ǽ������˳����ж�

�õ�������Խǿ��Ԫ�أ�������Խǿ��ʧ��������Խǿ��Ԫ�أ���ԭ��Խǿ
30�����ж�������ԭ��Ӧ�ķ����к������� ( )
A�� Cu2+�����Ա�Na+ǿ
B�� Cl2�õ��ӵ�������Br2ǿ�����������ԣ�Cl2 ��Br2
C������������ԭ��Ӧ�����츣������
D��������ԭ��Ӧ��Ԫ�ص�ԭ�ӵ���ʧȥ��Խ�࣬��ԭ��Խǿ
�磺��ԭ����ʧȥ1�����ӣ���ԭ����ʧȥ3�����ӣ��������Ļ�ԭ�Ա���ǿ
���Ͷ�����ǿ������������ǿ�Ļ�ԭ�� �����Ļ�ԭ����������������
�����Ļ�ԭ����������������
�����ԣ�������>��������
��ԭ�ԣ���ԭ��>��ԭ����
31��05�㶫���Ӻ�ˮ�п�����ȡ�壬��Ҫ��ӦΪ��2Br��+Cl2=2Cl��+Br2������˵����ȷ����
A.�����Ӿ��������� B.�����ǻ�ԭ��
C.�÷�Ӧ���ڸ��ֽⷴӦ D.�����������Ա��嵥��ǿ
32����֪��ij�¶�ʱ��������������Ӧ��
(1)C��CO2��2CO (2)C��H2O��CO��H2 (3)CO��H2O��CO2��H2
�ݴ��жϣ����¶���C��CO��H2�Ļ�ԭ��ǿ��˳���ǣ�
A��CO��C��H2 B��C��CO��H2
C��C��H2��CO D��CO��H2��C
33�����������ĸ���Ӧ��
��1��H2S+I2=2H++2I-+S¯ ��2��H2SO3+2H2S=3S¯+3H2O
��3��2I-+Br2=2Br-+I2 ��4��H2SO3+I2+H2O=H2SO4+2HI
ȷ��Br-��I-��H2S��H2SO3��ԭ����ǿ������˳����
A��H2S>H2SO3>I->Br- B��Br->I->H2SO3>H2S
C��H2SO3>H2S>Br->I- D��I->Br->H2S>H2SO3
34����֪:��2FeCl3+2KI=2FeCl2+2KCl+I2 ��2FeCl2+Cl2=2FeCl3�ж��������ʵ����������ɴ�С��˳����
(A)Fe3+>Cl2>I2 (B)Cl2>Fe3+>I2 (C)I2>Cl2>Fe3+ (D)Cl2>I2>Fe3+
35�� �������з�Ӧ���ж�������ǿ����ȷ���ǣ� ��
��1��2H2S+O2===2S��+2H2O ��2��4NaI+O2+2H2O===4NaOH+2I2
��3��Na2S+I2===2NaI+S��
A��O2��I2��S (B) O2��S��I2 C��I2��O2��S D��S��I2��O2
36�������з�Ӧ������A��B��C��D������һ��Ԫ�أ�
2A����B2===2B����A2 2A����C2===2C��+A2 2B����C2===2C��+B2 2C����D2===2D����C2
������������ǿ�������ǣ� ��
A��A2 B��B2 C��C2 D��D2
�����������������ԡ���ԭ��ǿ���жϷ�Ӧ�ܷ����
37����05���գ���֪Co2O3��������Һ���ױ���ԭ��Co2+��Co2O3��Cl2��FeCl3��I2���������μ��������з�Ӧ��ˮ��Һ�в����ܷ�������
A��3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 B��Cl2 + FeI2 = FeCl2 + I2
C��Co2O3 + 6 HCl = 2CoCl2 + Cl2��+ 3H2O D��2Fe3+ + 2I�� = 2Fe2+ + I2
�����ģ��ж�Ԫ�صĻ��ϼ۱仯����
38��G��Q��X��Y��Z��Ϊ�ȵĺ�����������Dz��˽����ǵĻ�ѧʽ����֪��������һ�������¾������µ�ת����ϵ(δ��ƽ)�� (1)G �� Q+NaCl��
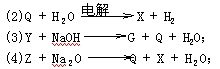
�����ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳��Ϊ( )��
A��QGZYX B��GYQZX�� C��GYZQX D��ZXGYQ��
����ʾ���ȵĺ���������һ��Cl�Ļ��ϼ�Ϊ����.��
39��G��Q��X��Y��Z��Ϊ���ȵĻ������һ���������¾�������ת����ϵ����G��Q��NaCl, ��Q��H2O��X��H2��, ��Y��NaOH��G��Q��H2O,��Z��NaOH��Q��X��H2O�����ж��ȵĻ��ϼ��ɸߵ��͵�����˳���ǡ��� �� ��
A��X>Y>Z>G>Q B��Y>X>Z>G>Q
C��G>Y>Q>Z>X D��X>Z>Q>Y>G
�����壺ѡ��������������������ԭ��
40����֪����3����Ӧ��2FeCl3+2KI=2FeCl2+2KCl+I2
2FeCl2+Cl2=2FeCl3
KClO3+6HCl=3Cl2��+3H2O+KCl
��ij��Һ����FeCl2��FeI2ͬʱ���ڣ�Ҫ����I-���õ�FeCl2��Һ��Ӧ�������� �� ��
A��FeCl3 B��Cl2 C��KClO3 D��HCl
�ġ��������ת�Ƶķ������Ŀ
41����˫���ű�ʾ����������ԭ��Ӧ�е���ת�Ʒ������Ŀ
��1��Cl2��2NaOH===NaCl��NaClO��H2O
��2��HgS + O2 === Hg + SO2
��3��2KNO3��S��3C=== K2S��N2��3CO2
��4��KClO3 + 6HCl ==== KCl + 3Cl2��+ 3H2O
42��3S��6KOH��2K2S��K2SO3��3H2O�У��������뱻��ԭ��Sԭ����֮��Ϊ
A��1 ��1 B��2 ��1 C��1 ��2 D��3 ��2
43����Ӧ8NH3��3C12��6NH4Cl��N2�У��������İ���δ�������İ����������ǣ� �� ��
A��3 ��1 B��1 ��3 C��1 ��1 D��3 ��8
44����֪6HCl + KClO3 �� KCl + 3Cl�� + 3H��O
�� (1)����H37Cl��K35ClO3��Ӧ�����������ķ������Ƕ���?��
(2)����H35Cl��K37ClO3��Ӧ�����������ķ�������Ϊ����?��
�塢������ԭ��Ӧ�ļ��㣺�����غ�
45����3Cu+8HNO3(ϡ)��3Cu(NO3)2+2NO��+4H2O��Ӧ�У�����64gCu����������ԭ��HNO3��������( )
A��168g B��42g C��126g D��60g
46����һ�������£�RO3n���ͷ����ɷ������·�Ӧ��
RO3n����F2��2OH����RO4����2F����H2O��
�Ӷ���֪��RO3n���У�Ԫ��R�Ļ��ϼ��� ���� ��
A����4 B����5 C����6 D����7
47�������з�Ӧ��11P��15CuSO4��24H2O��5Cu3P��6H3PO4��15H2SO4
�ٻ�ԭ���� ��������
�ڱ�������Pԭ�Ӹ����ͱ���ԭP�ĸ�������
��ÿ��Cu2��������Pԭ�Ӹ�����
48��R2O8n��������һ�������¿���Mn2����������ΪMnO4��,����Ӧ��R2O8n�����ӱ�ΪR042�����ӣ���֪��Ӧ��R2O8n����Mn2���ĸ���֮��Ϊ5 ��2, ��nֵ�Ƕ��٣�
�������
18��K2Cr2O7 ��HCl �� Cl �� Cr ��Cl2 ��CrCl3
19��K2Cr2O7��CH3CH2OH��CH3COOH�� Cr2(SO4)3
23����1����ԭ ������ ��2����ԭ ��ԭ
24��Na+ ��Fe ��Cl- ��Fe2+��Fe3+��Cl2
��1��B��2��C ��3��A ǿ��������
44�� ��1) Cl�� ==73.3�� (2) Cl�� ==70.7��
47����P��P��CuSO4��6:5��1/5
48��n=2
