分析化学 第二章总结
——误差及分析数据的统计处理
一. 误差与准确度:
1. 绝对误差:E=Xi-u (Xi为测定值,u为真值)
2. 相对误差:Er=[(Xi-u)/u]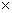 100%
100%
注:相对误差表示测定结果更为确切
3. 准确度:测定平均值与真值接近的程度,常用误差表示。
误差小,准确度高
二. 偏差与精密度
1. 绝对偏差:di=Xi-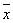 (Xi为测定值,
(Xi为测定值,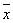 为测定结果的平均值)
为测定结果的平均值)
2. 相对偏差:dr=[(Xi-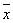 )/
)/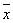 ]
]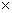 100%
100%
3. 平均偏差: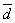 =
=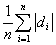 =
=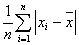
4. 相对平均偏差: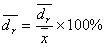
5. 标准偏差(均方根偏差): (测定次数n趋于无限多时)
(测定次数n趋于无限多时)
注意:这的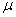 为总体平均值
为总体平均值
6.样本标准偏差: 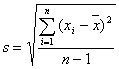 (测定次数有限)
(测定次数有限)
7.精密度:测试多次后,求出所得结果之间的一致度,用偏差表示。
注意:在偏差的表示中,标准偏差更为合理。
三. 准确度与精密度的关系
实验结果先要求精度高,才能保证有准确的结果,但高的精密度也不一定能保证有高的准确度
若没有系统误差存在,则精密度高,准确度也高
四. 误差的分类
1. 系统误差
⑴产生原因:方法错误,纯度不够,仪器缺陷,操作不当
⑵性质:重复性,单向性,可测性
⑶校正方法:选择正确方法,试剂提纯,对照试验,空白试验(除不加式样外其他步骤一样)
2. 随机误差
产生原因:由一些无法控制的不确定因素引起的
五. 随机误差的分布:
置信区间: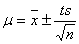 【t由置信度,测定次数两者决定可得(查t值表可得)】
【t由置信度,测定次数两者决定可得(查t值表可得)】
六. 可疑数据的取舍
1. Grubbs法
步骤:⑴将测定值按从小到大进行排列
⑵算出n个测定值的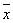 及标准偏差s
及标准偏差s
⑶ ①判断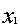 :
: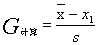
②判断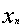 :
: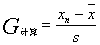
⑷若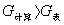 ,则
,则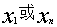 应弃去,反之则保留
应弃去,反之则保留
注意: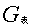 通过查表可得,其由置信度和次数决定的
通过查表可得,其由置信度和次数决定的
2. Q值检验法
步骤:⑴将测定值按从小到大进行排列
⑵ ①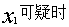 ,
,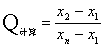
②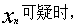
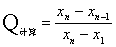
* 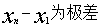
注:若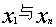 均可疑,则比较
均可疑,则比较 之差,差值大的先检验
之差,差值大的先检验
⑶若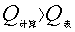 则去之,反之则保留
则去之,反之则保留
七. 有效数字及其运算规则
㈠有效数字的规则
1. 最高数字不为“0”
1.数字“0”在数据中有两种意义:①定位作用(不为有效数字);②普通数字(为有效数字).数字前面的“0”不是有效数字,数字后面的“0”是有效数字。
2.pH,pM,lgK等有效数字位数,按照对数的位数与真数的有效数字位数来定
3.[H+]= 6.3×10 -12 [mol/L] → pH = 11.20 两位
㈡修约规则
1. 当多余位数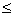 4时舍去尾数,
4时舍去尾数,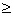 6时进位
6时进位
2. 尾数=5时:①5后数字不为0时,都进位
②5后无数字或为0,5前为奇数进位;5前为偶数舍去5
㈢运算规则
1. 加减法:以小数点后位数最少的数为准,以确定结果的小数点后的位数
2. 乘除法:以有效数字位数最少的数为准,以确定结果的有效数字
第三章 滴定分析
1.滴定分析法的分类与滴定反应的条件
(1)酸碱滴定法:用来测定酸碱
(2)沉淀滴定法:对离子进行测定
(3)配位滴定法:对金属离子进行测定
(4)氧化还原滴定法:测定具有氧化还原性质的物质及某些不具有氧化还原性质的物质
反应式:tT(滴定剂)+bB(被滴定物质)=cC+dD
适用于滴定分析法的化学反应所具备的条件:
(1) 反应定量地完成且进行完全(>99.9%)
(2) 反应速率要快
(3) 能用比较简便的方法确定滴定的终点
2.标准溶液
配制方法:
直接法:(1)物质必须具有足够的纯度,即含量≥99.9%
(2)物质的组成与化学式反应完全符合
(3)性质稳定
(4)具有较大的摩尔质量
间接法:粗略地称取一定量物质或量取一定量体积溶液,配制成接近于所需要浓度的溶液,用基准物或另一种物质的标准溶液来测定浓度。
3、标准溶液浓度表示法
物质的量浓度:CB=NB/V(N物质的量、C浓度,单位mol/L、V体积)
NB=mB/MB(m质量,M摩尔质量)
4、滴定度, 滴定度:指与每毫升标准溶液相当的被测组分的质量,用T(B/A)表示。
T(B/A)=m(B)/V(A) (g/mL) B(被测物) A(滴定剂)
aA+bB=cC+dD
mA/MA=a/b·CBVB/1000
TA/B=mA/VB=a/b·CBMA/100
5、被测组分的物质的量nA与滴定剂的物质的量nB的关系
aA+bB=cC+dD
nA:nB =a:b
∴nA=a/b·nB nB=b/a×nA
6、被测组分质量分数测定
WA=m/m试×100%
nA=a/b×nB =a/b×CB VB
nA=mA/MA
mA=a/b·(CB·VB·MA)
∴WA=(a/b·CB·VB·MA)/m试×100%
第4章 酸碱滴定
4.1酸碱平衡的理论基础
1) 酸碱质子理论:凡是能够给出质子的就是酸,凡是能够接受质子的就是碱。A.因一个质子的得失而互相转变的一对酸碱,称为共轭酸碱对。并且酸和碱可以是阴离子和阳离子,还可以是中性分子。
B.即能接受质子又能失去质子的叫做两性物质。
C.由于水分子的两性作用,一个水分子可以从另一个水分子中夺取质子而形成H3O+和OH-,这是水分子的自递作用,其平衡常数称为自递常数,用Kw表示。Kw=c(H+)*c(OH-)
2)酸碱解离平衡:酸越易给出质子,酸性就越强,其共轭碱的碱性越弱。碱越易得到质子,碱性就越强,共轭酸的酸性越弱。
4.2不同pH溶液中酸碱存在形式的分布情况——分布曲线
从酸或碱解离反应可知,当共轭酸碱对处于平衡状态时,溶液中存在着H3O+和不同的酸碱形式。这是他们的浓度称为平衡浓度。各种存在形式平衡浓度之和称为总浓度或分析浓度。某一存在形式的平衡浓度占总浓度的分数,即为该存在形式的分布系数以δi表示。
对于一元酸
δi=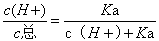
并且两种组分的分布系数之和为一,即:δ1 +δ2=1
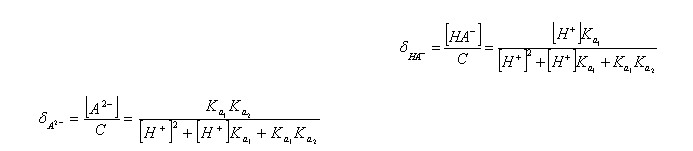
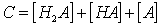 对于二元弱酸
对于二元弱酸
 三种组分的分布系数之和为一,即:δ1+δ2+δ3=1
三种组分的分布系数之和为一,即:δ1+δ2+δ3=1
4.3酸碱溶液pH的计算
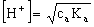 (1)当Ca
(1)当Ca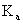 ≥10
≥10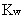 ,同时Ca/
,同时Ca/ ≥500时,最简式:
≥500时,最简式:
(2)对于两性物质的pH,在cKa2>=10Kw时,c/Ka1>=10Kw时,c(H+)=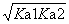
pH=0.5(pka1+pka2)
(3)对于一个多元弱酸,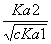 《0.05时,只考虑一步电离。
《0.05时,只考虑一步电离。
(4))缓冲溶液:共轭酸碱对,两性物质,高浓度的强酸强碱。配制原则:不干扰测定,有较大的缓冲能力,有足够的缓冲容量。对于缓冲对,当Ca/Ca接近1时,缓冲能力最大。pH=pKa+lgca/cb
缓冲能力pH=pKa+1或-1
4.4酸碱滴定指示方法
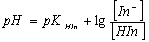
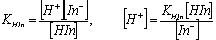 (一)变色范围
(一)变色范围
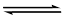 HIn H+ + In-
HIn H+ + In-
酸式 碱式
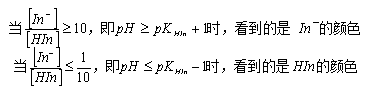
故指示剂的理论变色范围是: pH=pKHIn±1
由于人眼对深色比浅色灵敏,实际变色范围与理论推算的的变色范围并不完全相同。
pKa 理论范围 实际范围 酸色 碱色
甲基橙 3.4 2.4~4.4 3.1~4.4 红 黄
酚酞 9.1 8.1~10.1 8.0~10.0 无 红
注:一般而言,人们观察指示剂颜色的变化约有0.2~0.5pH单位的误差,称之为观测终点的不确定性,用△pH来表示,一般按△pH=±0.2来考虑,作为使用指示剂目测终点的分辨极限值。
(三)影响指示剂变色范围的因素
1. 指示剂的用量
Ø 对于双色指示剂用量多少对色调变化有影响,用量太多或太少都使色调变化不鲜明。
Ø 对于单色指示剂用量多少对色调变化影响不大,但影响变色范围和终点。
Ø 指示剂本身都是弱酸或弱碱,也会参与酸碱反应。
2. 温度:温度变时指示剂常数和水的离子积都会变,则指示剂的变色范围也随之发生改变。
3.指示剂离子强度影响pKa。
二、滴定曲线
Ø 在滴定过程中,我们把计量点附近溶液某种参数(如PH)的急剧变化称为滴定突跃
Ø 滴定百分率为99.9%至100.1%即滴定相对误差为±0.1%时,溶液某种参数(如PH)的变化范围称为滴定突跃范围。
Ø 滴定突跃范围是选择指示剂的重要依据。酸碱指示剂的选择原则:指示剂的变色范围要全部或至少有一部分落在滴定突跃范围内。
三、滴定突跃与指示剂选择
一、(1)影响滴定突跃范围的因素:
Ø 对于强酸强碱,溶液浓度越大,突跃范围越大,可供选择的指示剂愈多;浓度越小,突跃范围越小,可供选择的指示剂就越少。当突跃范围小于0.4PH时(C=10-4mol/L)就没有合适的指示剂了。
Ø 对于弱酸弱碱的滴定,浓度越大、离解常数越大,则突跃范围就越大,反之则越小。当突跃范围减小至约0.4PH时(CK=10-8),指示剂就不合适了。
Ø 当滴定试剂和被滴定物质的浓度同时增加10倍,突跃范围增加2个单位。
(2)指示剂的选择
Ø 强酸强碱的滴定,计量点时溶液呈中性,突跃范围横跨酸性区和碱性区,突跃范围较大,酸性范围内和碱性范围内变色的指示剂都可以考虑选用。
Ø 强碱滴定弱酸,计量点时溶液呈弱碱性,突跃范围较小,位于碱性区,碱性范围内变色的指示剂可以考虑选用。
Ø 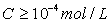 强酸滴定弱碱,计量点时溶液呈弱酸性,突跃范围较小,位于酸性区,酸性范围内变色的指示剂可以考虑选用。
强酸滴定弱碱,计量点时溶液呈弱酸性,突跃范围较小,位于酸性区,酸性范围内变色的指示剂可以考虑选用。
¨ 强酸强碱准确滴定的条件:
¨  一元弱酸弱碱准确滴定的条件:
一元弱酸弱碱准确滴定的条件:
4.5一元弱酸弱碱的滴定
1.滴定曲线
现以NaOH滴定一元弱酸HAc
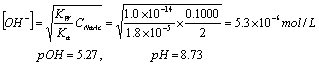 化学计量点
化学计量点
2,.强碱滴定弱酸
① 起点pH高。
② 突跃长短与Ka和c有关。
③ pH突跃小
④ 化学计量点pH>7,选用碱性范围变色指示剂。
随着弱酸pKa变小,pKa在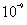 左右突跃消失。
左右突跃消失。
4-6 多元酸、混合酸和多元碱的滴定
在滴定多元酸时,在其生成两性物质的化学计量点附近,滴定突跃较小,甚至不出现,因而对多元酸测定准确度要求降低,一般允许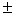 1%的终点误差,在滴定突跃>=0.4PH的情况下,要进行分部滴定需满足
1%的终点误差,在滴定突跃>=0.4PH的情况下,要进行分部滴定需满足
 C0Ka1>=
C0Ka1>=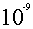 Ka1/Ka2>
Ka1/Ka2> (C0为初始浓度,允许误差
(C0为初始浓度,允许误差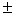 1%)
1%)
此外Ka1/Ka2越大,C0也允许低一些
2混合酸的滴定
两弱酸(HA(较强弱酸)+HB)
确定能否分布滴定条件: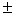 1%的终点误差和滴定突跃>PH满足
1%的终点误差和滴定突跃>PH满足
C(HA)K(HA)>=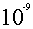 C(HA)K(HA)/ C(HBK(HB)>
C(HA)K(HA)/ C(HBK(HB)>
3多元碱的滴定(以HCl滴定Na2CO3)
 H2CO3 H++HCO3- PKa1=6.38 PKb2=7.62
H2CO3 H++HCO3- PKa1=6.38 PKb2=7.62
 HCO3- H++CO32- PKa2=10.25 PKb1=3.75
HCO3- H++CO32- PKa2=10.25 PKb1=3.75
PKb1=3.75 CO32-为中等强度弱碱,可用强酸直接滴定
由于Kb1/Kb2<104,无真正第一化学计量点,在PH=3.89附近有一滴定突跃,为第二化学计量点
[H+]1= =
=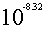 mol/l
mol/l
到达第二学计量点时即H2CO3的饱和溶液,PH=3.89
工业上使用指示剂第一化学计量点用甲酚红和百里酚蓝混合指示剂(PH=8.3)(第二学计量点用参比溶液、加热煮沸)
4-7酸碱滴定法应用示例
直接滴定一元酸碱的条件:ck>=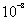
直接滴定多元酸碱的条件:ck>= K1/k2>=
K1/k2>=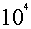
双指示法连续滴定确定物质组成(NaOH NaCO3 NaHCO3 )用盐酸滴定确定其成分
1. NaOH V1>0 V2=0
2. NaCO3 V1>0 V2>0 V1=V2
3. NaHCO3V1=0 V2>0
4. NaOH- NaCO3 V1>0 V2>0 V1>V2
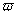 ( NaOH)=
( NaOH)=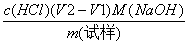
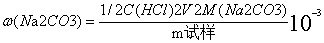
5. NaCO3- NaHCO3 V1>0 V2>0 V1
4-8酸碱标准溶液的配制
(一)酸标准溶液(HCl标准溶液)
间接配制法,基准物:无水Na2CO3,硼砂
(1用Na2CO3标定HCl,用甲基橙指示终点
缺点:易吸水,由于称量而造成的误差也稍大,终点变色也不甚敏锐
(2用硼砂标定HCl,用甲基红指示终点
优点:易得纯品,不易吸水,由于称量而造成的误差较小。
缺点:当空气相对湿度小于39%,易失去结晶水(应将其保存在湿度为60%的恒湿器中)
(二)碱标准溶液(NaOH标准溶液)
间接配制法,基准物:邻苯二甲酸氢钾(苯酸钾、草酸氢钾、二水合草酸)
用邻苯二甲酸氢钾标定NaOH,用酚酞指示终点
第5章 配位滴定法
Ø 配位滴定对反应的要求:配位比恒定;配合物稳定性高;反应迅速; 有适当方法确定终点。
Ø 配位滴定最常使用的是氨羧配位剂(使用最广的是乙二胺四乙酸EDTA)
Ø EDTA配合物特点:1.配位比简单2.稳定性高3.水溶性好4.大多无色
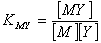 配位平衡
配位平衡
一、配合物的绝对稳定常数(稳定常数)
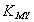 M + Y = MY
M + Y = MY
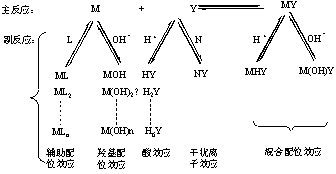 式中: 为一定温度时金属—EDTA配合物的稳定常数,此值越大,配合物越稳定;[M]为未参加配位反应的金属离子浓度;[MY]为生成的配合物浓度;[Y]为未参加配位反应的配位剂浓度。
式中: 为一定温度时金属—EDTA配合物的稳定常数,此值越大,配合物越稳定;[M]为未参加配位反应的金属离子浓度;[MY]为生成的配合物浓度;[Y]为未参加配位反应的配位剂浓度。
二、配位反应的副反应和副反应系数
副反应的发生程度以副反应系数α加以描述。
1.EDTA的副反应和副反应系数
(1)酸效应与酸效应系数

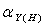 由于H+ 与Y4- 的结合使主反应的程度降低,这种现象称为酸效应。酸效应的大小用酸效应系数 来衡量。
由于H+ 与Y4- 的结合使主反应的程度降低,这种现象称为酸效应。酸效应的大小用酸效应系数 来衡量。

≥1,酸度越高(PH越小),酸效应系数就越大,酸效应就越强。 可查表。
(2)共存离子效应和共存离子效应系数
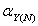 其它共存金属离子N与Y配位使主反应的程度降低,这种现象称为共存离子效应。共存离子效应的大小用共存离子效应系数 来衡量。
其它共存金属离子N与Y配位使主反应的程度降低,这种现象称为共存离子效应。共存离子效应的大小用共存离子效应系数 来衡量。

αY(N)≥1 ,N的浓度越大、KNY 越大,αY(N)就越大,共存离子效应就越强。
注:当酸效应和共存离子效应同时发生时,EDTA总的副反应系数是
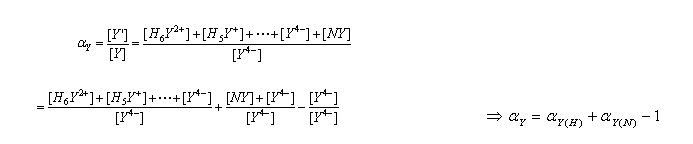
2. 金属离子的副反应和副反应系数
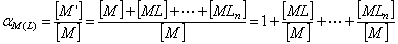
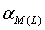 其它配位剂L与M发生配位反应,使主反应的程度降低,这种现象称配位效应,其大小用配位效应系数 来衡量。
其它配位剂L与M发生配位反应,使主反应的程度降低,这种现象称配位效应,其大小用配位效应系数 来衡量。
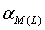

≥1。平衡时,游离L的浓度越大、ML各级配合物的稳定常数越大,αM(L)就越大,配位效应就越强。
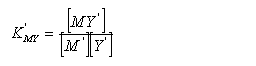
三、配合物的条件稳定常数
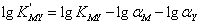 只有酸效应
只有酸效应 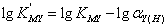
滴定基本原理
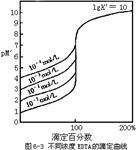
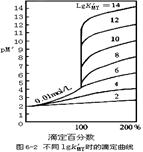 一、滴定曲线
一、滴定曲线
 影响滴定突跃范围的因素
影响滴定突跃范围的因素
 ① 一定时,浓度越大,突跃范围越大
① 一定时,浓度越大,突跃范围越大
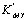 ②浓度一定时, 越大,突跃范围越大。所有对 产生影响的因素如酸效应、配位效应等,也会影响突跃范围的大小。
②浓度一定时, 越大,突跃范围越大。所有对 产生影响的因素如酸效应、配位效应等,也会影响突跃范围的大小。
二、化学计量点pM`值的计算
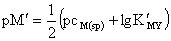 式中:
式中: 表示化学计量点时金属离子的总浓度,若滴定剂与被滴定物浓度相等
表示化学计量点时金属离子的总浓度,若滴定剂与被滴定物浓度相等 即为金属离子原始浓度的
即为金属离子原始浓度的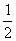
三、金属指示剂
(一)必备条件
1) 指示剂与金属离子形成的配合物与指示剂自身的颜色应有显著的区别
2) 显色反应必须灵敏、快速,并有良好的变色可逆性
3) 配合物MIn的稳定性适当,要求 >102
>102
4) 金属指示剂要控制pH,pH影响指示剂的形体从而直接影响它的颜色
(二)指示剂的封闭现象和僵化现象
1. 封闭现象:滴定达到计量点后,过量的EDTA不能夺取MIn中的金属离子,In无法释放出来,因而在计量点附近看不到溶液颜色的变化现象
产生封闭现象有两种情况:
一种情况是由被测离子引起的, >
> 。如EBT与Fe3+、Al3+生成的配合物非常稳定,置换反应不能发生。在直接滴定这些离子时,不能使用EBT指示剂。
。如EBT与Fe3+、Al3+生成的配合物非常稳定,置换反应不能发生。在直接滴定这些离子时,不能使用EBT指示剂。
另一种情况是由共存金属离子引起的,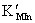 >
>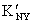 。如在pH=10时,以铬黑T为指示剂滴定Ca2+、Mg2+总量时,若含有Fe3+、Al3+、Co2+、Ni2+、Cu2+会封闭EBT。解决的办法是加入掩蔽剂,使干扰离子生成更稳定的配合物,从而不再与指示剂作用。可加三乙醇胺掩蔽Fe3+、Al3+,加KCN掩蔽Co2+、Ni2+、Cu2+。
。如在pH=10时,以铬黑T为指示剂滴定Ca2+、Mg2+总量时,若含有Fe3+、Al3+、Co2+、Ni2+、Cu2+会封闭EBT。解决的办法是加入掩蔽剂,使干扰离子生成更稳定的配合物,从而不再与指示剂作用。可加三乙醇胺掩蔽Fe3+、Al3+,加KCN掩蔽Co2+、Ni2+、Cu2+。
2. 僵化现象:有些金属-指示剂配合物难溶于水,使得滴定剂与金属-指示剂络合物置换反应缓慢,终点拖长,这种现象称为指示剂的僵化。解决的办法是加入有机溶剂或加热,以增大其溶解度,加快反应。
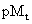 (三)指示剂理论变色点
(三)指示剂理论变色点
(计算)对于M与In的反应,只考虑In的酸效应,其它副反应忽略

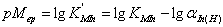

(四)常用的金属指示剂 铬黑T, 二甲酚橙
四、酸度的选择和控制
1.单一金属离子滴定的最高酸度
最高酸度可根据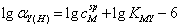 ,先计算
,先计算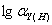 ,再查表或 酸效应曲线即可求得对应得PH
,再查表或 酸效应曲线即可求得对应得PH
2.单一金属离子滴定的最低酸度
我们把金属离子发生水解时溶液的pH值称为单一金属离子滴定的最低酸度(最高pH)。
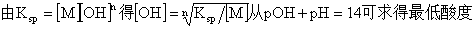
注:最高酸度和最低酸度就构成了单一金属离子M滴定的适宜酸度范围,滴定必须在该范围内进行。
3.配位滴定的选择性
(一)选择性滴定M的条件
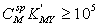 设溶液中有M和N两种金属离子共存,只考虑共存离子效应,忽略其它副反应,则计量点时
设溶液中有M和N两种金属离子共存,只考虑共存离子效应,忽略其它副反应,则计量点时
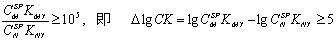 把△pH=0.2,TE≤0.3%代入林邦公式,得
把△pH=0.2,TE≤0.3%代入林邦公式,得
选择性滴定M的条件是
4.提高配位滴定选择性的途径
1. 控制溶液酸度:当△lgCK≥5时,可通过控制溶液的酸度,实现M的选择性准确滴定
2. 使用掩蔽剂
①配位掩蔽法:例:EDTA→Ca2+,Mg2+,加入三乙醇胺掩蔽Fe2+和AL3+
②沉淀掩蔽法:例:Ca2+,Mg2+时共存溶液,加入NaOH溶液,使pH>12,
Mg2+→Mg(0H)2 ,从而消除Mg2+干扰
③氧化还原掩蔽法:例:EDTA测Bi3+,Fe3+等,加入抗坏血酸将Fe3+→Fe2+
五、滴定方式
1. 直接滴定法
用EDTA标准溶液直接滴定被测金属离子。 例如 MgSO4的含量测定:Mg2+ + Y4- = MgY2-
2. 返滴定法:在试液中先加入已知量过量的EDTA标准溶液,用另一种金属盐类的标准溶液滴定过量的EDTA
返滴定法主要用于下列情况:
①缺乏符合要求的指示剂,或者被测离子对指示剂有封闭作用;
②被测离子与EDTA的络合速度很慢;
③被测离子发生水解等副反应,影响测定。
例如Al3+的测定,由于存在下列问题,不宜采用直接滴定法。
①Al3+对二甲酚授等指示剂有封闭作用。 ②Al3+与EDTA络合缓慢,
③在酸度不高时,Al3+水解生成一系列羟基配合物,
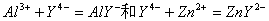 注:为了避免发生上述问题,可采用返滴定法。为此,可先加入一定量过量的EDTA标准溶液,在pH ≈ 3.5时,煮沸溶液。由于此时酸度较大(pH < 4.1),故不会发生水解;又因EDTA过量较多,故能使Al3+与EDTA配位完全。反应完全后,调节溶液 pH至 5~6(此时 AlY稳定.也不会重新水解),加入二甲酚橙,用Zn2+标准溶液进行返滴定。
注:为了避免发生上述问题,可采用返滴定法。为此,可先加入一定量过量的EDTA标准溶液,在pH ≈ 3.5时,煮沸溶液。由于此时酸度较大(pH < 4.1),故不会发生水解;又因EDTA过量较多,故能使Al3+与EDTA配位完全。反应完全后,调节溶液 pH至 5~6(此时 AlY稳定.也不会重新水解),加入二甲酚橙,用Zn2+标准溶液进行返滴定。
3. 置换滴定法:利用置换反应,置换出等物质的量的另一金属离子,或置换出EDTA,然后滴定,这就是置换滴定法。置换滴定法的方式灵活多样。
(1)置换出金属离子
被测离子M与EDTA反应不完全或所形成的络合物不稳定。可让M置换出另一络合物(如 NL)中等物质的量的N,用 EDTA滴定N,即可求得M的含量。
(2)置换出EDTA
将被测离子M与干扰离子全部用EDTA络合,加入选择性高的络合剂L以夺取 M,并释放出EDTA,用金属盐类标准溶液滴定释放出来的EDTA,即可测得M的含量。
4. 间接滴定法:有些金属离子和非金属离子不与EDTA络合或生成的络合物不稳定,这时可以采用间接滴定法。(间接滴定法手续较烦琐,引入误差的机会较多,故不是一种理想的方法。 )
应用示例
1.水的总硬度测定
水的总硬度就是水中Ca2+、Mg2+离子的总量,折算成每升含CaO或CaCO3多少mg表示,也可用度表示。
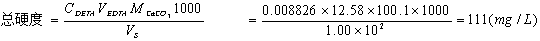 取自来水100ml,用氨性缓冲液调节PH=10,以EBT为指示剂,用0.008826mol/L的EDTA标液滴定至终点,消耗12.58ml。计算水的总硬度(CaCO3mg/L)。
取自来水100ml,用氨性缓冲液调节PH=10,以EBT为指示剂,用0.008826mol/L的EDTA标液滴定至终点,消耗12.58ml。计算水的总硬度(CaCO3mg/L)。
2.含铝化合物的含量测定
称取氧化铝凝胶0.3986克,加HCl使其溶解,转入250ml容量瓶中,稀释至刻度。精密吸取25.00ml,加入0.05000mol/L的EDTA标液25.00ml,煮沸放冷后,以XO为指示剂,
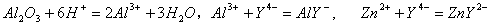 用0.05032mol/L的锌标液返滴定,用去16.02ml。计算试样中Al2O3的质量分数。
用0.05032mol/L的锌标液返滴定,用去16.02ml。计算试样中Al2O3的质量分数。
第6章 氧化还原滴法
Ø 氧化还原滴定:以氧化还原反应为基础的滴定方法。
Ø 氧化还原反应的特点:
(3)氧化还原反应机制比较复杂,反应分多步完成,常伴有多种副反应,
(4)有些反应K值很大,但速度很慢。
Ø 按选用的滴定剂的不同可分为:碘量法、高锰酸钾法、重铬酸钾法、
一、电极电势与Nernst方程
电对电极电势的大小可通过Nernst方程式计算。
对一个氧化还原半反应(也称为电极反应)
Ox + ne = Red
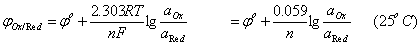 所构成的氧化还原电对用Ox/Red表示。该电对具有一定的电势称为电极电势,电极电势可以用Nernst方程表示。
所构成的氧化还原电对用Ox/Red表示。该电对具有一定的电势称为电极电势,电极电势可以用Nernst方程表示。
式中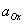 、
、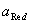 分别是游离Ox、Red的活度。式中φ0为标准电极电位,它是温度为25℃时,相关离子的活度均为1mol/L,气压为1.013×10 5Pa时,测出的相对于标准氢电极的电极电位(规定标准氢电极电位为零)。R为气体常数:8.314J/(K·mol);T为绝对温度K;F为法拉第常数(96487c/mol);n为氧化还原半反应转移的电子数目
分别是游离Ox、Red的活度。式中φ0为标准电极电位,它是温度为25℃时,相关离子的活度均为1mol/L,气压为1.013×10 5Pa时,测出的相对于标准氢电极的电极电位(规定标准氢电极电位为零)。R为气体常数:8.314J/(K·mol);T为绝对温度K;F为法拉第常数(96487c/mol);n为氧化还原半反应转移的电子数目
二、条件电极电位及其影响因素
(一)条件电极电位
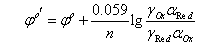
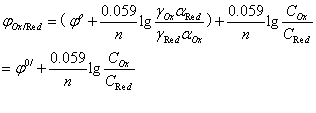
条件电位是在特定条件下,氧化态和还原态的总浓度Cox和CRed都为1mol/L时的实际电位。
(二)影响条件电位的因素
1.离子强度:溶液中盐类电解质对条件电位的影响。
2.酸效应:溶液酸度对条件电位的影响
① 氧化形或还原形是弱酸或弱碱,发生离解,其影响可由副反应系数计算。
② 半反应中有H 或OH 参加,因而条件电位的算式中应包括H 或OH 的浓度。
3.生成配合物:向溶液中加入一种配位剂,与氧化态或还原态反应。若氧化态生成稳定的配合物,则条件电位降低;若还原态生成稳定的配合物,则条件电位升高。
4.生成沉淀:加入可与氧化态或还原态生成沉淀的沉淀剂,因改变氧化态或还原态的浓度而改变电位。氧化态生成沉淀时,条件电位降低;还原态生成沉淀时,条件电位升高。
计算KI浓度为1mol/L时,Cu2+/Cu+电对的条件电位,在此条件下,Cu2+能否氧化I- ?
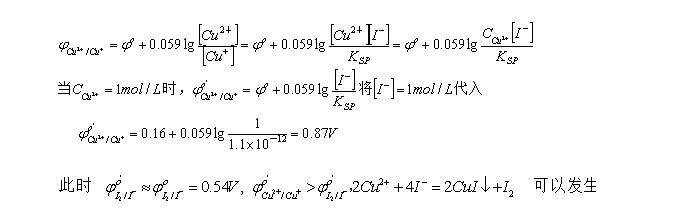
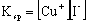 注:
注:
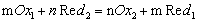 三、氧化还原反应进行的程度
三、氧化还原反应进行的程度
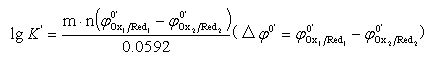
式中m、n是最小公倍数
(二)判断反应能否定量进行
要使反应定量进行,反应的完全程度应达到99.9%以上。
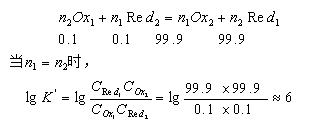
即 lgK/ ≥ 6时,反应能定量进行。
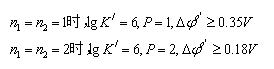
四、氧化还原反应速率及其影响因素
影响反应速度的因素很多,除了反应物本身的性质外,还与反应物的浓度、温度、催化剂等因素有关。
1.氧化剂、还原剂本身的性质:不同的氧化剂和还原剂,反应速率可以相差很大,这与它们的电子层结构以及反应机理有关。
2.反应物浓度
3.反应温度:升温可增加碰撞,使活化分子增多,加快反应。每增高100C,速度增加2~3倍
4.催化剂:加入催化剂可以改变反应的历程,因而改变反应速度。分析化学中主要利用正催化剂使反应加速,如Ce4+ 氧化AsO2- 的反应速度很慢,加入少量KI可使反应迅速进行;再如MnO4-氧化C2O42- 反应速度很慢,但反应生成的Mn2+ 对反应有催化作用,这种生成物本身起催化作用的反应叫自动催化反应。
5.诱导反应MnO4-氧化Cl-的反应进行得很慢,但当溶液中存在Fe2+时,由于MnO4-与Fe2+反应的进行,诱发MnO4-与Cl-反应加快进行。这种由一个反应的发生促进另一个反应进行的现象,称为诱导反应。例:
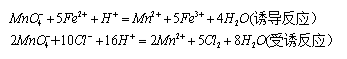
其中MnO4-称为作用体;Fe2+称为诱导体;Cl-称为受诱体。
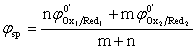
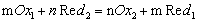 五、化学计量点点位
五、化学计量点点位
滴定 基本原理
一、滴定曲线
氧化还原滴定的突跃范围大小与反应电对条件电位差有关,条件电位差△φo/越大,滴定突跃范围越大。对称电对参与的氧化还原反应,浓度改变对突跃范围影响不大。
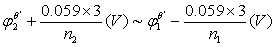 在一般氧化还原滴定中
在一般氧化还原滴定中
突跃范围是
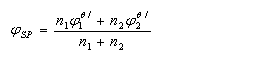
计量点是
当两个半电池反应转移电子数相等时,化学计量点电位恰好位于滴定突跃的中央;当半电池反应转移电子数不等时,化学计量点电位偏向转移电子数多的电对一方。
二、指示剂
指示氧化还原滴定终点的常用指示剂有以下四种:
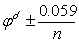 (一)氧化还原指示剂:指示剂本身是一种弱氧化剂或还原剂,它的氧化形或还原形具有明显不同的颜色。如二苯胺磺酸钠
(一)氧化还原指示剂:指示剂本身是一种弱氧化剂或还原剂,它的氧化形或还原形具有明显不同的颜色。如二苯胺磺酸钠
氧化还原指示剂变色的电位范围是
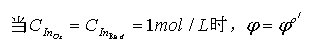
这一点称为氧化还原指示剂的变色点。
选择氧化还原指示剂时,应使指示剂的条件电位落在滴定突跃范围内,并尽可能靠近化学计量点,以减小终点误差
(二)自身指示剂:有些标准溶液本身有很深的颜色,滴定时无需另外加入指示剂,只要标准溶液稍微过量一点,即可显示终点的到达。如高锰酸钾
(三)特殊指示剂:有些指示剂本身不具有氧化还原性,但能与氧化剂或还原剂作用产生特殊的颜色,利用这种特殊颜色的出现或消失指示滴定终点,称为特殊指示剂。如淀粉
第三节 碘量法
一、基本原理
碘量法(iodimetry)是以碘作为氧化剂,或以碘化物作为还原剂,进行氧化还原滴定的方法。
(一)直接碘量法:以I2 标液为滴定剂的碘量法凡电极电位低于I2/I- 电对的,其还原形可用I2 标准溶液直接滴定。
(考点)直接碘量法只能在酸性、中性或弱碱性溶液中进行.
Ø 间接碘量法:以Na2S2O3标液为滴定剂的碘量法,包括剩余滴定和置换滴定。
• 凡标准电极电位高于I2/I- 电对的,其氧化形可将加入的I-氧化成I2 ,再用Na2S2O3 标准溶液滴定置换出来的I2 ,这种滴定方法,叫做置换碘量法
注:反应要求在中性或弱酸性溶液中进行.
• 还有些还原性物质与I2的反应速度慢,可先加入过量的I2标准溶液,待反应完全后,用Na2S2O3 标准溶液滴定剩余的I2,这种滴定方法,叫做剩余碘量法。
二、误差来源及措施
防止碘挥发的方法:
1)过量加入KI;2)在室温下进行;3)使用碘量瓶;4)快滴慢摇
防止碘离子氧化的方法:
1)溶液酸度不宜过高;2)密塞避光放置 ;3)除去催化性杂质(NO2-,Cu2+)
4)I2完全析出后立即滴定;5)滴定速度稍快
三、指示剂
碘量法中应用最多的是淀粉指示剂。
注意:
a) 滴定时应注意淀粉指示剂的加入时刻。直接碘量法,可于滴定前加入,滴定至浅蓝色出现即为终点。间接碘量法则须在临近终点时加入,滴定蓝色消失即为终点。如果过早加入,溶液中有大量碘存在,碘被淀粉表面牢固吸附,不易与Na2S2O3 立即作用,致使终点拖后。
b) 淀粉指示剂应取可溶性直链淀粉新鲜配制,放置过久会腐败变质。支链淀粉只能松动地吸附I2 ,形成一种红紫色产物,不能用作碘量法的终点指示剂。
四、标准溶液的配制与标定
(一)碘标准溶液
注:1)为了避免KI的氧化,配制好的碘标准溶液,须盛于棕色瓶中,密塞存放。
(5)碘标准溶液的准确浓度,可采用已知浓度的硫代硫酸钠溶液标定;也可用基准物As2O3进行标定。
(二)硫代硫酸钠标准溶液
硫代硫酸钠标准溶液不稳定,原因是:
a.水中溶解的CO2易使NaS2O3分解 S2O32- + CO2 + H2O → HSO3- + HCO3-+ S↓
b.空气氧化: 2S2O32-+ O2 →SO42- + S↓
c.水中微生物作用: S2O32- →Na2SO3 + S↓
在配制Na2S2O3 标准溶液,应注意以下问题:
1.采用新煮沸放冷的蒸馏水 这样既可驱除水中残留的CO2 和O2 ,又能杀死微生物。
2.加入少量Na2CO3 作为稳定剂 使溶液呈弱碱性,抑制细菌生长。
3. 贮于棕色瓶中,暗处保存,待浓度稳定后(7~10天),再进行标定。
第四节 高锰酸钾法
一、基本原理
反应需在强酸中进行,且通常为H2SO4才能全部生成Mn2+
二、指示剂
• KMnO4作自身指示剂,以出现粉红色且30秒不褪为终点。
• 若标准溶液的浓度较低(0.002mol/L以下),可选用二苯胺磺酸钠等氧化还原指示剂指示终点。
二、标准溶液的配制与标定
高锰酸钾在制备和贮存过程中,常混入少量二氧化锰杂质,蒸馏水中常含有少量有机杂质,能还原KMnO4 使其水溶液浓度在配制初期有较大变化, 因此不能用直接法配制标准溶液。间接法配制时,常将溶液煮沸以加速与其杂质的反应,并将配成的溶液盛在棕色玻璃瓶中在冷暗处放置7~10天,待浓度稳定后,过滤除去MnO2等杂质,方可进行标定。
标定KMnO4 溶液常用的基准物有:As2O3 、Na2C2O4 、H2C2O4 ·2H O等。
标定时应注意:
1. 温度:一般控制在75~85oC
2. 酸度:用H2SO4调节酸度,滴定刚开始的酸度一般应控制在约1mol/L。
3. 滴定速度:刚开始滴定的速度不宜太快
4. 催化剂:在滴定前可加几滴MnSO4溶液。
5. 指示剂:一般情况下,高锰酸钾自身可作为指示剂
三、应用与示例
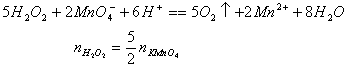 取双氧水10.00ml于100ml容量瓶中,加水稀释至刻度。取25.00ml硫酸酸化,用0.3100mol/L的KMnO4标准溶液滴定,用去31.50ml。问双氧水中H2O2的含量是多少(g/L)
取双氧水10.00ml于100ml容量瓶中,加水稀释至刻度。取25.00ml硫酸酸化,用0.3100mol/L的KMnO4标准溶液滴定,用去31.50ml。问双氧水中H2O2的含量是多少(g/L)
第五节 其他氧化还原滴定法
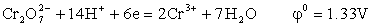 一、重铬酸钾法
一、重铬酸钾法
以二苯胺磺酸钠为指示剂
第7章 重量分析法和沉淀滴定法
重量分析法简称重量法,是通过精密称量物质的质量来进行定量分析的方法。
特点:常量分析准确,不需要标准物质。操作较烦琐、费时;对低含量组分的测定误差较大
沉淀法
利用沉淀反应将待测组分以难溶化合物形式沉淀下来,经过滤、洗涤、烘干或灼烧后,转化成具有确定组成的称量形式,称量并计算被测组分含量的分析方法。
Ø 试样的称取和溶解
在沉淀法中,试样的称取量必须适当,若称取量太多使沉淀量过大,给过滤、洗涤都带来困难;称样量太少,则称量误差以及各个步骤中所产生的误差将在测定结果中占较大比重,致使分析结果准确度降低。
取样量可根据最后所得称量形式的重量为基础进行计算。所得晶体沉淀可取0.1~0.5g,所得非晶形沉淀则以0.08~0.1g为宜。
取样后,需用适当的溶剂溶解试样,常用的溶剂是水。对难溶于水的试样,可用酸、碱及氧化物等溶剂
一、沉淀的制备
1、沉淀形式和称量形式
Ø 被测组分与试样溶液分离时,生成沉淀的化学组成称为沉淀形式;
Ø 沉淀形式经过处理,供最后称量的物质的化学组成称为称量形式。
2.沉淀法对沉淀形式的要求
(1)溶解度小(溶解损失不超过0.2mg);(2)易过滤和洗涤(沉淀颗粒粗大,比较紧密)
(3)纯净;(4)易转化成称量形式
3.沉淀法对称量形式的要求
(1)确定的化学组成(确定计量关系);(2)较大的摩尔质量(减小称量的相对误差)
(3)性质稳定(不受空气中的H2O、O2和CO2的影响)
二、沉淀的溶解度及影响因素
沉淀法中要求沉淀完全程度大于99.9%。而沉淀完全与否是根据反应达平衡后,沉淀的溶解度来判断。影响沉淀溶解度的主要因素有以下几种:
1. 同离子效应:当沉淀达平衡后,若向溶液中加入组成沉淀的构晶离子试剂或溶液,使沉淀溶解度降低的现象
沉淀剂用量: 一般 —— 过量50%~100%为宜,非挥发性 —— 过量20%~30%
2. 盐效应:溶液中存在大量强电解质使沉淀溶解度增大的现象
3. 酸效应:溶液酸度对沉淀溶解度的影响称为酸效应。
如:弱酸盐沉淀的溶解度受溶液的pH值影响很大,溶液[H+ ]大,沉淀溶解度增大。
4. 配位效应:配位剂与构晶离子形成配位体,使沉淀的溶解度增大的现象
三、沉淀的纯度及影响因素
影响沉淀纯度的原因主要有两个:共沉淀和后沉淀。
1. 共沉淀:当一种沉淀从溶液中析出时,溶液中某些本来可溶的杂质也同时沉淀下来的现象。
(1)表面吸附:由于沉淀表面吸附所引起的杂质共沉淀的现象
表面吸附是有选择性的,选择吸附的规律是:
Ø 第一吸附层:先吸附过量的构晶离子,再吸附与构晶离子大小接近、电荷相同的离子,浓度较高的离子被优先吸附
Ø 第二吸附层:优先吸附与构晶离子形成的盐溶解度小的离子。离子价数高、浓度大的离子,优先被吸附
减小方法:制备大颗粒沉淀或晶形沉淀,适当提高溶液温度,洗涤沉淀。
(2)混晶:沉淀过程中杂质离子占据沉淀中某些晶格位置而进入沉淀内部 形成混合晶体。
减小方法:将杂质事先分离除去,或加入络合剂或改变沉淀剂
(3)包藏或吸留:沉淀速度过快,表面吸附的杂质来不及离开沉淀表面就被随后沉积下来的沉淀所覆盖,包埋在沉淀内部。
减小方法:改变沉淀条件,重结晶或陈化
2. 后沉淀:溶液中某些本来可溶的杂质在沉淀放置一端时间后沉淀到原沉淀表面的现象
减小方法:缩短沉淀与母液的共置时间,或沉淀生成后,及时过滤
3. 提高沉淀纯度的措施
(1)选择合理的分析步骤 ;(2)降低易被吸附杂质离子的浓度 ;(3)选择合适的沉淀剂
(4)选择合理的沉淀条件 ;(5)必要时进行再沉淀
沉淀滴定法是以沉淀反应为基础的滴定分析法。
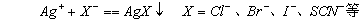 用于沉淀滴定法的反应,主要是生成难溶性银盐的反应。
用于沉淀滴定法的反应,主要是生成难溶性银盐的反应。
利用生成难溶性银盐的沉淀滴定法,习惯上称为银量法
第一节
一、滴定曲线
二、终点的指示方法
(一)铬酸钾指示剂法(Mohr法,莫尔法):以铬酸钾为指示剂的银量法。
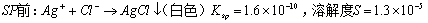 1. 原理
1. 原理
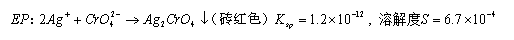
2. 滴定条件
(1)指示剂的用量要适当
(2)应在中性或弱碱性溶液中进行
(3)滴定时应剧烈摇动:AgCl对Cl -、AgBr对Br-有较强吸附,剧烈摇动可以有
效解吸附,防止终点提前。
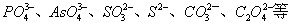 (4) 预先分离干扰离子
(4) 预先分离干扰离子
能与Ag+生成沉淀的阴离子有:
能与CrO42-生成沉淀的阳离子有: Ba2+、Pb2+等这些干扰离子应预先分离
3. 应用范围
可测CL-, Br-,Ag+ ,CN-,不可测I- ,SCN- ,因为吸附太强烈 。
(二)铁铵钒指示剂法(Volhard法,佛尔哈德法 ):以铁铵钒 NH4Fe(SO4)2 · 12H2O 为指示剂的银量法。
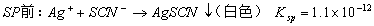 1. 原理
1. 原理
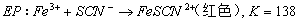 直接滴定
直接滴定

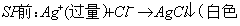 剩余滴定
剩余滴定
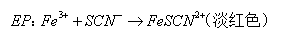
2. 滴定条件
(1)在HNO3溶液中进行:可防止Fe3+的水解,许多能与Ag+生成沉淀的阴离子如PO43-、AsO43-、CO32-等也不产生干扰。
(2)充分振摇:直接滴定时,AgSCN吸附Ag+;返滴定时,沉淀吸附Cl-、Br-、I-、SCN-
(3)指示剂的浓度要适当:理论计算指示剂的浓度(Fe3+的浓度)为0.043mol/L,但这时黄色较深,一般控制Fe3+的浓度为0.015mol/L,误差在0.1%以内。
(4)测Cl-时应防止AgCl转化为AgSCN
返滴定法测Cl-,当滴定到达终点时,AgSCN的溶度积( KSP=1.0×10 -12)小于AgCl的溶度积常数(KSP=1.8×10-10 ),沉淀转化 发生
AgCl + SCN- = AgSCN + Cl-
促使已生成的Fe(SCN)2+ 又分解,使红色褪去。
(考点)为了避免上述转化反应的发生,可以采取下列措施之一:
①将生成的AgCl沉淀滤去;②用有机物覆盖AgCl沉淀
(5)测 I – 应先加AgNO3后加指示剂
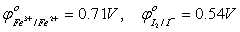 若先加指示剂,I -与Fe 3+ 反应而析出I 2 ,造成误差。其反应为:2Fe3+ + 2I-=2Fe2+ +I2
若先加指示剂,I -与Fe 3+ 反应而析出I 2 ,造成误差。其反应为:2Fe3+ + 2I-=2Fe2+ +I2
若先加AgNO3生成AgI沉淀,I-的浓度降低,电极电位升高,使Fe3+不能氧化I-
3. 应用范围
返滴定法测定CL-,Br-,I-,SCN-,直接滴定测Ag+
(三)吸附指示剂法(Fayans法,法扬司法 ):以吸附指示剂确定滴定终点的银量法。
1. 原理
AgNO3标液滴定NaCl,以荧光黄(HFl)为指示剂
终点前 HFI ==== H+ + FI-
Cl-过量 AgCl·Cl-┇M+
终点时 Ag+稍过量 AgCl·Ag+
AgCl·Ag+ + FI- ===== AgCI·Ag+┇FI-
黄绿色 淡红色
2.滴定条件
(1)溶液的酸度要适当
(2)加入糊精保护剂:可加入糊精等亲水性高分子物质,保护胶体,以防止胶体的凝聚,使AgX沉淀具有较大的表面积.
(3) 胶体颗粒对指示剂的吸附力,应略小于被测离子的吸附力
(4) 应避免在强光照射下进行滴定
3. 应用范围:可直接测定CL-,Br-,I-,SCN-和Ag +
第8章 电位法
第一节 电位法的基本原理
一、化学电池
1、化学电池的组成:由两个电极插入适当电解质溶液中组成, 可分为原电池和电解池。
原电池: 电极反应可自发进行并向外输送电流,是一种将化学能转变为电能的装置。
二、指示电极和参比电极
(一)指示电极:电极电位随电解质溶液的浓度或活度变化而改变的电极
基本要求:①符合Nernst响应;②响应速度快、重现性好;③结构简单、耐用。
离子选择性电极
以固(液)体膜为传感体 ,电极电位的产生是基于离子的交换和扩散。由于膜电极对被测特定离子有很高的选择性响应,常称为离子选择性电极。
(二)参比电极:电极电位基本不变,不受溶液组成变化的影响
基本要求:①电极电位稳定,可逆性好;②重现性好;③装置简单、耐用。
常见的参比电极有:
1.标准氢电极 (SHE)
电极组成 Pt ︳H2(1标准大气压),H+(1mol/L )
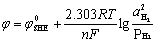 电极反应 2H+ + 2e =H2
电极反应 2H+ + 2e =H2
电极电位
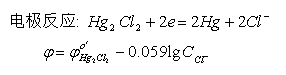
2、饱和甘汞电极(SCE)
电极组成 Hg,Hg2Cl2| KCl(sat.)
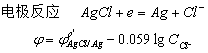 在一定温度下,内充KCl溶液浓度不变时,电极电位稳定不变。25度时,SCE的电位是0.2412V。
在一定温度下,内充KCl溶液浓度不变时,电极电位稳定不变。25度时,SCE的电位是0.2412V。
3、银 - 氯化银电极(SSE)
电极组成 Ag,AgCl|KCl(a)
在温度为25度、内充KCl浓度为0.1mol/L时,电位是0.288V.
三、原电池电动势的测量
单个电极的电位是无法测定的,必须将指示电极和参比电极插入试液中组成测量原电池,通过测量原电池的电动势得到指示电极的相对电极电位。
电池电动势(E)可表示为: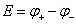
第二节 直接电位法
一、溶液pH值的测定
目前最常用的指示电极是PH玻璃电极,参比电极为饱和甘汞电极
(一)PH玻璃电极
1. 电极构造:球状玻璃膜含Na2O、CaO和SiO2,厚度约0.1mm。这种膜主要是硅酸钠晶格组成.
2.响应机理:
膜电位的产生过程:
①干玻璃膜吸水形成水化胶层:玻璃膜内、外表面与水溶液接触时,吸水形成水化凝层(厚度约10-4mm),晶格彭涨松动,有利于H+的交换和扩散。
②水化胶层中的Na+与溶液中的H+发生交换: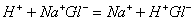 平衡后,内、外水化胶层中的H+活度分别为a2/ 和a1/。
平衡后,内、外水化胶层中的H+活度分别为a2/ 和a1/。
③水化胶层中的H+与溶液中的H+由于浓差发生扩散
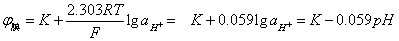
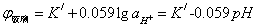
(二)测量原理和方法
1.原理
(-)玻璃电极︱待测溶液([H+] x mol/L)‖饱和甘汞电极 (+)
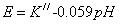
标准比较法(两次测量法):配制一个标液和试样溶液
标准溶液: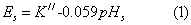
试液: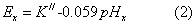
(2)-(1)得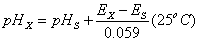
3. 注意事项
(1)在玻璃电极的适用pH范围内测定
(2)定位缓冲液的pHS值应与待测溶液的pHx值尽可能接近,相差不应超过3个pH单位
(3)标准缓冲溶液与待测溶液的温度必须相同;
(4)电极浸入溶液后需有足够的平衡时间方可读数
(5)不宜在F -含量高的溶液测定
(6)在pH精密测量中常采用两点校正法
二、离子选择电极(ISE):ISE是一种对溶液中特定离子(阴、阳离子)有选择性响应能力的电极。
(一)离子选择电极基本结构及响应机理
1.基本构造:电极膜、电极管、支持体、内参比电极和内参比溶液(填空题)
2.响应机理:电极膜浸入外部溶液时,膜内外有选择响应的离子,通过交换和扩散作用在膜两侧建立电位差,达平衡后即形成稳定的膜电位即电极电位。
有些离子选择电极的电极电位不只是通过离子交换和扩散作用建立的,还与离子缔合、配位等作用有关。
(二)离子选择性电极的分类

三、定量分析的条件和方法
(一)定量条件
常用的定量方法有直接比较法、标准曲线法和标准加入法。前两种方法都要在标液和试液中加入总离子强度调节缓冲剂(TISAB)。TISAB中含有惰性电解质、pH缓冲剂和配位剂。它有三方面的作用:
(5)使溶液的离子强度及活度系数相同
(6)②控制溶液的pH值
(7)③掩蔽干扰离子
例:典型组成(测F-):
1mol/L的NaCl,使溶液保持较大稳定的离子强度;
0.25mol/LHAc+0.75mol/LNaAc, 使溶液pH在6左右;
0.001mol/L的柠檬酸钠, 掩蔽Fe3+、Al3+等干扰离子。
(二)定量方法
1.标准比较法(两次测量法):配制一个标液和试样溶液,加入TISAB,分别测量电动势。
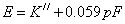
标准溶液:
试液: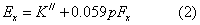
(2)-(1)得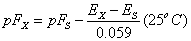
2.标准曲线法:配制系列标液和试样溶液,加入TISAB,测定系列标液的电动势,绘制E~ lgC曲线;在相同条件下测定试样溶液的电动势,并从标准曲线上求出待测离子浓度。
可通过线性回归方程求出待测离子浓度。
3.标准加入法
先测定试样溶液(CX,VX)的电动势EX,再向试样溶中加入小体积高浓度的标准溶液(CS>10CX,VS < VX/10),再测量其电池的电动势ES。
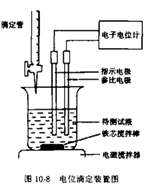
该法不用绘制标准曲线,不加TISAB,操作简便快速,准确度较高。当基体浓度较高且组成复杂时,可采用此法。
四、测量误差
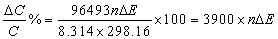
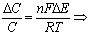 电池电动势的测量误差(△E)导致试样浓度相对误差的大小为
电池电动势的测量误差(△E)导致试样浓度相对误差的大小为
注:在25℃时,若电池电动势的测量误差△E=±0.001V,则一价离子有4%的误差,二价离子有8%的误差。
由此可见,测量结果的相对误差随离子价数n的升高而增大。故直接电位法多用于测定低价离子。
第三节 电位滴定法
一、原理与装置
电位滴定法准确度较高,易于自动化,不受样品溶液有色或浑浊的影响,但操作和数据处理麻烦、费时。除了定量分析外,还可用于某些常数的测定。
二、终点确定方法
电位滴定时,应边滴定边记录加入滴定剂的体积和电位剂读数E或pH,见典型的电位滴定数据。
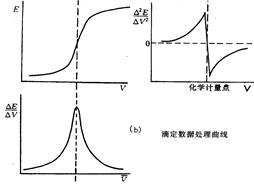
确定终点的方法有以下几种:
1.E ~V曲线法
滴定终点:曲线上的转折点(拐点)对应的体积
特点:作图简便,但要求计量点处电位突跃明显,
否则误差较大。
2.⊿E/⊿V~ V曲线法
滴定终点:曲线的最高点所对应的体积
特点:作图较麻烦,但准确度较高
3.⊿2E/⊿V2~ V曲线法
滴定终点:⊿2E/⊿V2=0处对应的体积
特点:作图麻烦,但准确度高
三、应用:可用于酸碱、配位、氧化还原和沉淀滴定。
电位滴定法除了用于定量分析,还可以用来测量某些酸碱的解离常数、沉淀的溶度积和配合物的稳定常数。
第9章 吸光光度分析法
1,如果将两种适当颜色的单色光按一定强度比例混合,也可以得到白光,我们通常将这两种颜色的单色光称为互补色光
2,对于溶液来说,它所呈现的不同颜色,是由于溶液中的质点选择性地吸收了某种颜色的光而引起的
3,朗伯-比耳定律
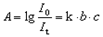
4,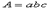 吸光系数,单位为L·g—1·cm—1
吸光系数,单位为L·g—1·cm—1
5,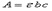 摩尔吸光系数,单位为L·mol—1·cm—1
摩尔吸光系数,单位为L·mol—1·cm—1
6,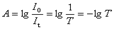
7,光度分析仪器的基本部件: 光源、单色器、吸收池、检测器和显示记录系统(指示器)。
8,入射光为单色光是朗伯-比耳定律的前提条件之一,单色器就是将光源发出的连续光分解为单色光,并可从中分出任一波长单色光的装置
9,吸收光谱 1)最大吸收波长不随浓度的变化而改变,且不同浓度溶液的吸收光谱形状是完全相似的。2)不同物质的吸收光谱形状和最大吸收波长均不相同,各种物质均有它的特征吸收光谱,以此可作为定性分析的依据;3)不同浓度的同种物质溶液,在一定波长处吸光度随溶液浓度的增加而增大。以此可作为定量分析的依据。

10. 光度测量误差:通过计算可知,一般被测溶液的吸光度在0.2~0.8或透光率在65%~15%范围内,测量的相对误差较小,能够满足准确度的要求;当 A = 0.434( T = 36.8%)时,测量的相对误差最小。
