四、离子反应
1、电解质的概念
1.1 电解质与非电解质(辨析并举例)
电解质:在水溶液里或熔融状态下能够导电的化合物。包括酸、碱、盐活泼金属的氧化物某些非金属氢化物,某些有机物。
举例NaCl固体不导电,溶于水后可以导电,所以是电解质。CaSO4、BaSO4等难溶物质在水中溶解度很小,在熔融状态下可以导电,所以这些物质也是电解质。
非电解质:在水溶液里和熔融状态下不能够导电的化合物。包括大多数有机物非金属氧化物某些非金属氢化物等。
举例:CO2、SO3、NH3、蔗糖、酒精
注:我们讨论的电解质和非电解质都是化合物,单质或混合物既不是电解质也不是非电解质。
1.2 强电解质与弱电解质(辨析并举例)
强电解质: 在水溶液里或熔融状态下全部电离成离子的电解质。包括大多数盐类、强酸、强碱。在溶液中的粒子主要是离子。
弱电解质:在水溶液里部分电离成离子的电解质包括弱酸(如HAc、H2S)、中强酸(H3PO4)弱碱(如NH3·H2O)、水。
例题:CH3COOH极易溶于水,为什么它是弱电解质, Ca(OH)2微溶于水,为什么它是强电解质?
解释:CH3COOH之所以是弱酸是因为和同浓度的强酸相比,它溶于水电离电离出的氢离子比强酸少得多,只有一部分CH3COOH发生电离产生氢离子,所以CH3COOH是弱电解质。同样,Ca(OH)2虽然微溶于水,但是它在水溶液中溶解的部分能够完全电离,所以Ca(OH)2是强电解质。
2、离子反应及离子反应方程式
离子反应定义:有离子参加的反应
2.1 离子反应的分类与条件
离子反应类型
一.非氧化还原反应的离子反应
反应发生条件:
①生成难溶的物质。如生成BaSO4、AgCl、CaCO3等。
②生成难电离的物质。如生成CH3COOH、H2O、NH3?H2O、HClO等。
③生成挥发性物质。如生成CO2、SO2、H2S等
这类反应的共同特征是朝着离子浓度减小的方向移动或者说反应物中某种离子的浓度减小,反应即可发生。
(1) 酸碱盐之间的复分解反应
a中和反应,根据参加反应的酸和碱的性质不同,又可分为强酸与强碱、强碱与弱酸、强酸与弱碱、强酸与难溶性的碱的反应等。
例如:盐酸与氢氧化钠,盐酸和氨水,盐酸与氢氧化铁反应,氢氟酸与氢氧化钠反应
b酸和盐的反应
例如:盐酸和碳酸钙的反应
c碱和盐的反应
例如:氯化镁水溶液与氢氧化钠的反应,碳酸氢钙溶液加入适量的氢氧化钠
d盐和盐的反应
例如:硝酸银溶液和氯化钠溶液反应
(2) 酸或碱与氧化物之间的反应
例如:氧化铜和盐酸的中和反应,三氧化铝与氢氧化钠溶液的反应
(3) 盐类的水解反应
例如:碳酸钠溶液呈碱性的原因,制氢氧化铁胶体
(5) 生成络离子的反应
例如:氯化铁溶液中加入硫氰化钾溶液,氢氧化铜溶于氨水:
二.氧化还原反应型的离子反应
发生的条件:反应中有电子转移。总的来说,仍然是反应物中某种离子浓度减小。
(1)电解质与电解质之间的氧化还原反应
例如:高锰酸钾与浓盐酸反应制氯气
(2)单质与电解质之间的置换反应
例如:氯水加入溴化钠溶液中
铁片放入氯化铜溶液中
(3)非置换的氧化还原反应
例如:铜与氯化铁溶液的反应:
铜与稀硝酸的反应
2.2 离子反应方程式的书写
2.2.1 离子方程式的书写步骤
大致分为四步:。
(1) 写,写出化学方程式:
(2) 改,将易溶并且易电离的物质拆开写成离子形式:
注:拆成离子形式的有:易溶且易电离的物质(强酸强碱易溶的盐)(牢记酸、碱、盐的溶解性表)写化学式的有:沉淀、气体、单质、氧化物和水等。微溶物作为反应物,若是澄清溶液写离子符号,若是浊液写化学式。微溶物作为生成物,一般写化学式(标号↓)
(3) 删,删去两边相同的离子:
(4) 查,检查反应前后各元素原子个数和电荷总数是否相等。
例题:以CuSO4与BaCl2两个溶液的的反应为例:
(1)写: CuSO4+ BaCl2=CuCl2+BaSO4↓
“写”化学方程式,必须根据实验事实;
(2)改:Cu2++SO42-+Ba2++2Cl-=Cu2++2Cl-+BaSO4↓
改反应物和生成物,以其在溶液中的主要存在形态出现;如易溶于水且易电离的物质写成离子形式,其他物质写化学式。如难溶、难电离物质、气体、单质、氧化物等。
(3)删: SO42-+Ba2+=BaSO4↓
“删”两边相同的离子,去除与离子反应无关的粒子;
(4)查两边原子个数和电荷数是否相等、反应条件、沉淀符号、气体符号等。
2.2.2 离子方程式书写的注意事项
(1)要遵循反应事实,不能臆造化学反应
如:Cu+2H+=Cu2++H2↑(错)
(2)要遵循元素原子守恒及电荷守恒,若是氧化还原反应要遵循电子守恒
(3)要遵循拆写原则(反应物和生成物都一样)
(4)不能违背约简原则
如:稀硫酸和氢氧化钡溶液反应:H++SO2-+Ba2++OH-=BaSO4↓+H2O(错)
解析:不能局部约去H+、OH-、H2O前面的计量数(系数)2,而忽视其他分子和离子。正确的为:2H++SO2-+Ba2++2OH-=BaSO4+2H2O。
(5)要注意题中有关量的关系(如过量、足量、少量等)
如:用氨水吸收少量的SO2:NH3?H2O +SO2=NH+4+HSO-(错)
正确的:2NH3?H2O+SO2=2NH4++SO2-3+H2O(要注意过量的CO2、SO2、H2S等气体分别与碱溶液或某些盐反应时生成这些气体对应的酸式根离子)
(6)关于酸式盐与量有关的离子反应方程式
一般书写时量不足的物质其参加反应的离子的物质的量之比一定要它的化学式相符合,而足量的物质其参加反应的离子的物质的量之比不一定与化学式相符合。如果没有明确的用量,写成恰好完全反应的情况。
2.2.3 与量相关的离子方程式的书写方法
2.2.3.1 复分解型(举例说明)
若是复分解反应,可令不足量系数为”1”来书写,如Ca(HCO3)2溶液中加入过量的NaOH溶液,先确定1molCa(HCO3)2含1molCa2+,2molHCO3-,再取用OH 中和2molHCO3—需2molOH,则可写Ca2++2HCO3+2OH =CaCO3+CO32-+2H2O,若是加入少量的NaOH溶液,则反应为:Ca2++HCO3+OH=CaCO3+H2。另外,NaHSO4与Ba(HCO3)2,Ca(OH)2与NaHCO3,NaH2PO4与Ba(OH)2,Al3+与NaOH,CO2与NaOH ,NaCO3 与HCl ,Mg(HCO3)2过量的NaOH等反应均与量有关。
2.2.3.2 氧化还原型(举例说明)
氧化性:Cl2 > Br2 > Fe3+ > I2 ,还原性:Cl- < Br < Fe2+ < I-
所以向FeBr2溶液中通入少量Cl2,反应的离子方程式为2 Fe2+ + Cl2 =2 Fe3+ +2Cl- ,向FeBr2溶液中通入过量Cl2,反应的离子方程式为:2 Fe2+ +4 Br-+3 Cl2 =2 Fe3+ + Br2 +6Cl-
等量的Cl2与FeBr2 反应时的离子方程式为:2 Fe2+ +2 Br- +2 Cl2 =2 Fe3+ + Br2 +4Cl-
铁和稀硝酸的反应:
铁不足时:Fe+4H+ +NO3-=Fe3++NO+2H2O
铁足量时:3Fe+8H+ +2NO3-=3Fe3++2NO+4H2O
2.2.3.3 总结常见与量有关的离子方程式的书写
(1)碳酸氢钙溶液中加盐酸:HCO3-+H+=CO2↑+H2O
(2)把金属铁放入稀硫酸中:2Fe2+6H+=2Fe3++3H2↑
(3)向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
(4)硫化钠水解:S2-+2H2O=H2S+2OH-
(5)氯气通入水中:Cl2+H2O=2H++Cl-+ClO-
(6)磷酸二氢钙溶液与氢氧化钠溶液反应:H2PO4-+2OH-=PO43-+2H2O
(7)碳酸钙与醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O
(8)碘化钾与适量溴水反应:2I-+Br2=I2+2Br-
(9)铜片与稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
(10)将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑
(11)三氯化铁溶液跟过量氨水反应:Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+
(12)小苏打溶液跟烧碱溶液反应:HCO3-+OH-=CO32-+H2O
2.3 离子方程式正误的判断
2.3.1 判断方法(总结并举例说明)
(1)看生成物是否与事实相符。
(2)看反应在什么情况下进行,能否用离子方程式表示。
(3)看表示各物质的化学式是否正确。
(4)看所用连接符号与生成物状态符号是否正确。离子互换反应的方程式通常用“=” 号连接,生成沉淀或气体则标出“↑”或“↓”符号;在离子方程式中只有某些水解反应用可逆符号,且无沉淀或气体符号;但要区别于弱电解质的电离方程式。
(5)看质量与电荷是否守恒。
(6)看离子的配比数是否正确
(7)看生成物中是否有多种沉淀与难电离电解质同时生成,正确的离子方程式全面顾及。
(8)看反应物的用量多少是否加以考虑。某些化学反应因反应物用量多少不同,生成 物也不同,甚至来源同一物质的阴、阳离子配比数也可能不同。如:“过量”、“少量”、 “等物质的量”、“适量”、“任意量”以及滴加顺序等都可能对反应产生影响。
(9)看离子符号书写是否正确。离子方程式中的易电离的电解质不仅要考虑用离子符号表示,而且还应注意离子符号书写是否完整。
例题:下列反应的离子方程式中,正确的是(D )
A.氢硫酸中滴入少量NaOH溶液:H2S + OH-=HS- + H2O (元素不守恒)
B.FeBr2溶液中通入过量Cl2:2Fe2++ 2Br-+ 2Cl2 = 2Fe3++ Br2 + 4Cl
C.碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+ OH-= CO32- + H2O(过量氢氧化钠会与水中的NH4+反应生成氨水)
D.投入足量的稀盐酸中:CO32- + 2H+ =CO2↑+ H2O(碳酸钡不应该拆写)
3、离子共存和离子推断
3.1 判断离子能否大量共存的规律
3.1.1 溶液颜色
即溶液颜色。若限定无色溶液,常见有色离子有Cu2+(蓝色)、Fe3+(棕黄色)、Fe2+(浅绿色)、MnO4-(紫色)Cr2O72- (橙色)、 Cr3+铬离子---绿色 CrO42-铬酸根离子----黄色 Cr2O72-重铬酸根离子---橙 [Fe(SCN)](2+)硫氰合铁络离子血红等有色离子。
3.1.2 溶液的酸碱性
即溶液的酸碱性。在强酸性溶液中,OH-及弱酸根阴离子(如CO32-、SO32-、S2-、CH3COO-等)均不能大量存在;在强碱性溶液中,H+及弱碱阳离子(如NH4+、Al3+、Mg2+、Fe3+等)均不能大量存在,酸式弱酸根离子(如HCO3-、HSO3-、HS-等)在强酸性或强碱性溶液中均不可能大量存在。
3.1.3 其他规律(总结并举例说明)
(1)一些特殊的规律:(1)AlO2-与HCO3-不能大量共存:AlO2-+HCO3-+H2O===Al(OH)3↓+CO32-;(2)“NO3-+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO32-等因发生氧化还原反应而不能大量共存;(3)NH4+与CH3COO-、CO32-,Mg2+与HCO3-等组合中,虽然两种离子都能水解且水解相互促进,但总的水解程度仍很小,它们在溶液中能大量共存。
(2)离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
a.复分解反应,生成难溶的物质。如生成BaSO4、AgCl、CaCO3等。生成难电离的物质。如生成CH3COOH、H2O、NH3?H2O、HClO等。生成挥发性物质。如生成CO2、SO2、H2S等
b.氧化还原反应,如Fe3+与I-、NO3-(H+)与Fe2+、MnO4-与Br-、H+与S2O32-等;
c.相互促进的水解反应,如Al3+与HCO3-、Al3+与AlO2-等;
d.络合反应,如Fe3+与SCN-等。
3.2 溶液中离子是否存在的判断
3.2.1 四大基本原
1、互斥性原则
当利用题给实验现象判断出一定有某种离子存在时,应立即运用已有知识,将不能与之大量共存的离子排除掉,从而判断出一定没有哪种离子。
2、溶液的酸、碱性原则
根据溶液的酸、碱性判断,一是初步判断可能组成那些物质,联系盐类的水解,二是在酸性或碱性溶液中哪些离子不能大量存在。
3、进出性原则
在进行离子检验时,往往需要加入试剂,这样就会引入新的离子,原溶液中是否存在该种离子就无法判断,还会有一些离子会随着实验过程中所产生的沉淀或气体而消失,有可能会对后续的实验造成影响。
4、电中性原则
在任何电解质溶液中,阴、阳离子的总电荷数是守恒的,即溶液呈电中性。在判断混合体系中某些离子存在与否时,有的离子并未通过实验验证,但我们可运用溶液中电荷守恒理论来判段其是否存在。
3.2.2 常见的离子检验方法及现象(自己总结)
一、常见阳离子的检验
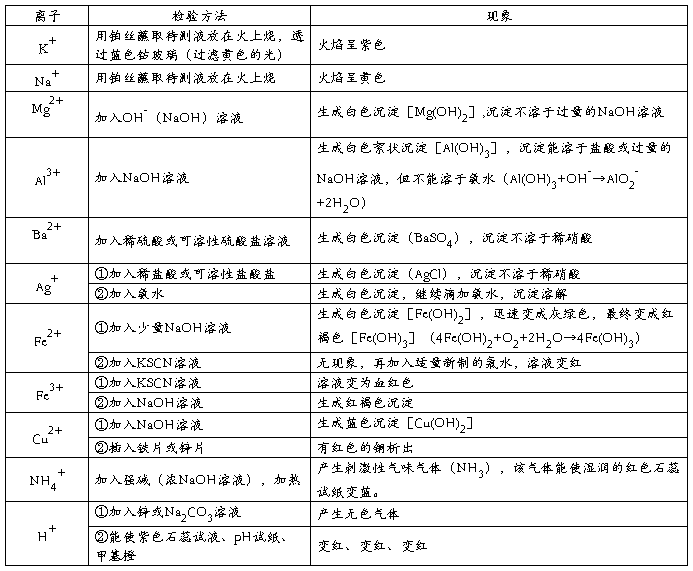
二、常见阴离子的检验去
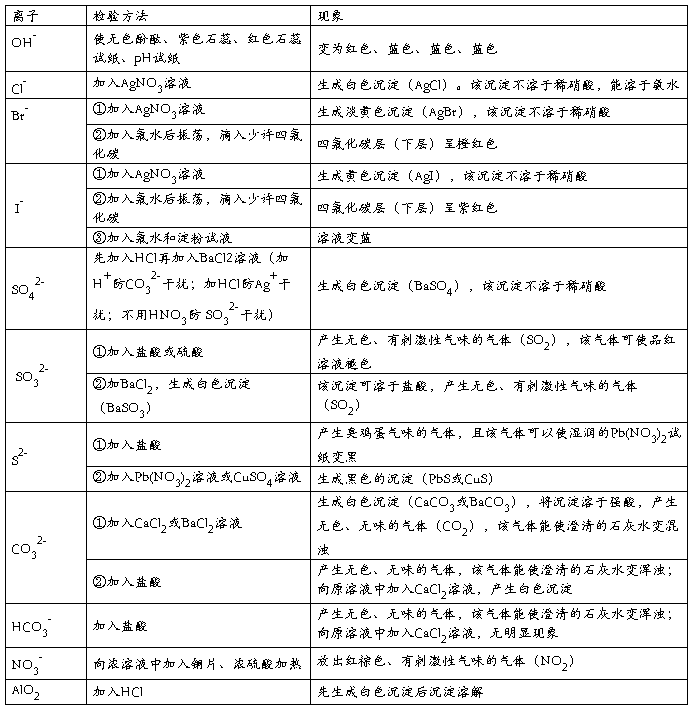
第二篇:高中化学离子反应知识点总结精讲精练
离子反应和离子方程式知识点复习
一、电解质、非电解质、强电解质、弱电解质
1.电解质、非电解质
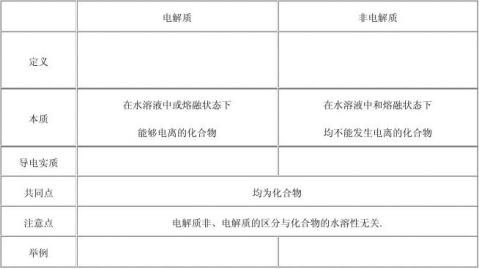
2.强电解质、弱电解质
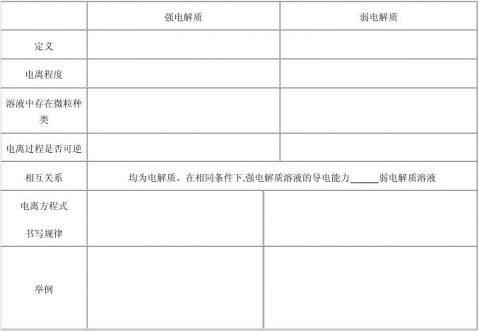
1
特别提醒:
1.电解质是指在水溶液中或熔融状态下能够导电的化合物。水溶液中或熔融状态下,这两者之间只需满足一者就行了,但必须强调的是其本身能够导电,而不是反应的生成物。如SO2、SO3的水溶液虽然能导电,但它们都不是电解质,原因是在溶液中真正起到导电作用的是它们与水反应的生成物H2SO3、H2SO4,而不是它们自己本身。Na2O的水溶液的导电虽然也是它与水反应生成的NaOH导电,但因为其在熔融状态下本身能够导电,所以Na2O是电解质。
2.电解质和非电解质都是化合物,单质它既不是电解质,也不是非电解质。
3.判断某电解质是强电解质还是弱电解质关键是看它在水溶液中电离时是完全电离还是部分电离,与其溶解度大小、导电能力强弱等因素无关。
例题现有①NaOH溶液 ②铜丝 ③液态HCl ④盐酸 ⑤稀硫酸 ⑥液氨 ⑦氨水 ⑧SO2 ⑨胆矾晶体 ⑩熔融NaCl ⑾蔗糖晶体 ⑿酒精 ⒀酒精溶液 ⒁氯气
(1)上述状态下可导电的是;?属于非电解质的是 ?上述状态下的电解质不能导电的是 _____ 。(4)本身属于非电解质,与水反应后生成电解质的是_ _ ;(5)本身既不属于电解质也不属于非电解质,与水反应后生成电解质的是_ _。
考点二 离子方程式的书写
1.
2.
3.离子方程式的书写:
1)书写规则:
①单质、氧化物、不溶物、难电离的物质(弱酸、弱碱及水等)不能拆开来写。如Cl2、Na2O等不可以拆开写成Cl-、Na+、O2-;BaSO4不可以拆开写成Ba2+、SO42-形式。
②易溶于水,易电离的物质的离子符号的改写同电离方程式中的离子形式。如NaHCO3改写Na+、HCO3-;NaHSO4应改写Na+,H+,SO42-
③微溶物,若出现在反应物中一般改写成离子符号(悬浊液除外);若出现在生成物中一般不改写。
④固体与固体物质反应不写离子方程式。如实验室制取NH3的离子方程式为:
2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
⑤浓H2SO4一般不拆开写成离子形式;HCl、HNO3无论浓稀,均应改写成离子符号。如Cu片与浓H2SO4反应的离子方程式为:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
(2)书写步骤(以CuSO4溶液与BaCl2 溶液反应为)
①写出反应的化学方程式:CuSO4+BaCl2==CuCl2+BaSO4↓
②把易溶于水、易电离的物质拆开写成离子形式,难溶的物质或难电离的物质以及气体等仍用化学式来表示。上述化学方程式可改写成:
Cu2++SO42-+Ba2+ +2Cl- =Cu2++2Cl-+BaSO4↓
③删去方程式两边不参加反应的离子符号:Ba2+ + SO42- =BaSO4↓
④检查离子方程式两边各元素的原子个数和电荷总数是否相等。
特别提醒: 常见离子方程式的书写错误
(1)不配平(一般表现为等式两边原子不守恒或电荷数不守恒)。如Fe3++Cu =Cu2++Fe2+; Na+H2O=Na++OH-+H2↑
2
(2)该改的不改或不该改的改了。如Na2O溶于水:O2- + H2O = 2OH-;大理石和稀盐酸反应:CO32-+2H+=CO2↑+H2O;醋酸铵溶液与烧碱溶液共热:CH3COONH4+OH- =CH3COO-+ NH3↑+H2O;乙醛做银镜反应:CH3CHO+2[Ag(NH3)2]OH→CH3COO-+NH4++2Ag↓+3NH3+H2O等等……
(3)与反应事实不相符合。如铁片溶于稀HCl:2Fe+6H+ =2Fe3++ 3H2↑;铝条溶于稀HNO3:2Al+6H+ = 2Al3++3H2↑
(4)不是离子反应的写离子方程式。离子反应发生在水溶液中或熔融状态下,否则就不能写离子方程式。如浓硫酸与食盐共热制HCl;浓硫酸与Cu共热制SO2;实验室制CH4和NH3等都无离子方程式。
(5)乱用↑、↓、 == 、

符号。如FeCl3溶液的水解:Fe3+ + 3H2O = Fe(OH)3↓+ 3H+;F2通入水中:2F2+2H2O=4HF+O2↑;Na2CO3的水解:CO32-+H2O=HCO3-+OH-
(6)漏写一种产物。如CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓;Ba(OH)2溶液中滴加稀H2SO4:H+ + OH- = H2O。
(7)随便约简或不约简。如Ba(OH)2溶液不断滴加稀H2SO4:Ba2++H++OH-+SO42-=BaSO4↓+ H2O;Al2(SO4)3溶液中加氨水:2Al3+ +6NH3·H2O=2Al(OH)3↓+6NH4+
三 溶液中的离子共存
1.离子共存条件:
同一溶液中若离子间符合下列任意一个条件就会发生离子反应,它们之间便不能在溶液中大量共存。 ?生成难溶物或微溶物:如:Ba2+与CO32-,Ag+与Br-,Ca2+与SO42-等不能大量共存。 ?生成气体或挥发性物质:如:NH4+与OH-,H+与CO32-、HCO3-、S2-、HS-、SO32-、HSO3-等不能大量共存。 ?生成难电离物质:如:H+与CH3COO-、CO32-、S2-、SO32-等因生成弱酸不能大量共存;OH-与NH4+因生成的弱碱不能大量共存;H+与OH-生成水不能大量共存。
?发生氧化还原反应:
氧化性离子(如Fe3+、NO3-、ClO-、MnO4-(H+)等)与还原性离子(如S2-、I-、Fe2+、SO32-等)不能大量共存。
2.附加隐含条件的应用规律: ?溶液无色透明时,则溶液中一定没有有色离子,如Cu2+、Fe3+、Fe2+、MnO4-
?强碱性溶液中肯定不存在与OH-反应的离子,如Fe3+、 Fe2+、HCO3-、NH4+、Al3+
?强酸性溶液中肯定不存在与H+反应的离子,如HCO3-、CO32-、S2-、CH3COO-、AlO2-
【典型例题】
[例1] 下列离子方程式中,正确的是( )
A. 金属钠与水反应:Na?2H2O?Na?2OH?H2?
B. 石灰石和盐酸反应:CO32????2H??CO2??H2O
??C. 氢氧化钡溶液和稀硫酸反应:H?OH?H2O
D. 过量的二氧化碳和石灰水反应:CO2?OH??HCO3
[例2] 在强酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
A. Ca
??2?、Na、NO3、SO4???2? B. Mg2?、Cl、Al?3?、SO42? ?2??3?C. K、Cl、HCO3、NO3 D. Ca、Na、Fe、NO3 ??
[例3] (1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液显中性,请写出发生反应的离子方程式:
3
(2)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式。
1. 能用H??OH??H2O来表示的化学反应方程式的是( )
A. H2SO4?Ba(OH)2?BaSO4??2H2O
B. Cu(OH)2?2HCl?CuCl2?2H2O
C. KOH?HCl?KCl?H2O
D. NaOH?CH3COOH?CH3COONa?H2O
2. 下列离子在强碱性条件下,能大量共存的是( )
2????A. K、Ba、HCO3、Cl B. Na、K、CO3、Cl ???2?
C. NH4、K、SO4??2?、S2? D. Fe、Na、Cl、NO3
?3????3. 下列反应的离子方程式正确的是( ) A. 碳酸氢钙溶液跟稀HNO3反应HCO3?H??H2O?CO2?
B. 饱和石灰水跟稀HNO3反应 Ca(OH)2?2H??Ca2??2H2O
C. 向稀氨水中加入稀盐酸 NH3?H2O?H??NH4?H2O
D. 碳酸钙溶于醋酸溶液 CaCO3?2H??Ca2??H2O?CO2
4. 下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是( )
A. Cu(OH)2和盐酸;Cu(OH)2和CH3COOH
B. BaCl2和Na2SO4;Ba(OH)2和(NH4)2SO4
C. NaHCO3和NaHSO4;Na2CO3和NaHSO4
D. NaHCO3(过量)和Ca(OH)2;Ca(HCO3)2和NaOH(过量)
5. NaHCO3溶液和NaHSO4溶液混合后,实际参加反应的离子是( )
?A. H和CO3 B. HCO3和HSO4 C. Na、HCO3和H D. HCO3和H ??2???????
6. 下列各组离子在水溶液中能大量共存的是( )
3????A. Fe、K、Cl、OH B. K、Na、SO4
???2?、NO3 ?????C. K、HCO3、Cl、CO3 D. H、Na、Cl、OH ?2??
7. 下列各组离子中,在酸性溶液中能大量共存,并且溶液为无色透明的是( )
A. Ca2?
???2??、Na、NO3、Cl B. K、Ba、Cl、NO3 ???C. Na、HCO3、CO3、K D. Na、Cl、K、MnO4
9. 用一种试剂除去下列各物质中的杂质(括号内物质)写出所用试剂及离子方程式。
(1)CO2(HCl):试剂(2)O2(CO2):试剂
10. 某河边两旁有甲、乙两厂,它们排放的工业废水中,共含K、Ag、Fe、Cl、OH、??2???????3???NO3六种离子。
甲厂的废水明显呈碱性,故甲丁废水中所含的三种离子是
乙厂的废水中含有另外三种离子。如果加入一定量 (填“活性炭”、“硫酸亚铁”、“铁粉”)可以回收其中的金属 (填写金属元素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的 (填写离子符号)转化为沉淀。经过滤后的废水主要含 可用来浇灌农田。
4 ?
