有机化学实验
一、复习要点
1.反应原理(方程式); 2.反应装置特点及仪器的作用; 3.有关试剂及作用;
4.反应条件; 5.实验现象的观察分析与记录; 6.操作注意事项;
7.安全与可能事故的模拟处理; 8.其他(如气密性检验,产物的鉴别与分离提纯,仪器的使用要领).
二、性质实验
(一)物理性质实验
现行中学化学教材中,真正涉及有机物物理性质的实验只有两个:
1.石油的分馏
实验:装配一套蒸馏装置,将100mL 石油注入蒸馏烧瓶中,再加几片碎瓷片以防石油暴沸。然后加热,分别收集60℃~150℃和150℃~300℃时的馏分。
现象与解释:石油是烃的混合物,没有固定的沸点。在给石油加热时,低沸点的烃先气化,经过蒸馏分离出来;随着温度的升高,高沸点的烃再气化,经过蒸馏后又分离出来。收集到的60℃~150℃时的馏分是汽油,150℃~300℃时的馏分是煤油。
2.蛋白质的盐析
实验:在盛有鸡蛋白溶液的试管里,缓慢地加入饱和(NH4)2SO4或Na2SO4溶液,观察现象。然后把少量带有沉淀的液体加入盛有蒸馏水的试管里,观察沉淀是否溶解。
现象与解释:有沉淀的析出,析出的沉淀可以溶解在水中。向蛋白质溶液中加入某些浓的无机盐溶液后,蛋白质的溶解度减小,使蛋白质凝聚析出,这种作用叫盐析。盐析是一个可逆的过程。
(二)化学性质实验
1.甲烷
(1)甲烷通入酸性KMnO4溶液中
实验:把甲烷通入盛有酸性KMnO4溶液的试管里,观察紫色溶液是否有变化?
现象与解释:溶液颜色没有变化。说明甲烷与酸性KMnO4溶液不反应,进一步说明甲烷的性质比较稳定。
…… …… 余下全文


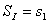 ,
,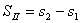 ,
,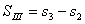 ,
,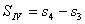 ,
,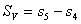 ,
,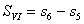
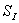 、
、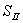 、
、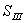 、
、 、
、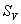 、
、 基本相等,则可判定物体在实验误差范围内作匀速直线运动。
基本相等,则可判定物体在实验误差范围内作匀速直线运动。