免疫组织化学染色原理和操作步骤
一、免疫组织化学原理
免疫组织化学(IHC)又称免疫细胞化学,是根据抗原—抗体特异性结合的原理,应用带有可见标记的特异性抗体作为探针,检测组织和细胞中抗原性物质的一种技术。免疫组化技术主要有直接法和间接法:直接法是以标记的一抗孵育标本以检测其中的抗原成分;间接法则先后加入一抗和二抗,形成抗原—一抗—二抗复合体以达到检测该抗原的目的,该法因二抗的放大作用而具有较高的敏感性。间接法常用的有过氧化物酶—抗过氧化物酶(PAP)法、亲和素—生物素—过氧化物酶(ABC)法和链霉亲和素—过氧化物酶(SP)法。
PAP法一抗和二抗均不标记,避免了标记过程对抗体活性的影响,但需要制备过氧化物酶的抗体,与适量过氧化物酶混合形成PAP复合物(含3个酶分子和2个抗体分子),染色时依次加入一抗、二抗、PAP复合物孵育标本,最后用H2O2和二氨基联苯(DAB)为底物显示过氧化物酶,即可检测标本中的抗原成分。
生物素为含硫的杂环单羧酸,可通过其羧基与蛋白质中的氨基结合,从而标记抗体和酶。亲合素又称抗生物素蛋白,与生物素有很高的亲合力,1分子亲合素可结合4分子生物素,ABC法即在此基础上建立。ABC法与PAP法相似,一抗不标记,二抗用生物素标记,染色前按一定比例将亲和素与生物素标记的过氧化物酶混合,制成ABC复合物,并使亲合素分子上至少空出一个生物素结合位点。在标本孵育过一抗和二抗后,再加入ABC复合物使其结合到二抗的生物素上,最后加入DAB进行显色。ABC法的敏感性较PAP法更高。
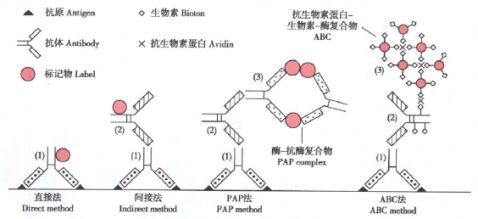
图1. 免疫组织化学基本原理示意图(引自八年制《组织学与胚胎学》)
SP法与ABC法相似,其不同于ABC法之处在于用
生物学特性与亲和素相似的链亲和素标记过氧化物酶
(图2)。在标本孵育过一抗和二抗后,加入链亲和素标
记的过氧化物酶使其结合到二抗的生物素上,最后加入
DAB进行显色。与亲和素相比,链酶亲和素的结合力与
亲和素相似而非特异性结合较亲和素低。SP法简化了操
作步骤,同时也减少了非特异性背景,是目前应用最为
广泛的免疫组化染色技术。本实验室也采用SP法进行常
规免疫组化染色。
二、实验准备:
1. 标本准备(取材信息了解)
①石蜡包埋组织切片:
石蜡包埋组织切片由病理室常规制备,具体流程见样本库相关文件。
注意:实验前应充分了解组织的取材和处理过程,组织固定材料、固定方法、固定时间、石蜡包埋过程、切片批次、切片保存条件和保存时间都可影响实验结果。要确认临床诊断信息、切片HE报告和病人临床信息,明确所选切片是否可用。
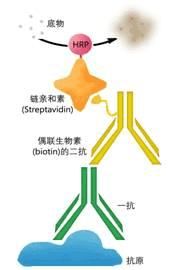
图2. SP法原理示意图
②冰冻组织切片:由病理室常规处理。
③细胞爬片:将无菌盖玻片置于六孔板中,接种细胞,待细胞生长达到60%以上后取出玻片,4%多聚甲醛固定2 h。
2. 试剂准备
①? 抗体选择
单克隆抗体针对单一表位,具有较高的特异性,但在该表位破坏后将得不到阳性结果;多克隆抗体表位针对多个表位,可避免单克隆抗体的缺点,但是可能出现非特异性杂交,敏感性好。因此,在选择抗体应注意如下方面:
(1)一定要明确是能够做IHC的抗体,抗体说明书必须有IHC测试结果,如有免疫荧光测试结果更佳。
(2)查找该分子的相关文献报道,选择文献上常用的经典抗体,但是不能迷信文献,尤其是影响力较低的文献。临床诊断用抗体须选择政府部门批准用于诊断的抗体。
(3)注意抗体品牌的信誉,了解同行使用经验。
(4)了解抗体的克隆号和抗原肽序列,明确抗体的交叉反应性。
(5)一些极昂贵的低效价抗体可探索回收利用方法。
②二抗试剂盒
目前本实验室所用二抗试剂盒为Life Technologies Histostain-Plus Kit (HRP, Broad Spectrum),货号85-9043,一抗反应性有小鼠、大鼠、兔和豚鼠。
③DAB试剂盒
目前本实验室所用为迈新加强型DAB显色试剂盒,货号DAB-2032。 ④其他试剂
二甲苯、无水乙醇、苏木素、中性封片树脂、柠檬酸钠、APES胶
3. 抗体特异性验证
所有免疫组化抗体均须Western blot验证抗体特异性,并需免疫荧光实验验证抗原定位。
4. 耗材准备
免疫组化笔或者蜡笔、盖玻片、载玻片
5. 溶液配制
①磷酸盐缓冲液(PBS)
10×PBS母液配制
NaCl 72 g
37.3 g
4.3 g Na2HPO4·12H2O KH2PO4
加蒸馏水至1000 ml,充分混匀贮存。
使用时用蒸馏水10倍稀释,调整pH值至7.3—7.4。
注意:PBS的pH值对抗体的结合力有很大影响,配制时须用酸度计精密测定并调整。调整pH值幅度过大会增加调整次数,导致溶液盐离子浓度升高。
②柠檬酸抗原修复液
抗原修复使用柠檬酸-磷酸氢二钠缓冲液,配方如下:
称取柠檬酸10.5 g,溶于500 ml蒸馏水;称取Na2HPO4·12H2O 57.3g,溶于800 ml蒸馏水。分别量取358 ml柠檬酸溶液和642 ml Na2HPO4溶液,充分混匀后调整pH值至6.0,即得2×母液,贮存备用。 ③1%盐酸酒精
浓盐酸与75%酒精按照1:99比例混合,充分混匀。
6. 免疫组化预实验
预实验的目的在于探索实验条件和方法,直接决定后期实验结果,主要注意如下方面:
(1)最佳抗体稀释浓度设定:可根据抗体说明书来设定抗体稀释梯度,也可根据文献报道设置抗体稀释梯度,最终确定合适的抗体稀释浓度。
(2)抗原修复方法和修复液的选择:不同抗体不同组织可能有不同的修复方法,查阅相关文献,比较不同修复方法和修复液的差异。通过前期实验比较,本实验室常规采用柠檬酸高压修复法。
(3)显色方法选择:SP法显色有二步法和三步法,二步法较三步
法操作简单,特异性较好,但敏感性不及三步法。因此临床诊断多用二步法,而科学实验常选择三步法。本实验室根据以往经验,常规采用三步法显色。
(4)每次预实验均须设阳性对照和阴性对照,对于前次实验已经确定特异性的抗体,可只设阳性对照。
三、免疫组化操作步骤
1. 烤片
60℃烤片30 min以上。
2. 组织片脱蜡水化
①将组织片依次放入3个装有二甲苯溶液的玻璃缸中浸泡,每缸15 min。
②依次放入2个装有无水乙醇的玻璃缸,每缸5 min。
③依次放入2个装有95%乙醇的玻璃缸,每缸5 min。
④依次放入90%乙醇、85%乙醇、75%乙醇的玻璃缸,每缸2 min,取出。
⑤放入PBS的玻璃缸中清洗,重复3次。
3. 抗原修复
将切片浸入1×柠檬酸-磷酸氢二钠缓冲液中,高压煮沸后继续加热2 min,然后停止加热让切片自然冷却。
注意:抗原修复过度或不足,均会影响最终染色结果。切片骤冷可致脱片,必须自然冷却!
4. 封闭内源性过氧化氢酶
①放入3% H2O2溶液的玻璃缸中,浸泡15 min。
②放入蒸馏水的玻璃缸中清洗,重复3次。
③放入PBS缓冲液的玻璃缸中,浸泡5 min。
5. 抗体杂交
①甩去PBS余液,将组织片平辅在湿盒中,加正常山羊血清1滴20 ?l(试剂盒中的A液,根据组织大小调整用量),28℃放置20 min,甩干。
②加稀释好的一抗1滴(20~50 ?l,根据组织块大小进行调整),置于湿盒4℃过夜。
③置PBS缓冲液的玻璃缸中,缓慢振荡清洗5 min,更换PBS缓冲液,同法操作4次,甩干。
④加入生物素偶联的二抗20~50 ?l(试剂盒中的B液,根据组织块大小进行调整),放置湿盒,37℃放置20 min。
⑤置PBS缓冲液的玻璃缸中,缓慢振荡清洗5 min,更换PBS缓冲液,同法操作3次,甩干。
6. 显色
①加链亲和素—辣根过氧化物酶20~50 ?l(试剂盒中的C液,根据组织块大小进行调整),湿盒内28℃放置5~20 min,甩干。
②置PBS缓冲液的玻璃缸中,缓慢振荡清洗5 min,更换PBS缓冲液,同法操作3次,甩干。
③滴加新鲜配制的DAB工作液100 ?l(以覆盖组织为宜),放置观察反应部位呈现黄褐色时(约5 min),置装有自来水玻璃缸中涮洗3次。
注意:DAB显色5 min即可达到平台期,之后延长显色时间并不能加深颜色,决定最终显色深浅的是一抗浓度。
7. 复染
浸入苏木精溶液中复染,放置5 min后,用自来水反复涮洗至水不变色,再用1%盐酸酒精分化1—2 s后,自来水冲洗后,反蓝水洗2 min。
8. 脱水、透明和封片
①依次放入95%、95%乙醇溶液的玻璃缸中,每缸浸泡5 min,取出;
②依次放入2个无水乙醇的玻璃缸中,每缸浸泡5 min,取出。 ③依次放入2个装有二甲苯的玻璃缸中,每缸浸泡5 min,取出。 ④滴加适量中性树胶,封片,晾干。
9. 注意事项
①整个染色过程中组织块要保持湿润,不能干片,否则会导致非特异性染色。
②组织切片边缘易干,因此抗体、封闭液、显色液等试剂要充分覆盖组织块,避免干片。
四、结果判读
判读结果前必须掌握目标组织的组织学和细胞学特点,选择正确的目标组织,才能对结果作出正确评价。阅片时应注意抗原的组织定位和细胞定位,比较不同组织、不同细胞之间的差异,以及同一组织不同细胞群的表达差异。
1. 阳性细胞判断
DAB显色呈黄色。每批染色都要有特异性阳性和阴性对照为基础,才能对染色结果作出判断。抗原表达必须在特定部位,对于临床诊断来说,不在抗原所在部位的阳性着色,一概不能视为阳性。尽量避开出血、坏死、切片刀痕和组织切片边缘,这些边缘区域由于液体表面张力而具有较高的抗体浓度,因而着色较深,边缘着色不能视为阳性。为避免边缘效应,实验时液体应充分覆盖组织,至少超过边缘2 mm,免疫组化笔圈组织应离边缘3 mm以上,避免油剂的影响。组织前期处理和取材须规范,尽量避免坏死较多的组织,切出尽量薄的切片不超过4 ?m。
2. 抗原表达评价
免疫显色强度和阳性细胞密度是定性定量指标,实际工作中常采用强度和密度结合的方法综合计量,我们常用的免疫组化评分方法如下:
细胞染色强度评分:0(无染色),1(弱染色),2(中染色),3(强染色)
肿瘤细胞阳性率评分:0(0~9%),1(10%~25%),2(26%~50%),3(51%~75%),4(76%~100%)
将染色强度评分和阳性细胞率评分的乘积作为该切片评分值。
第二篇:免疫组化非特异性染色的主要原因和消除方法
免疫组化非特异性染色的主要原因和消除方法
一、非特异性染色的主要因素
组织的非特异性染色的机理很复杂,其产生的原因主要可分为以下几点:
(1)一部分荧光素未与蛋白质结合,形成了聚合物和衍化物,而不能被透析除去。
(2)抗体以外的血清蛋白与荧光素结合形成荧光素脲蛋白,可与组织成分结合。
(3)除去检查的抗原以外,组织中还可能存在类属抗原(如Forssman氏抗原),可与组织中特异性抗原以外之之相应抗体结合。
(4)从组织中难于提纯抗原性物质,所以制备的免疫血清中往往混杂一些抗其他组织成分的抗体,以致容易混淆。
(5)抗体分子上标记的荧光素分子太多,这种过量标记的抗体分子带过多的阴离子,可吸附于正常组织上而呈现非特异性染色。
(6)荧光素不纯,标本固定不当等。
二、消除非特异性染色的方法
消除荧光抗体非特异性染色的方法应根据产生的原因采取适当的方法,常用的方法有以下几种:
(一)动物脏器粉末吸收法
常用肝粉(猪、大白鼠或小白鼠),其次是骨髓粉、鼠脑粉和鸡胚粉等。每毫升荧光抗体中加入肝粉50~100mg,在离心管中充分混匀,在室温中振动2h,4℃中过夜,再搅拌10min,高速离心(3000~15000r/min)30min,1~2次后,即可使用其上清液。吸收一般应在临用前进行,吸收后之荧光抗体保存冰箱中勿超过2周。染色应作吸收前后之比较,吸收时可先用缓冲盐水将组织干粉浸湿,离心(3000~15000r/min)30min,除去上清液,再加入荧光抗体进行吸收,以免消耗过多的抗体。
肝粉或新鲜细胞吸收是一种非特异性的消除方法,对荧光抗体的荧光色素和蛋白都有吸附作用。如检查组织中的病毒抗原时,也可用相同的组织干粉或匀浆沉淀物吸收之。
用脏器肝粉吸收对荧光抗体损失较多,如果根据Hiramotos氏等的方法将组织的20%生理盐水匀浆液,用生理盐水洗2~3次,12000r/min
10min离心沉淀,用其沉淀物吸收其荧光抗体即能完全达到目的,京极方久氏认为这样吸收对荧光抗体几乎没有损失,他们常用此法,效果甚佳,吸收后放置一周左右,用时有必要再吸收一次。
【肝粉的制法】
(1)将若干只小白鼠或大白鼠放血杀死,取出肝脏,用生理盐水洗2~3次,除去血液,剥掉表面的结缔组织的脂肪。
(2)剪碎,用生理盐水反复洗涤至无血色止,然后再加生理盐水少许,用组织捣碎机或匀浆器作成匀浆。
(3)将肝匀浆装入离心管内(1/3左右),交换地用2~3倍量生理盐水和丙酮反复洗涤各三次,至上清无血色止,每次完毕先用2000r/min离心沉淀15 min后,再除去上清液。
(4)最后用丙酮洗涤肝浆,再用布氏漏斗过滤,或离心沉淀,将沉淀物平铺在洁净的玻璃板上,37℃烤干(过夜)。
(5)在乳钵中充分研磨,用120目铜筛筛选过后,分装,密封,低温干燥保存。 (二)透析法
荧光素如FITC分子可以通过半透膜,而蛋白质大分子不能透过,可将未与蛋白结合的荧光素透析除去。
(1)将标记完毕的荧光蛋白液装入一透析袋或玻璃纸袋内,液面稍留空隙,紧扎。
(2)浸入0.02mol/pH
7.1~7.4的PBS中(悬于大于标记物体积约50~100倍的PBS内),在4℃中透析,每日更换3~4次PBS,约5~7天,透析液中无荧即可(在荧光光源照射下)。
(三)葡聚糖凝胶G-50柱层析法
除游离荧光素可用2×46cm柱层析法,详细方法参阅第二章。加入荧光抗体15~18ml(按床体积的5%~10%加样),使其缓慢渗入柱内,待即将全部入柱时,加入PBS少许,关闭下口,停留30~40min ,使游离荧光充分进入细筛孔中,然后再接通洗脱瓶开始滴入洗脱液。加入洗脱液一定量后,荧光抗体即向下移行,逐渐与存留于上端的游离荧光素之间拉开明显的界线,随着大量洗脱液的不断加入,二者分离距离越来越大,荧光抗体最先流出,分前、中、后三部分收集,测F/P比值,合格者合并,浓缩,分装。洗脱液用20%磺基水杨酸测定蛋白(发生沉淀反应),继续洗脱,游离荧光素则相继被洗脱下来,至洗脱液中无蛋白和荧光素后,此层析柱即可再用。
若用以除去荧光抗体中的游离荧光素和硫酸铵等盐类,可先在过柱前透析一夜,否则,NH 4+太浓,在蛋白未完全洗脱时即出现NH4+,因而影响提纯与回收蛋白,一般待洗脱液出现蛋白时,即进行收集,之后出现SO4++(用1%BaCl2检查发生白色沉淀)。最后是NH 4+,(用纳氏试剂检查呈黄棕色沉淀),待洗脱液无SO4++及NH 4+后可再用。
如仅用小量荧光抗体,可用1×20cm的柱层析柱,取2g Sephadex G-50装柱,即可过滤2~
3.5ml荧光抗体。
(四)DEAE纤维素柱层析法
标记过多或过少荧光素的抗体分子可用DEAE-纤维素柱层析法除去。方法如下: DEAE-
纤维素柱的装柱,洗脱、再生方法等与提纯IgG方法相同。装柱所需DEAE-纤维素量以干重每克交换20~50mg标记蛋白量为宜
。常用梯度洗脱法如下:
(1)层析柱用0.01mol/L、pH7.2PB平衡,标记物上柱后,先用0.01mol/L、pH7.2PB洗脱,洗出无色或淡绿色液体,洗脱液量(根据床体积大小每梯度乘3),然后依下列各种离子强度洗脱液,
分别洗脱和收集:
0.01mol/L、pH7.2PBS(0.05mol/L NaCl)……洗脱部分1。
0.01mol/L、pH7.2PBS(0.01mol/L NaCl)……洗脱部分2。
0.01mol/L、pH7.2PBS(0.02mol/L NaCl)……洗脱部分3。
将此三部分收集液(每管5ml)分别测定其F/P比值,0.05mol/L NaCl pH7.2PB洗脱液280nm光密度高峰管合并,浓缩保存备用。因这部分非特异性染色荧光最少,是比较好的荧光抗体。其他两部分可以废弃。
来源:生物帮
/list-130.html RNAi技术文档,RNAi技术文档下载
/list-133.html RNA提取技术文档,RNA提取技术文档下载 lb
