430139���﹤�̣�Biotechnology Engineering��
ȫ���ƹ���˶ʿרҵѧλ
�����������
������λ�� ������ѧѧԺ(204)
ҩѧԺ(306)
һ������Ŀ��
�����������﹤�������ʵ�Ļ������ۺͿ����רҵ֪ʶ�����н�ǿ�Ľ��ʵ��������������ܹ������е�רҵ����������������������õ�ְҵ�����ĸ߲��Ӧ����ר���˲ţ�����Ҫ��Ϊ��
1.ӵ�����Ļ���·�ߺͷ������ߣ��Ȱ����������ط����������õ�ְҵ���º;�ҵ�����п�ѧ�Ͻ���������ʵ��ѧϰ̬�Ⱥ������磬���Ľ�����
2.���ձ�����Ļ������ۡ��Ƚ������������ֶΣ��������ijһ������ж������¹�����ơ�����ʵʩ�������о������̿��������̹�����������
3.����һ������
����������
��Ҫ���ǣ�ֲ�����\�����������\�������\��ҽҩ����̬�����������̡����̡������ʹ��̡�ϸ�����̡��������̵ȡ�
��������������ѧϰ����
���й���������д�ѧ����ѧ�� ( ��ͬ��ѧ�� ) ��Ա��
����ȫ����ѧϰ��ʽ��ѧϰ����һ��Ϊ2�ꡣ
�ġ�������ʽ
���ÿγ�ѧϰ��ʵ����ѧ��ѧλ�������ϵ�������ʽ��
�γ��������ֺ�������ۡ���ʵ��Ӧ�á���ǰ��֪ʶ������ͻ��רҵʵ����γ̺���ʵ����γ̡�ʵ����ѧ��ȫ���ƹ���˶ʿ�о��������е���Ҫ���ڣ���������˶ʿ�о�������ҵʵϰ���ɲ��ü���ʵ����ֶ�ʵ�����ϵķ�ʽ������˶ʿ�о�����ѧ�ڼ䣬���뱣֤�����ڰ����ʵ����ѧ��Ӧ�챾�Ʊ�ҵ����ʵ����ѧʱ��ԭ���ϲ�����1�ꡣ
�塢�γ�����
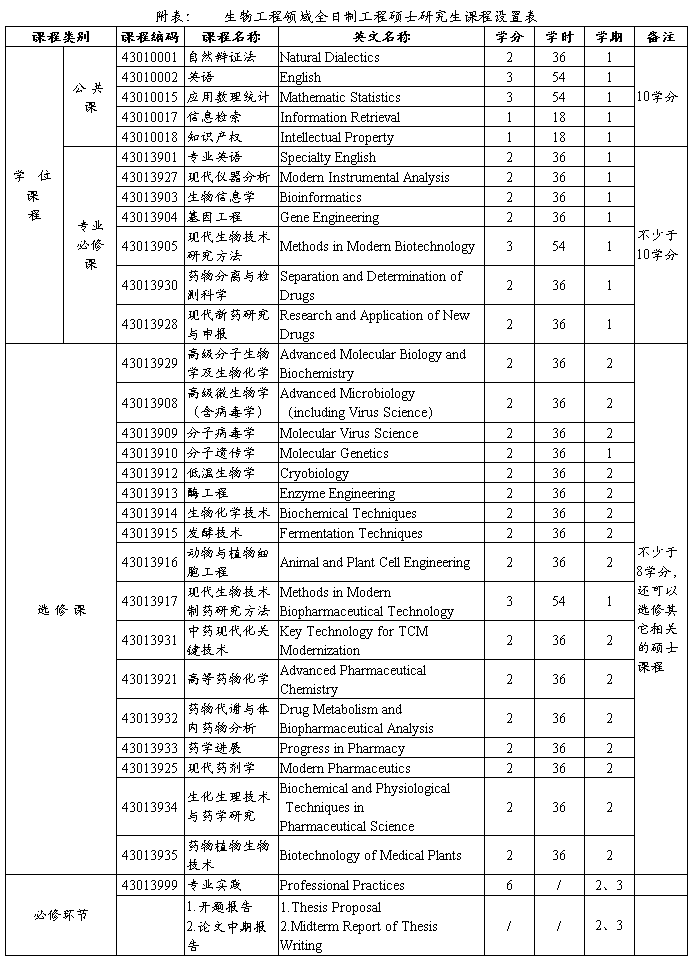
����������˶ʿѧλ���о�����Ӧ�����ѧ�ֲ�����34ѧ�֣�
��һ��ѧλ�γ̲�����20ѧ�֣�����������10ѧ�֡�רҵ����10ѧ�֣�
������ѡ�γ̲�����8ѧ�֣�
������רҵʵ��6ѧ�֡�
���⣬����ɿ��ⱨ�桢�������ڱ������������ڡ�����γ����ü�ѧ��Ҫ���������
����ʵ������
��ѧ�ڼ���뱣֤�����ڰ����רҵʵ�����ɲ��ü���ʵ����ֶ�ʵ�����ϵķ�ʽ������ѧԺ�ѽ����������������ؽ���ʵ����Ҳ���Խ�Ϲ�����Ŀ���û���λʵ�������ݹ�����Ŀ��Ҫ����Ҫ�ڱ�Уʵ�����о��������ɵ�ʦ����������룬ѧԺ������������о���Ժ��鱸����
�о������ڵ�1ѧ����ĩȷ�����ĵ�ʦ���ڵ�ʦָ�����ƶ����ύʵ���ƻ���רҵʵ��һ��Ӧ�����ڵ�2��3ѧ���ڼ䣬����Ԥ�ȼƻ��ķ�������ɣ�ÿ��רҵʵ��������ɺ��о����������Ҽ���������ָ���û��ڵ�ָ���ˣ�������У���ʦ��Ҳ������ʵ�����ŵ�ר�ң�����������רҵʵ����ɺ��о�����дʵ���ܽᱨ�档�о���һ��Ӧ���רҵʵ��ȷ��ѧλ���ĵ�ѡ�⡣ʵ�����֡��ܽᱨ�澭��ʦ��ɵ�����С������ͨ�����о����ɻ����Ӧ��ѧ�֣������������ѧλ���Ĵ�硣
���人��ѧרҵѧλ�о���ʵ���ֲᡷ���о���Ժר���ƶ�����Ҫ���ϣ�רҵѧλ�о���ÿ��һ�ᣬ����ʵʱ����ϸ������רҵʵ�������ڵ�ʵʩ��������������������ɺ���ͬʵ���ܽᱨ��һ������о�����ѧλ������
�ߡ�ѧλ����
����ѡ��Ӧ��Դ�ڹ���ʵ�ʻ������ȷ�Ĺ��̼����������������¼������¹��ա����豸���²��ϡ��²�Ʒ�������뿪�������ĵ����ݿ����ǣ�����������о��������о��������췽���о�������������Ӧ���������������̹����ȡ�
���Ĺ������ڵ�ʦָ���¶�����ɡ�ʵ��˫��ʦ�ƣ�����һλ��ʦ����У�ڣ���һλ��ʦΪ������ҵ�뱾������ص�ר�ҡ�
����д��ɺ������ʦд����ϸ����������⣬��Ӧ��2λ����������һλ����У�⣩���������������ר�����ġ���������Ӧ�ص���ˣ����������ۺ����ÿ�ѧ���ۡ������ͼ����ֶν�����̼�����������������Ĺ����ļ����ѶȺ��������������̼����������˼�롢�·������½�չ�����¹��ա��¼���������Ƶ��Ƚ��Ժ�ʵ���ԣ��䴴��ľ���Ч������Ч��ȷ��档
����ȫ���ƹ���˶ʿ�о���������������й涨�����л��ڣ���ù涨��ѧ�֣��ɼ��ϸ����������Ĵ�硣���ίԱ��Ӧ��5λ����������һλ����У�⣩�뱾������ص�ר����ɡ�
ͨ�����Ĵ���ߣ���Уѧλ����ίԱ�����ͨ���������蹤��˶ʿרҵѧλ��ͬʱ���˶ʿ�о�����ҵ֤�顣
�ڶ�ƪ���й����﹤����־ China Biotechnology Vol25 No9 20xx
�й����﹤����־China Biotechnology, 2005, 25(9):84~88
����ɽҩ��������������صĴ�������������*
�Ŵ���ƹ����־������������������**
������ʦ����ѧ������ѧѧԺ����130024��
ժҪ������立ּ����������ӽ�����HPLC�����ȷ������ӳ���ɽҩ���������ľ�˿���з��봿����һ�������أ�Ganoderma applanatum lectin�����GAL����SDS��PAGE�����Ϊ��һ��������������SDS-PAGE������ǻ�������Ϊ15kDa���ң�HPLC����������Ϊ58kDa���ң�����GAL��4���ǻ���ɡ���������ɷ���������GAL�иʰ��Ậ���ϸߣ������������ɫ���ᣬ�����Ǻ���Լ11.2%��Բ��ɫCD����ʾ�京��3.6%�Ħ�������46.8%�Ħ�ת�Ǻ�49.6%��������������Ц��۵���GAL�����������Ե�2�ֶ���Ѫ��3��Ѫ����Ѫ��Ѫ��ϸ�������Բ�ͬ��Դ��Ѫ��ϸ�������ζȲ�ͬ��������ʵ�������ֻ�������Ǻ�D-�����Dz�������GAL����Ѫ���ԡ�GAL���нϺõ����ȶ���������Ѫ���Բ���Ca2+��Mg2+��Zn2+�ȶ��������ӵ�Ӱ�졣
�ؼ���������������������Ѫ��������
�ո����ڣ�2005��06��27�����ڣ�2005��08��05
*������ѧ������������(2003),����ʡ�Ƽ����ش��б�������Ŀ(20040401��3)
** ͨѶ���ߣ��������䣺liulx062@�����أ�Lectin����һ��㷺�����ڶ�ֲ��������з�������Դ�ĵ����ʻ��ǵ��ף���������רһ�Եؽ�ϣ���������Ѫϸ�������ã�1�ݡ�Ŀǰȫ�����Լ��50����ҩ����������ر��������������Ϊ12~190kDa��������Ϊ0%~18����2�ݣ���Щ�������ܹ�����ͽ鵼ϸ���и�����������ĵ��ڣ��������������Ŀ������������������ǵĹ㷺��ע���о���������֥��Ganoderma Capense�������빽��Flammulina velutipes������������Agrocybe aegerita���Ϳ�Ģ��Tricholoma mongolicum��������з���������ض����к�ǿ�Ŀ��������ԣ�3~6�ݡ��ɴ˿ɼ�����������ҩ�������һ����Ҫҩ���ɷ֡�
����ɽ�����зḻ��ʳ�ú�ҩ�������Դ�����ز��������Ǿ��нϸ�ҩ�ü�ֵ�Ĵ�����������ı����˴ӳ���ɽ��Դ�������˿���з������Ȼ�������سɷ֣����������������ʡ�Ѫ�������Ժ��ص㣬Ϊҩ���������������������ʵ��о��������ṩ���ݡ�
1�����뷽��
1.1����
������ֹ��Լ���ũҵ��ѧ��������С����ͼ��ù��Լ���ʡ������Ʒ��ʵ�鶯�����ģ�������Ѫ�ɼ��ִ�ѧ����ҽѧ�о����ṩ���ռ���Ѫ���2%�ĺ�ϸ����Һ��
DEAE Sephadex A��25ΪPharmacia��Ʒ����ϩ�������ײ��ϩ������Tris��ʮ����������ƣ�SDS���Ȼ�ѧ�Լ������Ϻ��������\������˾���ͷ�����������Ϊ��̩�˲�Ʒ��������ʵ�������õ��Ǿ�ΪSigma��Ʒ��ʵ�������������Լ���Ϊ������������
1.2����
1.2.1�����صķ��봿����ȡҺ�������������˿��60g�����أ�������10mmol/L Tris��HCl (pH8.0)�ñ������24h�������ٵ�����Ƚ����IJ�ɴ�����ˣ���Һ��3500r/min����������20min���ռ�����Һ�������м����������林�40�����Ͷȣ����½���20min��4��
�����ҹ��4 000r/min����������30min��������������������Һ�м����������林�90�����Ͷȣ����衢���á�����ͬǰ������ȡ�ij��������κ�����������أ�GAL����Ʒ��ȡDEAE Sephadex A��25��������װ����2.6cm��40cm����NaClҺƽ�⣬ȡ����GAL����Һ��Ũ��Ϊ3mg/ml������������30ml/h��5ml/tube��0.1~1.6mol/L NaClϴ��Һ4�������������������ݶ�ϴ�ѣ��ռ�ϴ�ѷ������ɺ��ã���������Ѫ���Լ�⡣
1.2.2��������HPLC�ϵĴ����ͼ�⽫���ɺ���Ʒ��10mmol/L Tris-HCl (pH8.0)�ܽ⣬��HPLC����������Ϊ��������Japan SHIMADZU LC-10AVPϵͳ���������SHIMADZU SPD��10AVP������վ��CLASS-Vp��ɫ������TSK-GEL��G3000PWXL��SIL-10ADVP�Զ�������������������0.9%NaCl��pH8.0��������0.5ml/min������Ϊ4�棬ѹ��Ϊ1.6 mpa, ȡ������Ʒ��Ũ��Ϊ2mg/ml��1 ml��045��m��ͷ�������˹����趨20��l������,��¼ɫ��ͼ�����ռ��ĵ���ͼ�¼����ս�����Ѫ���Լ�⣬�ϸ��ռ���1���Է壬�����Σ��䶳������GAL��Ʒ�� 2005, 25(9)�Ŵ���ȣ�����ɽҩ��������������صĴ�������������
�й����﹤����־ China Biotechnology Vol.25 No.9 2005
1.2.3�������ⶨ��1��SDS��PAGE�ⶨ�ǻ���������7�ݣ����뽺Ũ��Ϊ15%��Ũ����Ũ��Ϊ5%������˹����R��250Ⱦɫ�����ñ�����Ϊ�����ữøB��MW=97 400����ţѪ����ף�MW=66 200�����ü������ף�MW=43 000����ţ̼����ø��MW=31 000�����ȵ���ø���Ƽ���MW=20100���ͼ������ܾ�ø��MW=14 400������2��HPLC���ⶨ����������������Ʒ������ͬ��,ȡ������Ũ��Ϊ2mg/ml��������Ʒ��Ũ��Ϊ2mg/ml����1 ml���趨20��l����������¼ɫ��ͼ�����ݲ���SHIMADZU��GPCר������������ͨ��������������������
1.2.4��������ɷ������ִ�ѧ�����������IJ��ԡ�������GAL��6mol/L HCl��110��ˮ��18h��Agilent1100�Ͱ������Զ������Ƿ�����������֡�
1.2.5�������ⶨ����-���ᷨ��8�ݲⶨ��
1.2.6Բ��ɫCD���J��810��Բ��ɫ���Ǽ��ͼ�¼��������Ũ����Folin���ӷ���9�ݲⶨ��Բ��ɫ����ƽ���л���Բֵ�ۦȣݱ�ʾ����λ��deg��cm2/d��mol��ͨ�����������GAL�����ṹ����ĵ�Ԫ������
1.2.7Ѫ���������10���ڡ�V����Ѫ�����м���25��l��������ˮ��ȡGAL��Ũ��Ϊ1mg/ml��25��l������ϡ�ͣ�ÿ����2����Ѫ����Һ��ҡ��Ѫ����ʹ��Һ���ȣ�Ѫ���������·���
1.5~2h�������¼��۲�����Ѫ���ζ���2n��nΪʹѪ����������ĩ��������ʾ��
1.2.8���������鷽��ͬѪ�����顣GAL������ϡ�ͣ�������80mmol/L������Һ��ҡ��Ѫ����ʹ��Һ���ȣ����·���1.5~2h�������¼��۲�����
1.2.9�¶��ȶ���ȡ1mg/ml GAL���ݣ��ֱ���30��40��50��55��60��70��ˮԡ�д���10min��Ѹ����ȴ�����£���������Ѫ��ϸ�����������ԡ�
1.2.10�������Ӷ���Ѫ���Ե�Ӱ�콫GAL��20mmol/L EDTA��Na2��������������Һ�зֱ����10mmol/L ��CaCl2��MgCl2��ZnCl2���ټ�����Ѫ��ϸ������Ѫ���Ե�Ӱ�졣 2��������2.1���������صĴ����ͼ��
���������صĴ���Һ����DEAE Sephadex A��25���ӽ�������0.1mol/L��1.6mol/L NaCl��Һ��pH8.0���ݶ�ϴ�Ѻ�õ�һ��ϴ�ѷ壨ͼ1�����ռ�ϴ�ѷ��پ�HPLC������ͼ2������������Ѫ���Լ�⡣�����������1��������Ѫ���Խ�ǿ��Ϊ���������أ�GAL����Ʒ����2����������Ѫ���ԣ�������������ķ������ܽӽ��������ӽ����������ڷֿ�������HPLC�������������ȸߣ��ɽ����������ʷֿ���ʵ�����ϸ�ȡ����1�壬ȷ����GAL�ĸߴ��ȡ� ͼ1������������DEAE Sephadex A��25���ϵ�
���������ݶ�ϴ��
Fig.1The plot of linear��gradient system for Ganoderma
applanatum lectin on DEAE Sephadex A��25column
2.6cm��40cm��flow rate,30ml/h, 5ml/tube��
NaCl, phosphate buffer
������GAL��Ʒ��SDS��PAGE�������ͼ3��
2.2���������صķ��������ǻ�����������������ɼ�������
���������ؾ�HPLC������ͨ��GPC�����ڼ�����Ϸ���������ԼΪ58kDa���ң�SDS��PAGE������ǻ�������ԼΪ15kDa���ң�����GAL��4���ǻ���ɣ���������ַ����������1��������GAL�иʰ��Ậ���ϸߣ������е������ɫ������ӣ����ᷨ���GAL����11.2���������ǣ�����GAL��һ���ǵ��ס�
ͼ2���������صĸ�ЧҺ��ɫ��ͼ
Fig.2HPLC pattern of Ganoderma applanatum lectin
1��Activity peak�� 2��Inert protein peak
ͼ3���������ص�SDS��PAGE��Ӿ
Fig 3SDS��PAGE of Ganoderma applanatum lectin
M��Standard protein�� 1��Precipitation of 40%~90 %( NH4)2SO4��
2��HPLC��Crude GAL����3��DEAE Sephadex A��25
��1���������صİ�������ɣ�%��
Table1Animo acid composition of Ganoderma
applanatum lectin��%��
��������������������������������������Asp����1.34����Thr����0.62Glu����3.11����Val����0.66Ser����1.35����Phe����0.67Trp����nd����Ala����0.83His����0.67����Leu����1.09Gly����35.5����Pro����0.60Ile����0.56����Met����ndArg����0.72����Lys����1.18nd��not determined
2.3Բ��ɫCD��
�����ͼ4��������GAL�����ṹ�к���3.6%�Ħ�������46.8%�Ħ�ת�Ǽ�49.6%����������������۵���
ͼ4���������ص�CD����ͼ
Fig. 4Circular dichroic spectra of Ganoderma
applanatum lectin
2.4���������ص�����ѧ����
2.4.1���������ص���Ѫ����GAL�Թ��Ե�3��Ѫ�͵���Ѫ���ú�С���Ѫ��ϸ�������������ԣ���������3��Ѫ�͵�Ѫ��ϸ������Ѫ���Խ�ǿ��Ѫ���ζ�Ϊ28~215�����ú�С�����Խ���Ϊ23~28��
2.4.2���������ص�������ʵ��ӽ������2��������ֻ�������Ǻ�D-�����Ƕ�GAL����Ѫ�����в����������ã����ǺͶ������������á�
2.4.3���������ص����ȶ��Խ������3��������GAL��һ�ֶ��Ƚ��ȶ��������أ����¶���55������ʱ������ȫ����Ѫ���ԣ��¶ȳ���60��ʱ��������ʧȥ�ֻ��ԣ����ﵽ70��ʱ��ȫʧ��ɴ˿ɼ���GAL���нϺõ����ȶ��ԡ�
2.4.4���۽������ӵ�Ӱ��GAL����EDTA��������Ѫ����û�б仯�����������Һ�зֱ����10mmol/L CaCl2��MgCl2��ZnCl2����GAL��Ѫ����Ҳû��Ӱ�죬˵��GAL��Ѫ���Բ��ܶ��۽�������Ca2+��Mg2+��Zn2+��Ӱ�졣
3���۽��������������ص��о���չ�Ͽ죬��Ҫ�������������������Ժ�����ѧ���ܷ��棬����ֲ��������桢���̺Ϳ������ȷ������Ž�Ϊ������о��㷺��Ӧ��ǰ�������ı�����������������һ���µ�������2GAL��������ʵ����
Table 2Inhibition of agglutination of Ganoderma applanatum lectin by sugars Sugars����Ganoderma applanatum lectin����g/ml��1000����500����250����125����62.5����31.3����15.6����7.80����3.90����1.95����0.97����0.48����0.24D��Melezitose������������������������������������������������������������������������������Raffinose������������������������������������������������������������������������������Maltose������������������������������������������������������������������������������D��Galactose������������������������������������������������������������������������������L��Sorbose������������������������������������������������������������������������������L��Arabinose����������������������������������������������������������������������������������positive agglutination������negative agglutination
��3�¶ȶ�������������Ѫ���Ե�Ӱ��
Table 3 The effect of temperature on the hemagglutinating activity of Ganoderma applanatum lectin
Temperature���棩����Ganoderma applanatum lectin����g/ml��1000����500����250����125����62.5����31.3����15.6����7.80����3.90����1.95����0.97����0.48����0.2430������������������������������������������������������������������������������40������������������������������������������������������������������������������50������������������������������������������������������������������������������55������������������������������������������������������������������������������60������������������������������������������������������������������������������70����������������������������������������������������������������������������������positive agglutination������negative agglutination
�أ�����֪�ļ���ʳ�þ���ݹ����������ͽ��빽�������صķ���������������ֺͽṹ��һ���IJ��죬����������ͬ���������ԡ�ʵ��֤ʵ��GAL��Ѫ�������Բ��ܱ����ǺͶ��������ƣ������Բ��ֱ����������ƣ��ɴ˿ɼ�GAL���뵥�ǺͶ��ǽ�ϣ����ǽ���������д���һ���о���GAL���Ƚ��ȶ������ѱ����Ĵ����������������֮�������ٿ��ȣ�11���������¶ȶ��������������RNaseT1�����ṹ�ı仯�����ֳ����۵��нϴ��ƻ������������仯��С�������¶ȶ����������ػ���Ӱ���ʵ�����������ƣ������������к���3.6%�Ħ�������46.8%�Ħ�ת�Ǽ�49.6%����������������۵�������¶����߶�����Ա仯��Ӱ����Խ�С���������������������ȣ�GAL��������ߵ��ڵ�����һ��������֮��������Ѫ���Բ��ܱ����ǺͶ��������ƣ�2,12�ݣ������������û��Met�ȡ��ⰵʾ��GAL���ܾ���һ�������ߵ��ڻ��ԣ����յ���ͬ��ϸ�����Ӳ����������ﵽ������������Ϳ������Ĺ�Ч����������о�GAL������ѧ�����Լ����ߵ��ڻ��Լ���������ҩ���������Ľ�һ�������������ṩ�м�ֵ�����ݡ�
�����
��1�� Guillot L, Konska G. Lectins in higher fungi. Biochemical Systematics and Ecology, 1997, 25(3):203~230
��2�� Wang H X, Bunng T, Ooi V E. Lectins from mushrooms. Mycology Research, 1998, 102(8): 897~906
��3�� Patrick H K N, Ng T B. A mushroom (Ganoderma capense) lectin with spectacular thermo��stability, potent mitogenic activity on splenocytes, and antiproliferative activity toward tumor cells. Biochemical and Biophysical Research
Communications,2004, 314: 988~993
��4�� Wang H, Ng T B. Isolation and characterization of velutin, a novel low��molecular��weight ribosome��inactivating protein from winter mushroom (Flammulina velutipes) fruiting bodies. Life Sci, 2001, 68(18):2151~2158
��5�� Zhao C, Sun H, Qi Y. An antitumour lectin from the edible mushroom Agrocybe aegerita. Biochem J, 2003, 374:321~327
��6�� Wang H X, Ng T B, Ooi V E. Lectin activity in fruiting bodies of the edible mushroom Tricholoma mongolicu. Biochem Mol Biol Int,1998, 44(1):135~141
��7�� ��ķ��³�ˣ�������D W. ������,���몲���ӿ�¡ʵ��ָ��. ��3��. ��ѧ�����磬 2002��1713~1722
Sambrook J��Russell D W��Molecular Cloning. A Laboratory Manual. 3ed. Beijing:Science Press�� 2002.1713~1722
��8�� ��Ω��.�Ǹ����������о�����. ��2��. �㽭��ѧ�����磬1999
Zhang W J. Bio��Chemical Research Technique of Complex Carbohydrate. 2ed. Zhejiang University Press��1999
��9�� ������������. �����ʼ����ֲ�. ��������ѧ�����磬2000
Wang J ZH,Fan M. Protein Technical Manual. Beijing:Science Press��2000
��10�� ���, ������Ī�캺,�Ȫ�������.��������ѧ�����磬1986
Sun C, Zhu ZH, Mo H Q, et al. Lectins. Beijing��Science Press��1986
��11�����ٿ�,�˿���. Con A��Բ��ɫ������������Ե��о�. �Ĵ���ѧѧ��(��Ȼ��ѧ��), 1995, 32(6):720~724
Zeng ZH K��Deng J L. Journal of Sichuan University��Natural Science Edition��, 1995, 32(6):720~724
��12��Hsieh K Y, Hsu C I. Oral administration of an edible mushroom��derived protein inhibits the development of food��allergic reactions in mice. Clin Exp Allergy, 2003, 33(11): 1595~1602
Purification and Characterization of a Novel Lectin from the Medicinal
Fungus Ganoderma applanatum in Changbai Mountain
ZHANG Chun��yuHUANG Guo��huiLIN Jing��weiSUN FeiXU Shou��minLIU Li��xia (School of Life Sciences, Northeast Normal UniversityChangchun130024, China)
AbstractA novel lectin��GAL��from the liquid cultured mycelia of medicinal fungus Ganoderma applanatum was purified by precipitation of 40%~90 %( NH4)2SO4, followed by ion chromatography DEAE Sephadex A��25 and HPLC. The purified lectin showed a single band on SDS��PAGE. The relative molecular mass of GAL was about 58kDa tested by HPLC, the subunit of GAL was about 15kDa determined by SDS��PAGE. This implied GAL was composed of four subunits. It contained a high content of glycin, the inexistence of methionine and tryptophan and 11.2% carbohydrates. Circular Dichroic spectra showed it contained 3.6�� ����helix, 46.8% �ª�turn and 49.6% random without �ª�fold. GAL could agglutinated red blood cells, while its hemagglutinating activity for different resources of red blood was different. In a hemagglutination assay, D��Melezitose and Raffinose were the inhibitors of GAL
among the sugars tested. GAL was thermo-stable and metal cations such as Ca2+��Mg2+ and Zn2+had no effects on GAL.
Key wordsGanoderma applanatumLectinCharacteration of biochemistryHemagglutinating activity
