个性化教学辅导教案 天津学大教育信息咨询有限公司

个性化教学辅导教案
学科:化学 任课教师:庞向阳 授课时间: 20xx年 月 日

个性化教学辅导教案 天津学大教育信息咨询有限公司


…… …… 余下全文
个性化教学辅导教案 天津学大教育信息咨询有限公司

个性化教学辅导教案
学科:化学 任课教师:庞向阳 授课时间: 20xx年 月 日

个性化教学辅导教案 天津学大教育信息咨询有限公司


…… …… 余下全文
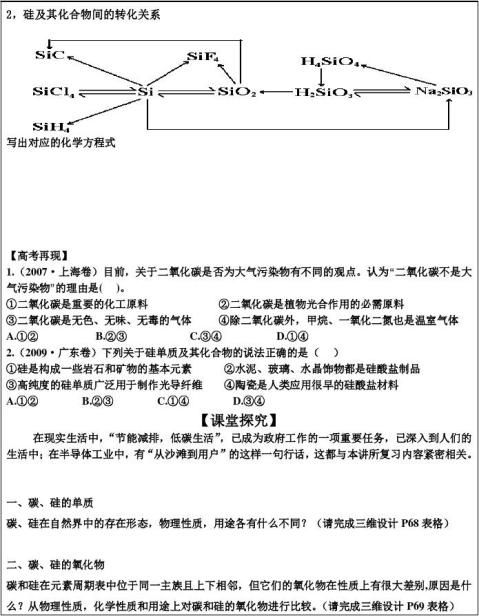
六、有关硅及其重要化合物化学方程式小结
1、Si
(1)与氧气反应
(2)与氯气反应
(3)与氟气反应
(4)与氢氟酸反应
(5)与氢氧化钠溶液反应
2、SiO2
(1)与氧化钙反应
(2)与氢氧化钠溶液反应
(3)与氢氟酸反应
(4)与碳酸钠反应
(5)与碳酸钙反应
(6)与碳单质反应
3、SiCl4
(1)与氢气反应
4、H2SiO3
(1)与氢氧化钠溶液反应
(2)受热分解
5、Na2SiO3
(1)与稀硫酸反应
(2)与二氧化碳和水反应
6、试画出硅及其重要化合物知识网络
…… …… 余下全文
1. 硅的反应
1、
2、
3、
4、
5、
(
6、
2. 二氧化硅的反应
1、
2、
(
3、
4、
5、
6、
3.硅酸钠的反应 1、
(
2、
(
3、
() ) ) ) )
…… …… 余下全文
非金属及其化合物(一)
一、硅Si
1、硅单质
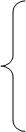 存在结构:化合态(自然界),在地壳中的含量第二(仅次于氧)
存在结构:化合态(自然界),在地壳中的含量第二(仅次于氧)
物理性质:灰黑色,金属光泽,硬度大,有脆性,熔沸点高的固体,
是良好的半导体材料(硅芯片、光电池)
性质
化学性质(常温下化学性质稳定)
下列关于硅的说法不正确的是 ( )
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.加热到一定温度时硅能与H2、O2等非金属反应
答案: C
2、二氧化硅
其化学性质很不活泼,氢氟酸HF是唯一能与之反应的酸!!!
天然二氧化硅的存在形式:结晶形和无定形
应用:石英光导纤维,石英坩埚,玛瑙饰品
1.下列物质的主要成分不是SiO2的是( )
A.石英 B.水晶 C.金刚砂 D.玛瑙
…… …… 余下全文
教师寄语: 鲜花与荆棘同路,泪水伴欢笑齐飞
高三化学一轮复习导学案
1
迎着朝阳自我激励,一天努力; 沐着晚霞自我反馈,一天无悔。
2
迎着朝阳自我激励,一天努力; 沐着晚霞自我反馈,一天无悔。

迎着朝阳自我激励,一天努力; 沐着晚霞自我反馈,一天无悔。
4
迎着朝阳自我激励,一天努力; 沐着晚霞自我反馈,一天无悔。
教师寄语: 鲜花与荆棘同路,泪水伴欢笑齐飞
5
迎着朝阳自我激励,一天努力; 沐着晚霞自我反馈,一天无悔。
…… …… 余下全文
复习专题七 硅 无机非金属材料
【复习目标】
1. 了解硅在自然界的存在形式和性质。
2. 知道二氧化硅的物理性质和化学性质。
3. 知道硅酸盐的性质和用途。
4.了解硅酸盐工业。
【知识归纳】
一.硅的性质
1.硅的物理性质:
2.硅的化学性质:
① 常温下,只能与氟气、氢氟酸(HF)和烧碱反应
② 加热条件下,能和一些非金属单质反应
Si + O2 =
Si + Cl2 =
Si + C =
3.硅的制备:
【典型例题】
例1.在自然界里,硅存在于地壳的各种矿物和岩石中的形式是 (
A.晶体硅 B.二氧化硅 C.硅酸 D.硅酸盐
例2.关于硅的说法不正确的是 (
A.晶体硅是非金属元素,它的单质是灰黑色的有金属光泽的固体
B.晶体硅的导电性介于金属和绝缘体之间,是良好的半导体
C.硅的化学性质不活泼,常温下不与任何物质反应
D.加热到一定温度时,硅能与碳、氧气等非金属反应
二.二氧化硅的性质
1.物理性质
2.化学性质:二氧化硅的化学性质不活泼不与水反应也不与酸﹙HF除外﹚反应① 具有酸性氧化物的性质
SiO2 + H2O ≠
SiO2 + CaO =
SiO2 + NaOH =
[思考] 如何保存强碱溶液?
② 与盐反应
SiO2 + Na2CO3 =
SiO2 + CaCO3 =
③ 弱氧化性
④ 特性:
[思考] 如何保存氢氟酸?制取氢氟酸用什么容器?
90 ) )
【典型例题】
例3.下列说法正确的是
A.二氧化硅溶于水显酸性
B.光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息
C.因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强
…… …… 余下全文
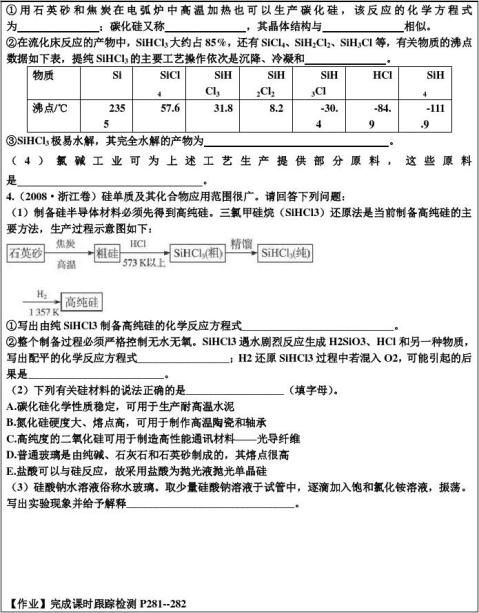
硅及硅的化合物在生活中应用
硅在我们生活中起很大的作用。 硅,一种四价的非金属元素,以化合物的形式,作为仅次于氧的最丰富的元素存在于地壳中,主要以熔点很高的氧化物和硅酸盐的形式存在。它的原子序数为Z=14,核外有14个电子,相对原子质量28.09。在计算中一般为28。电子在原子核外,按能级由低 到高,由里到外,层层环绕,这称为电子的壳层结构。硅原子的核外电子第一层有2个电子,第二层有8个电子,达到稳定态。最外层有4个电子即为价电子,它对硅原子的导电性等方面起着主导作用。由于电子排布的特点,硅具有一些特殊的性质:最外层的4个价电子让硅原子处于亚稳定结构,这些价电子使硅原子相互之间以共价键结合,由于共价键比较结实,硅具有较高的熔点和密度;硅晶体中没有明显的自由电子,能导电,但导电率不及金属,且随温度升高而增加。
在自然界中几乎没有游离态的硅。通常是在电炉中由碳还原二氧化硅而制得的,主要以合金的形式使用(如硅铁合金),也与陶瓷材料一起用于金属陶瓷中,或用作半导体材料(如在晶体管中)和光生电池的元件 [silicon]——元素符号Si相对原子量为28.08653,在元素周期表中的lVA族(第四主族),第三周期。
晶体硅为钢灰色,无定形硅为黑色,密度2.4g/cm3,熔点1414℃,沸点2355℃,晶体硅属于原子晶体,硬而有光泽,有半导体性质。硅的结构与金刚石类似,是正四面体结构。硅的化学性质比较活泼,在高温下能与氧气等多种元素化合,不溶于水、硝酸和盐酸,溶于氢氟酸和碱液,用于造制合金如硅铁、硅钢等,单晶硅是一种重要的半导体材料,用于制造大功率晶体管、整流器、太阳
能电池等。硅在自然界分布极广,主要以二氧化硅和硅酸盐的形式存在。地壳中,硅的含量在所有元素中含量仅次于氧,居第二。其形状分为结晶形和网状形
硅在元素周期表中处于金属元素和非金属元素之间,是很好的半导体,且高纯的单晶硅更是重要的半导体材料,结晶型的硅是暗黑蓝色的,很脆,是典型的半导体。化学性质非常稳定。在常温下,除氟化氢以外,很难与其他物质发生反应。在单晶硅中掺入微量的第IIIA族元素,形成p型硅半导体;掺入微量的第VA族元素,形成n型和p型半导体结合在一起,就可做成太阳能电池,将辐射能转变为电能。在开发能源方面是一种很有前途的材料。另外广泛应用的二极管、三极管、晶闸管和各种集成电路(包括我们计算机内的芯片和CPU)都是用硅做的原材料。
…… …… 余下全文
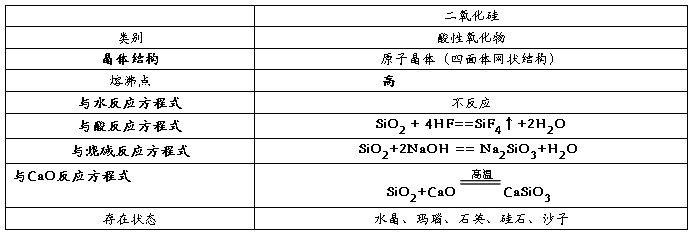
第四章 非金属及其化合物
一、本章知识结构框架
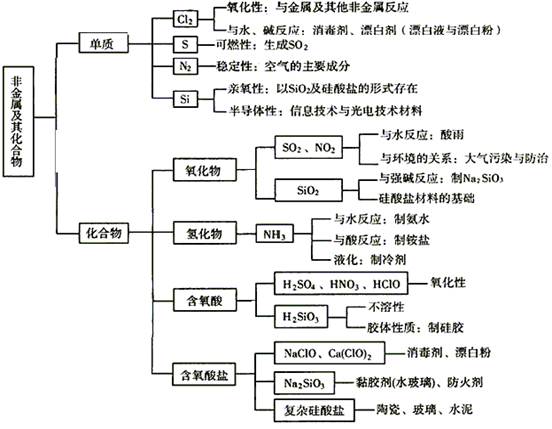
二、本章知识结构梳理
(一) 硅及其化合物
1、二氧化硅和二氧化碳比较
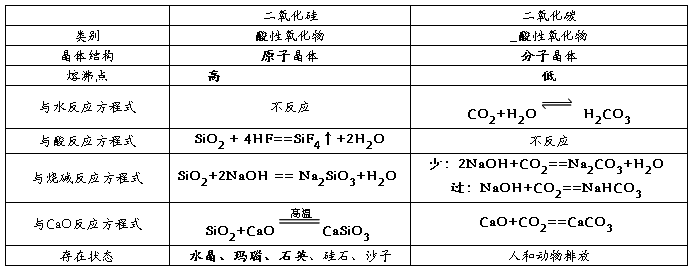
2、硅以及硅的化合物的用途

(二) 氯
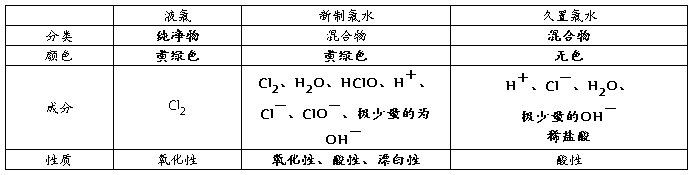
1、液氯、新制的氯水和久置的氯水比较
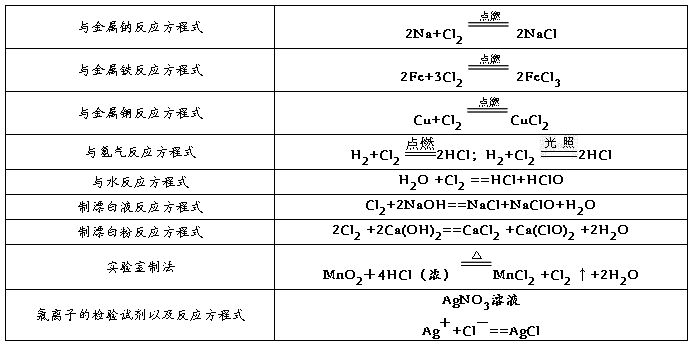
2、氯气的性质
(三) 硫、氮
1、二氧化硫的性质

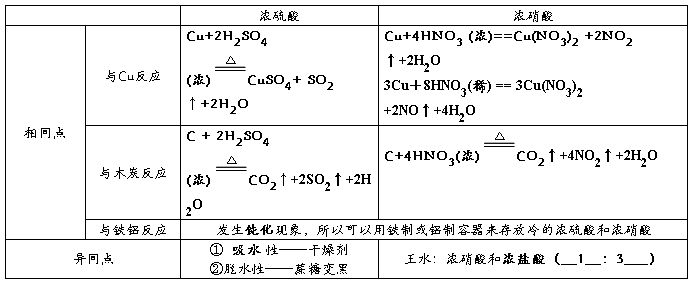
2、浓硫酸和浓硝酸的性质
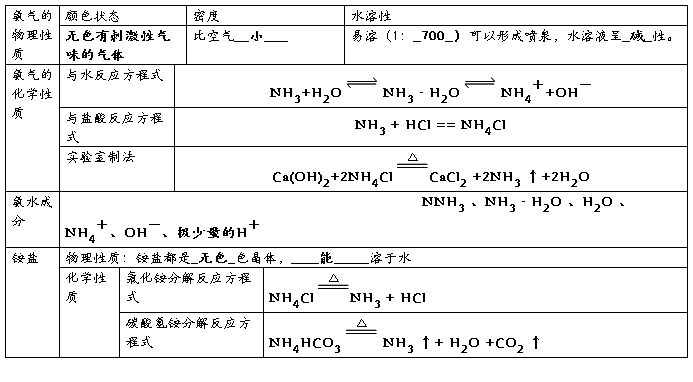
3、氨气、氨水与铵盐的性质
…… …… 余下全文
