铁、钴、镍实验报告
一、实验目的
二、实验内容
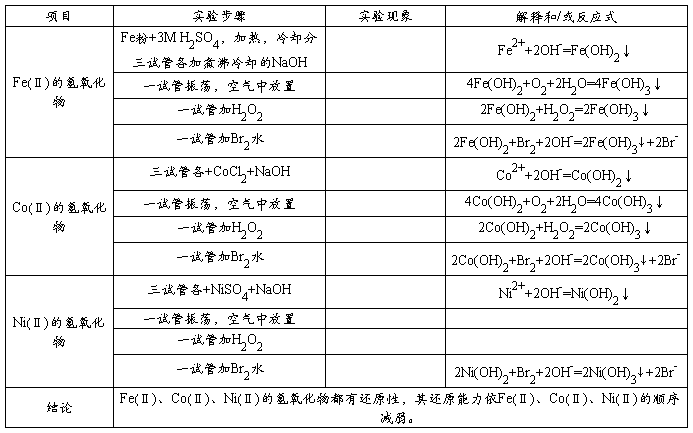
1、Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物的生成和性质
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质

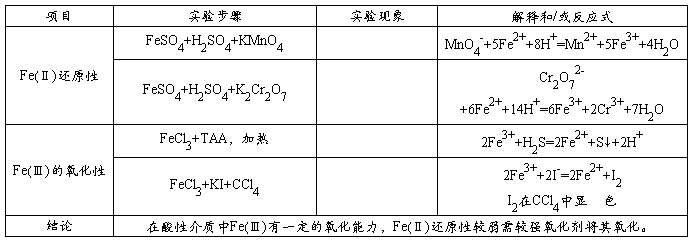
3、铁盐的氧化还原性
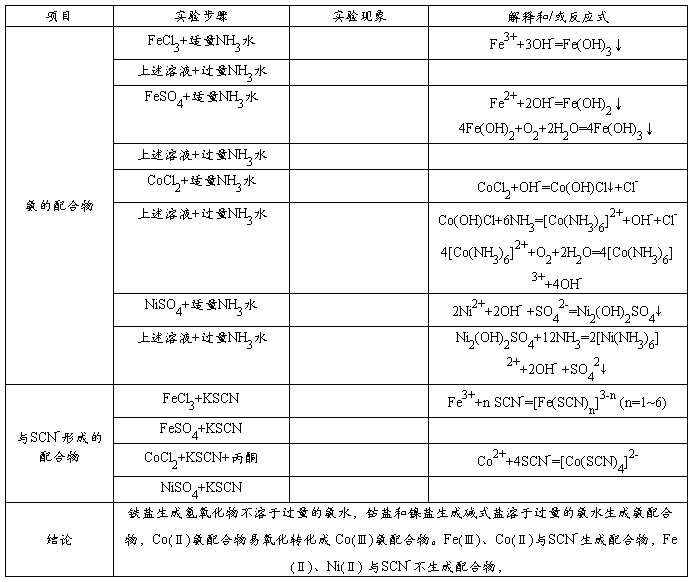
4、Fe、Co、Ni的配合物
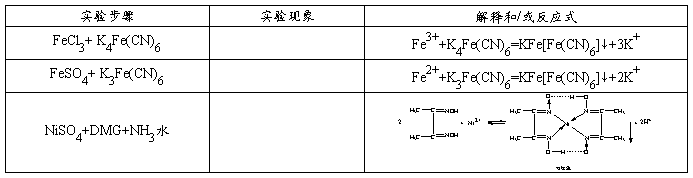
5、离子的鉴定
…… …… 余下全文
铁、钴、镍实验报告
一、实验目的
二、实验内容
1、Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物的生成和性质

2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质

3、铁盐的氧化还原性

4、Fe、Co、Ni的配合物

5、离子的鉴定

…… …… 余下全文





…… …… 余下全文
实验二十五 铁、钴、镍
[实验目的]
1、试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性;
2、试验并掌握铁、钴、镍配合物的生成和Fe2+、Fe3+、Co2+、Ni2+离子的鉴定方法;
3、了解金属铁腐蚀的基本原理及其防止腐蚀的方法。
[实验用品]
仪器:试管、离心试管
固体药品:硫酸亚铁铵、硫氰酸钾
液体药品:H2SO4(1mo1·L-1,6mo1·L-1)、HCl(浓)、NaOH(6mo1·L-1、2mo1·L-1)、
氨水(6 mo1·L-1,浓)、(NH4)2Fe(SO4)2(固体,0.1mo1·L-1)、CoC12(0.1mo1·L-1)、NiSO4(0.1mo1·L-1)、
KI(0.5mo1·L-1)、K4[Fe(CN)6](0.5mo1·L-1)、FeCl3(0.2mo1·L-1)、KSCN(0.5mo1·L-1)、H2O2(3%)、氯水、
碘水、四氯化碳、戌醇、乙醚
材料:碘化钾淀粉试纸
[实验内容]
一、铁(Ⅱ)、钴(Ⅱ)、镍(Ⅱ)的化合物·的还原性
1.铁(Ⅱ)的还原性
(1)酸性介质:往盛有5d氯水的试管中加入2d 6mo1·L-1硫酸溶液,然后滴加硫酸亚铁铵溶液1-2d,观察现象,写出反应式。(如现象不明显,可加1滴KSCN溶液,出现红色,证明有Fe3+生成)
(2)碱性介质:在一试管中放入2mL蒸馏水和3d 6mo1·L-1硫酸溶液,煮沸,以赶尽溶于其中的空气,然后溶入少量硫酸亚铁铵晶体(溶液表面若加3~4d油以隔绝空气,效果更好)。在另一试管中加入1m1 6mo1·L-1氢氧化钠溶液,煮沸(为什么?)。冷却后,用一长d管吸取氢氧化钠溶液,插入硫酸亚铁铵溶液(直至试管底部)内,慢慢放出氢氧化钠(整个操作都要避免空气带进溶液中,为什么?)观察产物颜色和状态。振荡后放置一段时间,观察又有何变化。写出反应方程式。产物留作下面实验用。
…… …… 余下全文
实验六 铁、钴、镍的性质
一、实验目的
1、 试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;
2、 试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验原理
铁、钴、镍常见氧化值:+2和+3 另外 Fe还有+6
1、Fe2+、Co2+、Ni2+的还原性
(1)酸性介质
Cl2 + 2Fe2+(浅绿)=2Fe3+(浅黄)+2Cl-
(2)碱性介质
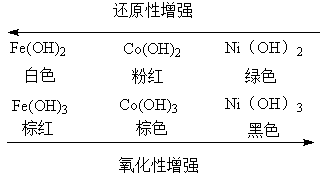
铁(II)、钴(II)、镍(II)的盐溶液中加入碱,均能得到相应的氢氧化物。
Fe(OH)2易被空气中的氧气氧化,往往得不到白色的氢氧化亚铁,而是变成灰绿色,最后成为红棕色的氢氧化铁。Co(OH)2也能被空气中的氧气慢慢氧化。
2、Fe3+、Co3+、Ni3+的氧化性
由于Co3+和Ni3+都具有强氧化性,Co(OH)3,NiO(OH)与浓盐酸反应分别生成Co(II)和Ni(II),并放出氯气。CoO(OH)和NiO(OH)通常由Co(II)和Ni(II)的盐在碱性条件下用强氧化剂(Cl2、Br2)氧化得到。
Fe3+易发生水解反应。Fe3+具有一定的氧化性,能与强还原剂反应生成Fe2+。
3、配合物的生成和Fe2+、Fe3+、Co2+、Ni2+的鉴定方法
(1)氨配合物
Fe2+和Fe3+难以形成稳定的氨配合物。在水溶液中加入氨时形成Fe(OH)2和Fe(OH)3沉淀。将过量的氨水加入Co2+或Ni2+离子的水溶液中,即生成可溶性的氨合配离子[Co(NH3)6]2+或[Ni(NH3)6]2+。不过[Co(NH3)6]2+ 不稳定,易氧化成[Co(NH3)6]3+。
…… …… 余下全文
实验24 铁钴镍
一、实验目的
1、 试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;
2、 试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验内容(实验现象根据自己所观察到的为准)
1、Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物的生成和性质
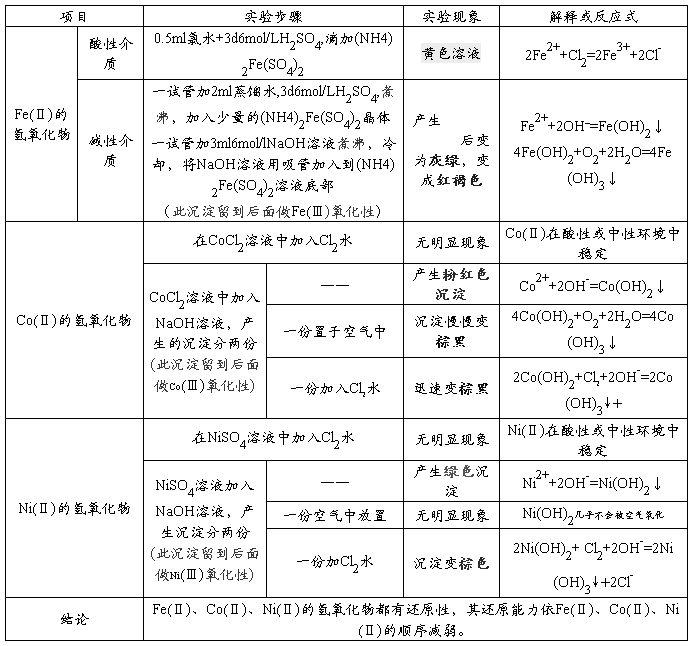
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质
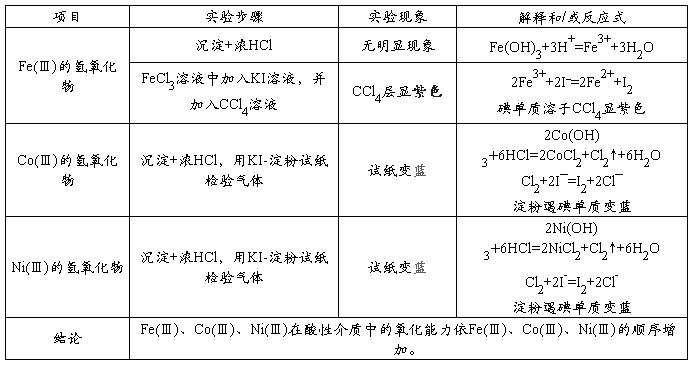
3、Fe、Co、Ni的配合物
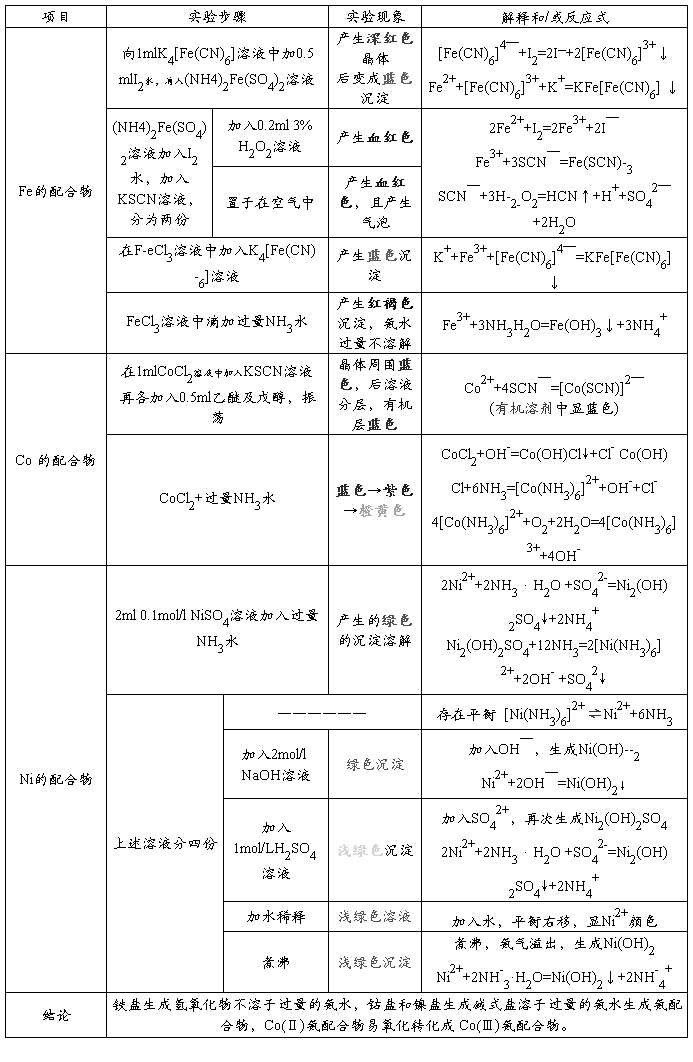
三、实验讨论(从自己实验操作展开)
四、实验思考题和习题
1.实验步骤(2)要求整个实验不能带入空气到溶液中,为什么?
Fe(Ⅱ)易被氧化,如若带入了空气,可能不能观察到颜色的转化过程。
2.根据实验现象总结+2价的铁、钴、镍化合物的还原性和+3价的铁钴镍化合物氧化性的变化规律。
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)在酸性介质中的氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的顺序增加。
3.比较钴镍氨配合物的氧化还原性相对大小及溶液稳定性。
钴盐和镍盐生成碱式盐溶于过量的氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co(Ⅲ)氨配合物。即镍盐更稳定。
4.为什么制取+3价的钴镍氢氧化物要用+2价为原料在碱性条件下进行氧化,而不+3价直接制取?
首先,作为最高价氧化值,Co3+、Ni3+氧化性比较不稳定,易变成其它价态,故不用采用+3价直接氧化得到。其次,而Co(OH)2、Ni(OH)2两性,在碱性条件下易被氧化成+3价氢氧化物。
…… …… 余下全文
实验五:铁、钴、镍
铁、钴、镍属于第八族元素,又称铁系元素。氢氧化铁为红棕色固体,氢氧化亚铁为白色固体,但是氢氧化亚铁很容易被氧气氧化为氢氧化铁。在Fe3+的溶液中滴加NH4SCN会得到Fe3+的血红色配合物,而在Fe2+的溶液中滴加NH4SCN不会有沉淀生成,也不会有颜色;
在Co2+和Ni2+的溶液中滴加强碱,会生成粉红色氢氧化钴(II)和苹果绿色的氢氧化镍(II)沉淀,氢氧化钴(II)会被空气中的氧缓慢氧化为暗棕色的氧化物水合物Co2O3.xH2O。氢氧化镍(II)需要在浓碱溶液中用较强的氧化剂(如次氯酸钠)才能氧化为黑色的NiO(OH)。Co2O3和NiO(OH)会和水或酸根离子迅速发生氧化还原反应;
在水溶液中Fe3+和Fe2+的水配合物的颜色分别为淡紫色和淡绿色的形式存在。在Fe3+和Fe2+的溶液中分别滴加K4[Fe(CN)6]和K3[Fe(CN)6]溶液,都得到蓝色沉淀,它们是组成相同的普鲁士蓝和滕氏蓝,可以用来鉴定Fe3+和Fe2+的存在;
由于Co3+在水溶液中不稳定,所以一般是将Co2+的盐溶在含有配合物的溶液中,用氧化剂将其氧化,从而得到Co3+的配合物;
在含有Co2+的溶液中滴加NH4SCN溶液,会生成蓝色的[Co(NCS)4]2+,由此鉴定Co2+的存在;
在含有Ni2+的溶液中逐滴滴加氨水,会得到蓝色Ni2+的配合物,在此基础上继续滴加丁二酮肟,得到鲜红色鳌合物沉淀,由此鉴定Ni2+的存在。
实验内容:
1:Fe3+的氧化性、Fe2+的还原性及其离子鉴定
(1)离子鉴定:分别用K4[Fe(CN)6]、K3[Fe(CN)6]、NH4SCN和0.25%邻菲罗啉来鉴定Fe3+和Fe2+。(2)氧化还原特性;
2:铁、钴、镍的氢氧化物,Co2+和Ni2+二价氢氧化物的制备与对比;
3:钴、镍的配合物。Co2+和Ni2+的鉴定反应。
…… …… 余下全文
实验17 铬、锰、铁、钴、镍
重点讲内容;:
性质
铬: 《天大》P410—P414 铁;P423—427
锰; P418—421 钴;P423—427
镍;P423—427
一.实验目的;
1、掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2、掌握铬、锰重要氧化钛之间的转化反应及其条件
3、掌握铁、钴、镍配合物的生成和性质
4、掌握锰、铬、铁、钴、镍硫化物的生成和溶解性
5、学习Cr3+ Mn2+ Fe2+ Fe3+ Co2+ Ni2+
二.实验原理;
铬、锰、铁、钴、镍是周期系第?周期第VIB—VIII族`元素,它们都是能形成多种氧化值的化合物。铬的重要氧化值为+3和+6;锰的重要氧化值为+2 +4 +6 +7; 铁、钴、镍的重要氧化值是+2 +3.
Cr(OH)3是两性的氢氧化物。Mn(OH)2和Fe(OH)2都很容易被空气的O2氧化,
…… …… 余下全文
实验八、铬、锰、铁、钴、镍
Chromium, Manganese, Iron, Cobalt,Nickel
实验学时:3 实验类型:验证性
实验所属实验课程名称:大学基础化学实验-1
实验指导书名称:无机化学实验讲义
相关理论课程名称:大学基础化学-1
撰稿人:谢亚勃 日期:2004.11.8
一、目的与任务:
本实验属验证性实验,是过渡元素教学过程中的一部分,对本科生进行这部分的理解和探索能力的培养方面有重要的作用。本实验将一部分课堂教学外的知识,放在实验课堂上进行研究。使学生在获得课堂知识的基础上,进一步探索元素及化合物的其它重要性质和反应,巩固和加深理解课堂上所学基本理论和基本知识;使学生受到观察实验现象,研究实验问题,总结实验结果及基本技能的训
练,培养学生具有观察问题和分析问题的能力、严谨的科学态度、实事求是的作风、勇于创新的精神。
二、内容、要求与安排方式:
1、实验项目内容 通过过渡元素性质的验证,对混合液设计分离鉴定方案,并通过实验对实验元素的性质进行总结。
2、实验要求要求通过实验加深对重要过渡元素和其化合物性质的理解,掌握定性分析的原理和方法,掌握过渡元素和化合物性质的重要递变规律。
3、为了使实验达到教学目标,对学生的要求如下:
(1)实验前要完成预习报告在阅读实验教材和参考资料的基础上,明确实验的目的和要求,弄清实验原理和方法,了解实验中的注意事项。预习报告简明扼要,切忌抄书,字迹清晰,实验方案思路清晰。
(2)实验过程要求认真按照实验内容和操作规程进行实验。如发现实验现象与理论不符,应独立思考,认真分
析查找原因,直到得出正确的结论。认真观察实验现象,记录实验数据。严格遵守实验室规则,爱护仪器设备,注意安全操作。
(3)实验记录要求在细心观察实验现象的基础上,将实验现象和数据记录预习报告上,不允许随手记在纸片或手上。
…… …… 余下全文
