24.多数光化学反应的量子效率都不等于1,因为初级过程中的活化的反应物分子还要进行次级反应。
25.在101325KPa下,纯净的水能以过冷的液态存在,这是因为; 微小晶体的化学位大于大晶体的化学位,新相产生困难。
26.对于化学反应Aa+bB→pP,其反应速度常数KA、KB、KC之间的关系式为:KA/a=KB/b=KC/p。
 27.离子强度 I=1/2(Σbizi2 ) 例题:有一电解质,其中KCl和Ca(NO3)2的浓度为0.01mol.kg-1,则此溶液的离子强度为0.04 mol.kg-1
27.离子强度 I=1/2(Σbizi2 ) 例题:有一电解质,其中KCl和Ca(NO3)2的浓度为0.01mol.kg-1,则此溶液的离子强度为0.04 mol.kg-1
28.原电池放电或者充电时,电极要发生极化现象,极化现象有2种,它们是:浓差极化和电化学极化。
29.1mol液态水在-10摄氏度下凝结为冰,其ΔSm ?0
当物质由固体熔化变为液体,或者由液体蒸发变成气体,总是伴随着吸热,
因此S气>S液>S固
30.相律:f=2+K-∏-R-R’
例题1 由物质A、B、C组成的三元系,当有两个部分互溶的液相与气相达到平衡时,其自由度 f=2+3-3=2
例题2 由物质Ag2O(S)、Ag(S)、O2(g) 组成的相平衡系统,其自由度f=2+3-3=2
例题3 石灰石在一容器中热分解并达到平衡,该平衡系统的自由度是 f=2+3-3-1=1
例题4 苯和乙醇两组分系统具有非常强烈的正偏差,以至于在一定压力下能形成最低恒沸混合物,则在101325Pa下,该恒沸系统的自由度为:f=1+2-2-1=0
例题5 当冰,水蒸气,水共存时,该平衡系统的自由度为0。
31.原电池放电时,阳极的超电势ηa>0
32.组分A、B可以形成四种固态稳定化合物A2B、AB、AB2、AB3,则在该系统完整的液固平衡相图中有几个最低共熔点? 答案:4+1=5。
33.一般来说,由统计力学所得统计熵总要比由热力学第三定律算得的熵要大。因为:气体从298.5K冷却到0K时,热熵没有吐尽,有一部分热熵转变成了不随温度变化的位形熵而残留在晶体中,以致0K时的熵值不等于零。这种位形熵是由于较高温度时具有较多的微观状态的位形,被保留在低温状态所致。
34.表面张力在数值上等于恒温恒压条件下系统增加单位表面时环境对系统所做的可逆体积功。(书上是δWR’=σdAS,界面张力等于增加单位界面面积时系统必须得到的可逆界面功)
35.电解质溶液是靠离子的定向迁移和电极反应导电。
36.热量Q从高温热源传导到低温热源,其作功的能力变小了。
37.若略去CO与N2的振动对熵的贡献差别,则CO与N2的摩尔熵大小关系是:Sm(CO)> Sm(N2)
原因是:Sr,m=Nk[1+lnT/σΘr], σ(CO)=1,σ(N2)=2。 对称的为2,不对称为1。
38.热力学标准状态:
气态组分------pΘ 下处于理想气体状态的气态纯物质
液态和固态组分-----pΘ 下的液态和固态纯物质
溶质------pΘ 下浓度为cΘ 或者bΘ的理想稀溶液
39.对于任意化学反应,其标准平衡常数KΘ 的值,除了决定于反应本性和温度,还决定于pΘ的选取。

 40. 徳拜-休克尔极限公式
40. 徳拜-休克尔极限公式
41. 迁移数
第二篇:河北科技大学物理化学考试题总结8
1.
2. 1 mol理想气体经节流膨胀压力自p1降低到p2,此过程的△A 0,△U 0 。(填>,=或<);
3. 系统经可逆循环后,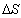 0,经不可逆循环后
0,经不可逆循环后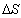 。(填>,=,<)。
。(填>,=,<)。
4. 热力学关系式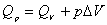 适用于 系统,其中
适用于 系统,其中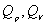 是等压和等容热效应。
是等压和等容热效应。
5. 在α,β相中有A,B两种物质,当达到相平衡时,下列那个关系式是正确的?
(A) 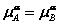 (B)
(B)  (C)
(C) 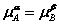 (D) 不能确定
(D) 不能确定
6. 封闭的箱子处于恒温环境中,箱内有二杯液体:A杯为纯水,B杯为蔗糖水溶液。静置足够长时间后,观察其变化,结果发现( )。
(A) A杯水减少,B杯水满后不再变化;(B) B杯水减少,B杯水满后不再变化;
(C) A杯变成空杯,B杯水满后并溢出;(D) B杯水干,并剩有蔗糖晶种,A杯水满后并溢出。
7. A、B可形成完全互溶系统,在一定温度下,若 >
>  ,则当此二组分构成的混合液处于气液平衡时 。(A)
,则当此二组分构成的混合液处于气液平衡时 。(A)  >
>  (B)
(B)  <
< 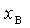 (C)
(C)  =
= 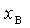 (D) 均可能
(D) 均可能
8. 下述说法中错误的是 。
(A) 通过相图可以确定一定条件下系统由几相构成(B) 相图可表示出平衡时每一相的组成如何
(C) 相图可表示出达到相平衡所需的时间长短(D) 通过杠杆规则可在相图上计算各相的相对数量多少
51. 在电泳实验中,观察到胶粒向阳极移动,表明 ( )。
(a) 胶粒带正电 (b) 胶团的扩散层带负电
(c) 胶团的扩散层带正电 (d) ζ电位相对与溶液本体为正值
52. 0.012 dm3 0.02 mol·dm-3的NaCl溶液和0.1 dm3 0.005 mol·dm-3的AgNO3溶液混合制得的溶胶电泳时,胶粒的移动方向是( )。
(a) 不移动 (b) 向正极 (c) 向负极 (d) 不能确定
53. 在一定量的KCl为稳定剂的AgCl溶胶中加入电解质使其聚沉,其聚沉能力顺序为( )。
(a)AlCl3 < ZnSO4 < KCl (b) KCl < ZnSO4 < AlCl3 (c) ZnSO4 < KCl < AlCl3 (d) KCl < AlCl3 < ZnSO4
54. 将毛细管分别插入25℃和5℃的水中,测得毛细管内液体上升的高度分别为h1和h2,若不考虑毛细管半径的变化,则h1____h2。
55. 液滴愈小其饱和蒸气压愈__ _ 。
56. 空气中肥皂泡的附加压力△p=__ g/ r。
57. 水能完全润湿洁净的玻璃,而Hg不能,现将一根毛细管插入水中,管内液面将_____,当毛细管插入Hg中,管内液面将__ ___。 (填 上升,下降,不变)。
58. 表面张力与物质的本性有关,不同的物质,分子间作用力越大,表面张力也越___,固体物质一般要比液体物质更___的表面张力。
59. 化学反应的平衡状态随 的改变而改变。
a 系统组成 b. 标准态 c 浓度表示方法 d. 化学反应计量式中的计量系数
64. 电泳、电渗、流动电势、沉降电势等电学性质均与 间的相对移动有关,故统称为电动现象。
65. 合成氨反应N2(g)+3 H2(g)= 2 NH3(g)平衡后加入惰性气体且保持系统温度、总压不变(设气体为理想气体),则 。
a.  b.
b. 
c. 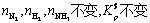 d.
d. 
66. 对于胶体粒子,电势梯度愈大,粒子带电愈多,粒子体积愈小,介质粘度愈小,电泳速度愈 。(填写 大、小)
67. MgO(s) + Cl2(g)=MgCl2+0.5 O2(g) 达平衡后,增加总压(视为理想气体),则 。
a.  b.
b. 
c.  d.
d. 
68. 化学反应等温式 ,当选取不同标准态时,
,当选取不同标准态时,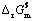 将改变,
将改变,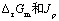 a.都随之改变 b.都不变 c.
a.都随之改变 b.都不变 c.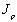 变,
变, 不变 d.
不变 d.
69. 298K时,苯蒸汽在石墨上的吸附服从朗缪尔吸附等温式, 在苯蒸汽压力为40 Pa时,覆盖度θ = 0.05,当θ = 0.5时,苯蒸气的平衡压力为 ( ) Pa 。(a) 400 (b) 760 (c) 1000 (d) 200
70. 已知水溶液表面张力γ与溶质活度a关系为γ = γ0-Aln(1+Ba), γ0为纯水的表面张力, A与B为常数,则溶液表面过剩Γ= ( )。
(a)  (b)
(b) 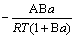 (c)
(c)  (d)
(d) 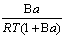
71. 溶液表面层对溶质发生吸附,当cB (表面浓度) > cB,0 (本体浓度),则 ( )。
(a) 称为正吸附,溶液表面张力降低 (b) 称为正吸附,溶液表面张力不变
(c) 称为负吸附,溶液表面张力增加 ( d) 称为负吸附,溶液表面张力降低
72. 某气相反应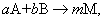 当A与B投料比不同时M在平衡混合物中的浓度不同,其中A与B投料比为
当A与B投料比不同时M在平衡混合物中的浓度不同,其中A与B投料比为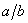 时, 。a. A的转化率最大 b. M在平衡混合物中的浓度最大
时, 。a. A的转化率最大 b. M在平衡混合物中的浓度最大
c. M平衡产量最大 d. A在平衡混合物中浓度最小
73. 丁达尔效应是光的 作用所引起的,其强度与入射光波长(λ)的_ _次方成反比,与粒子的数浓度成正比。
74. 已知25℃时,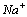 及
及 水溶液的无限稀释摩尔电导率
水溶液的无限稀释摩尔电导率 ,
, 分别是
分别是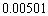 和
和 。则该温度下
。则该温度下 离子的
离子的
 。
。
90. 今有以下两电池
a. 
b.
其中 的电动势与氯离子的浓度 无关。
无关。
91. 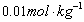 的
的 水溶液的离子平均活度系数
水溶液的离子平均活度系数 ,则其离子平均活度
,则其离子平均活度 ;离子强度I= 。
;离子强度I= 。
92. 用同一电导池分别测定浓度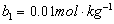 和
和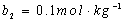 的两个电解质溶液,其电阻分别为
的两个电解质溶液,其电阻分别为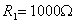 ,
, ,则它们的摩尔电导率之比
,则它们的摩尔电导率之比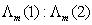 为 。
为 。
93. 下列两电池反应的标准电动势分别为 ,则两个
,则两个 的关系为( )。
的关系为( )。
(1)
(2)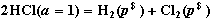
(a)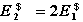 (b)
(b)  (c)
(c) 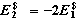 (d)
(d) 
94. 某电池在298K、 的压力下,可逆放电的热效应为
的压力下,可逆放电的热效应为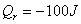 ,则该电池反应的
,则该电池反应的 值( )。
值( )。
(a) <-100J (b) = -100J (c) > 100J (d) = 100J
95. 298K时有如下两个反应
(1)
(2)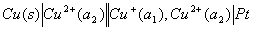
两个电池的电池反应都可写成  。则两个电池的
。则两个电池的 和
和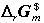 之间的关系为( )。
之间的关系为( )。
(a)  和
和 都相同 (b)
都相同 (b) 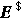 不同,
不同, 都相同
都相同
(c)  和
和 都不同 (d)
都不同 (d) 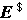 相同,
相同,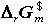 不同
不同
96. 在298K时,浓度为0.1和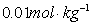 的HCl溶液的液接电势为
的HCl溶液的液接电势为 ,浓度相同而换用KCl溶液,其液接电势为
,浓度相同而换用KCl溶液,其液接电势为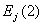 ,两者关系为( )。
,两者关系为( )。
(a) 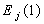 <
<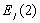 (b)
(b) 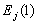 >
>
(c) 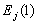 =
= (d)无法判断
(d)无法判断
97. 某反应,当起始浓度增加一倍时,反应的半衰期也增大一倍,此反应为( )级反应。
(A) 0; (B) 1; (C) 2; (D)3;
98. 已知某反应的反应物无论其起始浓度 为多少,反应掉
为多少,反应掉 的60%时所需的时间均相同,所以该反应为( )级反应。(A) 0; (B) 1; (C) 2; (D)3;
的60%时所需的时间均相同,所以该反应为( )级反应。(A) 0; (B) 1; (C) 2; (D)3;
99. 某反应在有限时间内可反应完全,所需时间为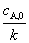 ,该反应级数为( )。
,该反应级数为( )。
(A) 零; (B) 一; (C) 二; (D) 三。
100.关于反应级数,说法正确的是( )。
(A) 只有基元反应的级数是正整数; (B) 反应级数不会小于零;
(C) 催化剂不会改变反应级数;(D) 反应级数都可以通过实验确定。
101.某反应,其半衰期与起始浓度成反比,则反应的反应级数为( )。
(A) 0; (B) 1; (C) 2; (D) 3。
102.有相同初始浓度的反应物在相同的温度下,经一级反应时,半衰期为 ;若经二级反应,其半衰期为
;若经二级反应,其半衰期为 ,那么( )。
,那么( )。
(A) ; (B)
; (B) ;
;
 (C)
(C)
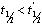 ; (D)两者大小无法确定。
; (D)两者大小无法确定。


103.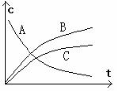 乙酸高温分解时,实验测得CH3COOH(A)、CO(B)、CH=CO(C) 的浓度随时间的变化曲线如下图,由此可以断定该反应是( )。
乙酸高温分解时,实验测得CH3COOH(A)、CO(B)、CH=CO(C) 的浓度随时间的变化曲线如下图,由此可以断定该反应是( )。
(A)基元反应; (B) 对峙反应;
(C) 平行反应; (D) 连串反应。
(119题图)
104.放热对峙反应 的正、逆反应均为基元反应,则( )。
的正、逆反应均为基元反应,则( )。
(A)  ; (B)
; (B) 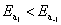 ; (C)
; (C)  ; (D)不能确定。
; (D)不能确定。
105.如果某一反应的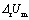 为
为 ,则该反应的活化能
,则该反应的活化能 是( )。
是( )。
(A)  ; (B)
; (B)  ;
;
(C)  ; (D) 无法确定 。
; (D) 无法确定 。
106.催化剂的作用是( )。
(A)只加快正反应速率; (B) 提高反应物平衡转化率;
(C)缩短反应达到平衡时间; (D) 降低反应压力
107. 平行反应
平行反应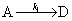 ,若
,若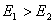
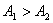 则升高反应温度会( )主产物D的产率。
则升高反应温度会( )主产物D的产率。 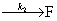
108.在光的作用下,O2可变成O3,当1molO3生成时吸收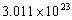 个光量子,此反应的光量子效率为( )。
个光量子,此反应的光量子效率为( )。
反应2A ,若A的初始浓度
,若A的初始浓度 ,经反应后,A消耗掉3/4的时间
,经反应后,A消耗掉3/4的时间
