物理化学论文
一个学期就这样马上就过去了,我们对物理化学这门课也有了系统的学习。对于物理化学这门课,我最大的感觉就是抽象,物化不像无机化学,每一个反应都能通过化学反应实验真实的反映出来,物化更多的是理论上的东西,在刚刚开始学物化的时候,我几乎被一大堆偏微分关系式所吓晕。虽然高中时就学过物理,进入大学时也学习过一个学期的大学物理,但由于成绩一直不理想,所以对于物理化学一学是真直都存在恐惧心理的。尤其是看那一大堆偏微分的公式,更是让我觉得头痛。然而通过阅读以及对以前高数的复习,我慢慢地能理解偏微分的含义了。由于物化是一门交叉性的学科,因此我们除了上课要认真听讲外,更重要的是联系以前学习过的知识,将它们融会贯通,这才能学习好物化。所以对物化的学习,需要靠理解,领悟,不过,认真的记住每一个公式也是很重要的,所以我先总结一下物化的学习心得:
勤于思考:十分重视教科书,把其原理、公式、概念、应用一一认真思考,不粗枝大叶,且眼手并用,不放过细节,如数学运算。对抽象的概念如熵等千方百计领悟其物理意义,甚至不妨采用形象化的理解。适当地与同学老师交流、讨论,在交流中摒弃错误。二、认真听讲:要抓住老师上课讲的重点知识,了解物化学习过程中的难点,思考老师是怎样理解书本中内容的,一定要紧跟老师的思路,不能松懈。 三、勤于总结:物理化学这门课知识点多,内容零散复杂,但是知识前后联系又很紧密,所以一定要善于总结,把前后知识联系在一起。四、善于联系实际:学习并不是一味的学习,还需要关注、联系生活中得事物。学习的目的是什么?以为学习就是把书本上的知识掌握,能够很便利的运用知识解决所有题目,这就是学习的目的,但现在发现,学习的目的是与生活分不开的,所以当熟练掌握书本知识后,不但学会解决联系题目,重要是懂得怎样把这些知识是运用到生活中或与生活联系。
在这门课中,我们主要学习了热力学部分的知识,在热力学中,我们学习了热力学三大定律,以及它们之间的相互关系,还掌握了几个状态函数的求解方法。尔后,我们还学习了溶液中普遍存在的拉乌尔定律和亨利定律。相平衡这张内容中我们见到了形形色色的相图,包括二组分、三组分以及多组分的相图及其应用。在化学平衡中我们掌握了温度、压力以及惰性气体对化学平衡的影响。最后,我们还学习了统计热力学基础,其中最重要的就是原子、分子配分函数以及用这些知识求热力学状态函数的值。
以下就是我对物理化学的公式与使用条件的一些总结,希望能与大家共同分享。
1. 理想气体状态方程
PV = nRT
对理想气体是万能公式,怎么用都没错。
2. 范德华方程

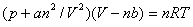
式中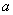 的单位为Pa·m6·mol-2,b的单位为m3·mol-1,
的单位为Pa·m6·mol-2,b的单位为m3·mol-1,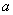 和
和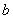 皆为与气体的种类有关的常数,称为范德华常数。
皆为与气体的种类有关的常数,称为范德华常数。
此式适用于最高压力仅为几个MPa的中压以下范围内实际气体p,V,T,n的相互计算。
3. 热力学第一定律的数学表示式
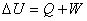
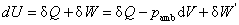
规定系统吸热为正,放热为负。系统得功为正,对环境作功为负。式中pamb为环境的压力,W’为非体积功。上式适用于封闭体系的一切过程。
4. 焓的定义式
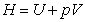
5. 焓变
(1)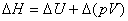
式中 为
为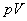 乘积的增量,只有在恒压下
乘积的增量,只有在恒压下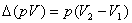 在数值上等于体积功。
在数值上等于体积功。
(2)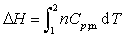
此式适用于理想气体单纯pVT变化的一切过程,或真实气体的恒压变温过程,或纯的液体、固体物质压力变化不大的变温过程。
6. 热力学能(又称内能)变
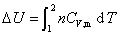
此式适用于理想气体单纯pVT变化的过程。
7. 热容的定义式
(1)定压热容和定容热容
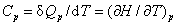
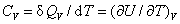
(2)摩尔定压热容和摩尔定容热容
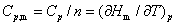
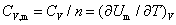
上式分别适用于无相变变化、无化学变化、非体积功为零的恒压和恒容过程。
8. 体积功
(1)定义式
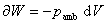
或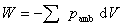
(2)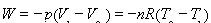 适用于理想气体恒压过程。
适用于理想气体恒压过程。
(3)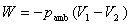 适用于恒外压过程。
适用于恒外压过程。
(4)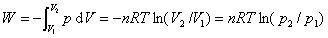 适用于理想气体恒温可逆过程。
适用于理想气体恒温可逆过程。
(5) 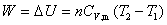 适用于
适用于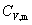 为常数的理想气体绝热过程。
为常数的理想气体绝热过程。
9. 理想气体可逆绝热过程方程

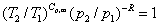

上式中,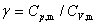 称为热容比(以前称为绝热指数),适用于
称为热容比(以前称为绝热指数),适用于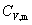 为常数,理想气体可逆绝热过程p,V,T的计算。
为常数,理想气体可逆绝热过程p,V,T的计算。
10. 反应进度
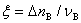
上式是用于反应开始时的反应进度为零的情况, ,
,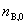 为反应前B的物质的量。
为反应前B的物质的量。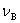 为B的反应计量系数,其量纲为一。
为B的反应计量系数,其量纲为一。 的量纲为mol。
的量纲为mol。
11. 标准摩尔反应焓
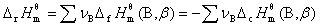
式中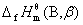 及
及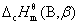 分别为相态为
分别为相态为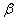 的物质B的标准摩尔生成焓和标准摩尔燃烧焓。上式适用于
的物质B的标准摩尔生成焓和标准摩尔燃烧焓。上式适用于 =1 mol,在标准状态下的反应。
=1 mol,在标准状态下的反应。
12. 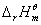 与温度的关系
与温度的关系

式中 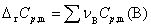 ,适用于恒压反应。
,适用于恒压反应。
13. 节流膨胀系数的定义式

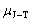 又称为焦耳-汤姆逊系数。
又称为焦耳-汤姆逊系数。
这些就是我对物理化学这门课这一学期学习的心得体会以及总结。
第二篇:大学物理热学思想论文
探讨热学中的物理思想论文
摘要:物理是研究物质结构及其运动规律的学说。物理学飞速发展到今天,是与各个孜孜不倦科学家的经典物理思想和物理实验密不可分的。有思后有行,可见物理学的思想在物理学中起到不可替代的指引作用。热学思想是物理学思想中一个不可缺少的一部分,它是热学实验的理论基础,推动了热学的发展,加速社会的进步。
关键词: 热学 物理思想
1、 量变与质变的关系
量变质变规律在坐标系上反应为连续的曲线,曲线有不相同的质点组成,只有导数相似的质点才相似。质量的变化是一切变化的根源,任何量(除质量外)都来源于质量。
2、能量转化与守恒 能量可以从一个物体传递给另一个物体,而且能量的形式也可以互相转换,但能量永远不会消失,这就是能量守恒热力学第一定律是对能量守恒和转换定律的一种表述方式。
3、墒增原理 熵增原理就是在孤立热力系所发生的不可逆微变化过程中,熵的变化量永远大于系统从热源吸收的热量与热源的热力学温度之比。可用于度量过程存在不可逆性的程度熵增原理表明,在绝热条件下,只可能发生dS>=0 的过程,其中dS = 0 表示可逆过程;dS>0表示不可逆过程,dS<0 过程是不可能发生的。但可逆过程毕竟是一个理想过程。因此,在绝热条件下,一切可能发生的实际过程都使系统的熵增大,直到达到平衡态。
4、结束语
物理学思想的形成是一个长期酝酿的过程,它是物理学发展前进道路的理论基石,所以培养具有实质性意义的、创新性的物理学思想是刻不容缓的。我们当代大学生应该在日常生活中形成多想、多学、多做的学习习惯,成为一个真正意义
上得创新性人才。
参考文献:
[1] 冯端.《普通物理教程 热学》【J】 南京大学出版社,20xx(2).
[2] 朱鋐雄.《物理学思想概论》 【J】 清华大学出版社,20xx(1).
