第二章 变压器
2-1 什么叫变压器的主磁通,什么叫漏磁通?空载和负载时,主磁通的大小取决于哪些因素?
答:变压器工作过程中,与原、副边同时交链的磁通叫主磁通,只与原边或副边绕组交链的磁通叫漏磁通。
由感应电动势公式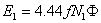 可知,空载或负载情况下
可知,空载或负载情况下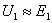 ,主磁通的大小取决于外加电压
,主磁通的大小取决于外加电压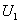 、频率
、频率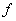 和绕组匝数
和绕组匝数 。
。
2-2 一台50Hz的变压器接到60Hz的电源上运行时,若额定电压不变,问激磁电流、铁耗、漏抗会怎样变化
答:(1)额定电压不变,则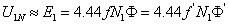
又

 , 即
, 即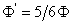 磁通降低,此时可认为磁路为线性的,磁阻
磁通降低,此时可认为磁路为线性的,磁阻 不变,励磁磁势
不变,励磁磁势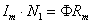 ,
,
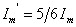 ;
;
(2)铁耗: ,
,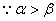 铁耗稍有减小;
铁耗稍有减小;
(3)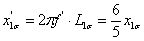 ,
, 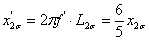
2-4在导出变压器的等效电路时,为什么要进行归算?归算是在什么条件下进行的?
答:因为变压器原、副边只有磁的联系,没有电的联系,两边电压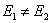 、电流不匹配,必须通过归算,才能得到两边直接连接的等效电路;
、电流不匹配,必须通过归算,才能得到两边直接连接的等效电路;
归算原则:保持归算前后副边的磁动势不变。
2-5 利用T型等效电路进行实际问题计算时,算出的一次和二次侧电压、电流和损耗、功率是否为实际值,为什么?
答:一次侧没有经过归算,所以为实际值;
二次侧电压、电流不是实际值,因为归算前后绕组匝数不同,但损耗、功率为实际值。
2-6 变压器的激磁阻抗和等效漏阻抗如何测定?
答:激磁阻抗由空载试验测量;等效漏阻抗由短路试验测量。
(具体测量方法略)
2-15有一台三相变压器,额定容量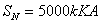 ,额定电压
,额定电压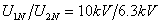 ,Y,d联结,试求:(1)一次、二次侧的额定电流;(2)一次、二次侧的额定相电压和相电流。
,Y,d联结,试求:(1)一次、二次侧的额定电流;(2)一次、二次侧的额定相电压和相电流。
解:(1)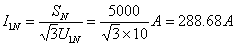

(2)原边Y联结: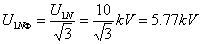
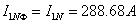
副边 联结:
联结: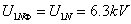
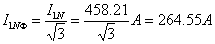
2-17有一台单相变压器,已知参数为: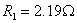 ,
,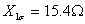 ,
, ,
,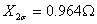 ,
, ,
,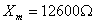 ,
,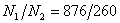 。当二次侧电压
。当二次侧电压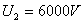 ,电流
,电流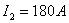 ,且
,且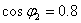 (滞后)时:(1)画出归算到高压侧的T型等效电路;(2)用T型等效电路和简化等效电路求
(滞后)时:(1)画出归算到高压侧的T型等效电路;(2)用T型等效电路和简化等效电路求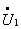 和
和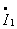 ,并比较其结果。
,并比较其结果。
解:(1)归算到高压侧:
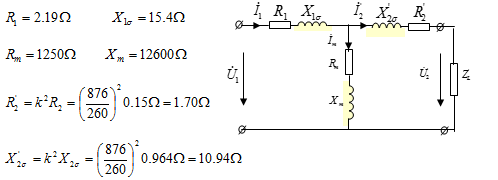
(2)T型等效电路如图示:
设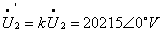
则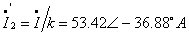

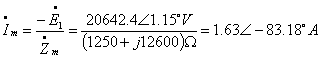
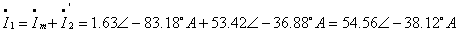
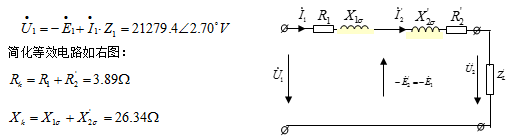
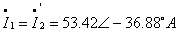
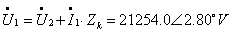
由于在满载的情况下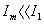 ,励磁支路可以忽落不计,所以两种方法计算的结果相差不大,在误差允许的范围之内。
,励磁支路可以忽落不计,所以两种方法计算的结果相差不大,在误差允许的范围之内。
2-18在图中,各铅垂线上对应的高、低压绕组绕于同一铁心柱上。已知A、B、C为正相序,试判断联结组a和b的组号。
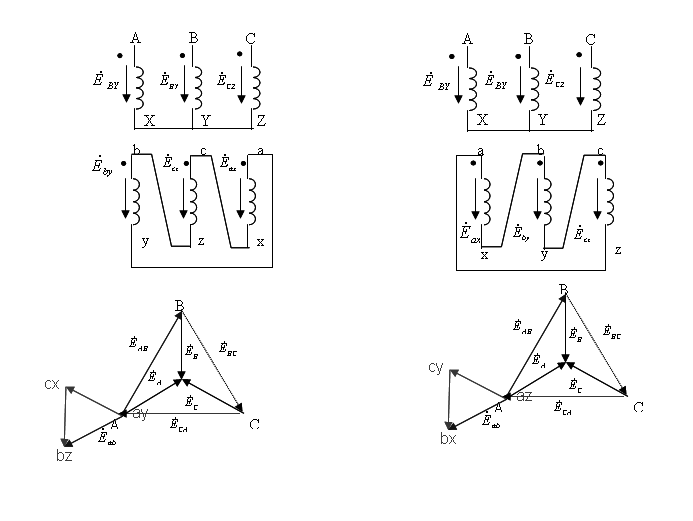
由图可以看出两组均为Y,d7
2-20 有一台1000kVA,10kV/6.3kV的单相变压器,额定电压下的空载损耗为4900W,空载电流为0.05(标幺值),额定电流下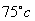 时的短路损耗为14000W,短路电压为5.2%(百分值)。设归算后一次和二次绕组的电阻相等,漏抗亦相等,试计算:(1)归算到一次侧时T型等效电路的参数;(2)用标幺值表示时近似等效电路的参数;(3)负载功率因数为0.8(滞后)时,变压器的额定电压调整率和额定效率;(4)变压器的最大效率,发生最大效率时负载的大小(
时的短路损耗为14000W,短路电压为5.2%(百分值)。设归算后一次和二次绕组的电阻相等,漏抗亦相等,试计算:(1)归算到一次侧时T型等效电路的参数;(2)用标幺值表示时近似等效电路的参数;(3)负载功率因数为0.8(滞后)时,变压器的额定电压调整率和额定效率;(4)变压器的最大效率,发生最大效率时负载的大小(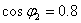 )。
)。
解:(1)归算到一次侧等效电路的参数:
空载试验在低压侧进行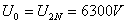 ,
,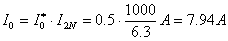
折算到高压侧: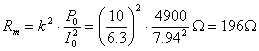
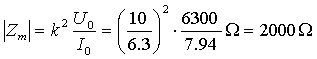
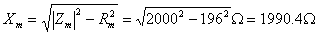
短路试验在高压侧进行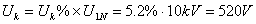
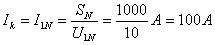
所以: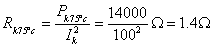
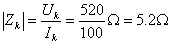

即: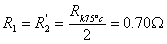 ,
,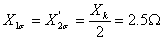
(2)标幺值:
高压侧的电阻基准值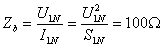

 ,
, 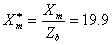
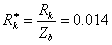 ,
, 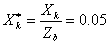
(3)变压器额定电压调整率和额定效率:
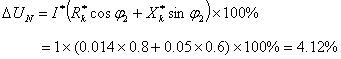
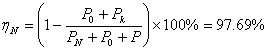
(4)变压器效率最大时,可变损耗等于不变损耗
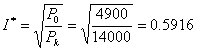
最大效率: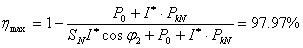
2-21 有一台三相变压器,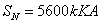 ,
,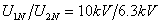 ,Y,d11联结组。变压器的开路及短路试验数据为
,Y,d11联结组。变压器的开路及短路试验数据为

试求一次侧加额定电压时:(1)归算到一次侧时近似等效电路的参数(实际值和标幺值);(2)满载且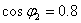 (滞后)时,二次侧电压
(滞后)时,二次侧电压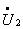 和一次侧电流
和一次侧电流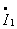 ;(3)满载且
;(3)满载且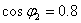 (滞后)时的额定电压调整率和额定效率。
(滞后)时的额定电压调整率和额定效率。
解:(1)归算到一次侧时近似等效电路的参数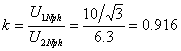
空载试验在低压侧,折算到高压侧:
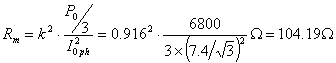

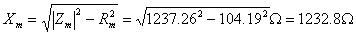
短路试验在高压侧进行
所以: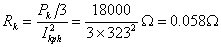
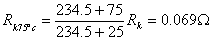
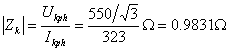
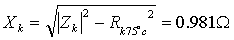
标幺值:高压侧的电阻基准值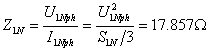

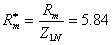 ,
, 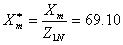
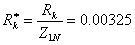 ,
, 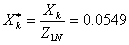
(2)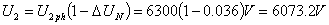
满载时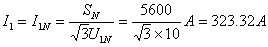
设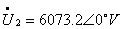 ,则由简化等效电路可知
,则由简化等效电路可知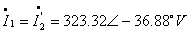
(3) 电压调整率和效率:
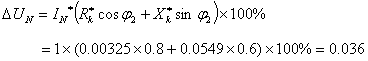
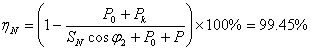
2-24 某变电所有两台组号为Y,yn0的三相变压器并联运行,其数据为
第一台: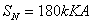 ,
,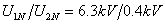 ,
,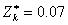 ;
;
第二台: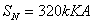 ,
,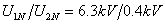 ,
,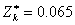 。
。
试计算:(1)当总负载为400kVA时,每台变压器分担多少负载;(2)在每台变压器均不过载的情况下,并联组的最大输出是多少?
解:(1)当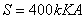 时,
时,
设第一台变压器分配负载为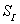 ,则第二台变压器的负载
,则第二台变压器的负载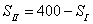 ,满足:
,满足:
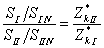 ,带入数值计算可得:
,带入数值计算可得: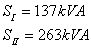
(2) 求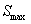 :负载增加时,
:负载增加时, 小的变压器(第二台)先满载,此时
小的变压器(第二台)先满载,此时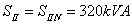
又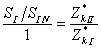

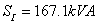
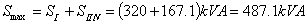
2-26 一台5kVA,480V/120V的普通两绕组变压器,改接成600V/480V的自耦变压器,试求改接后一次和二次的额定电流和变压器的容量。
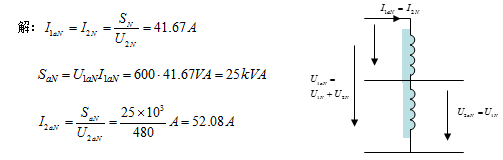
第二篇:化学必修1第二章第二节离子反应知识点归纳及同步练习
第二章第二节离子反应知识点归纳及同步练习
1、 下列叙述中正确的是( )
A、 氯化镁固体之所以不导电的原因是氯化镁固体中不含阴、阳离子;
B、 在电流作用下氯化钠在水溶液中电离成钠离子和氯离子;
C、 氯化钾固体不能导电而其水溶液能导电的原因是氯化钾与水发生反应产生了钾离子和氯离子;
氯化钾固体不能导电的原因是构成氯化钾固体的钾离子和氯离子不能自由移动,而溶于水后在水分子的作用下产生自由移动的钾离子和氯离子,所以其水溶液能导电。
2.下列离子方程式正确的是( )
A、澄清石灰水与稀盐酸反应
Ca(OH)2 + 2H+ =Ca2+ + 2H20
B、碳酸钠溶液与盐酸反应
Na2CO3 + 2H+ =2Na+ + H2O + CO2↑
C、稀硫酸与氢氧化钡溶液反应
H+ + OH- +Ba2+ +SO42-=H2O + BaSO4↓
D、氢氧化铜与稀硫酸反应
Cu(OH)2 + 2H+= Cu2+ +2H2O
3.下列四种物质的溶液中所含微粒(分子、离子)种类最多的是( )
A. 盐酸 B. 硫酸 C. 氢氧化钡 D. 醋酸
4. 欲配制含有大量下列各离子的溶液,能实现的是( )
A. Na+,CO32-,OH-,H+ B. Cu2+,NH4+,K+,NO3-
C. Ca2+,K+,NO3-,OH- D. Mg2+,HCO3-,Na+,Cl-
5. 在酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
A. NH4+、Fe3+、SO42-、NO3- B. K+、Na+、HCO3-、NO3-
C. K+、NH4+、MnO4-、SO42- D. Na+、K+、NO3-、SO42-
6.碱性溶液中能大量共存且溶液为无色透明的是( )
A.K+、MnO4-、Na+、Cl-
B.K+、Na+、NO3-、CO32-
C.Na+、H+、NO3-、SO42-
D.Fe3+、Na+、Cl-、SO42-
7.下列离子方程式改写成化学方程式正确的是( )
A.Mg2++2OH-===Mg(OH)2↓
MgSO4+Ba(OH)2===Mg(OH)2↓+BaSO4↓
B.Fe+Cu2+===Fe2++Cu
Fe+Cu(OH)2===Fe(OH)2+Cu
C.Ag++Cl-===AgCl↓
AgNO3+HCl===AgCl↓+HNO3
D.CO2+2OH-===CO32-+H2O
CO2+Ca(OH)2===CaCO3↓+H2O
8.某研究性学习小组的同学做了一个趣味实验:将一只鸡蛋放入食醋中,过一会儿发现蛋壳表面附有气泡,第二天发现蛋壳变软了,你认为鸡蛋壳与食醋发生反应的离子方程式正确的是( )
A.CO32-+2H+===H2O+CO2↑
B.CaCO3+2H+===Ca2++H2O+CO2↑
C.CaCO3+2CH3COOH===Ca2++2CH3COO-+H2O+CO2↑
D.CO32-+2CH3COOH===2CH3COO-+H2O+CO2↑
9.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
A.氢氧化钠与盐酸;氢氧化钠与碳酸
B.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液
C.Na2CO3溶液与硝酸溶液;CaCO3溶液与硝酸溶液
D.石灰石与硝酸反应;石灰石与盐酸
10.下列离子方程式书写正确的是( )
A.碳酸钙与盐酸反应:CO32-+2H+===CO2↑+H2O
B.硫酸和氯化钡溶液反应:Ba2++SO42-===BaSO4↓
C.铜片插入硝酸银溶液中:Cu+Ag+===Ag+Cu2+
D.铁钉放入硫酸铜溶液中:Fe+3Cu2+===2Fe3++3Cu
11.某溶液中可能含有HCO3-、Cl-、SO42-、NO3-、CO32-等阴离子。
(1)当溶液中有大量H+存在时,则上述阴离子在溶液中不可能大量存在的是 。
(2)当溶液中有大量Ba2+存在时,则上述阴离子在溶液中不可能大量存在的是 。
离子方程式的正误判断:
有关离子方程式的正误,大致可以从以下几个方面来判断,这也是正确书写离子方程式的要求。
1.离子反应是否符合客观事实,不可主观臆造反应在产物及反应。如2Fe+6H+==2Fe3++3H2↑就不符合客观事实。
2.“=”、“ ”、“↓”、“↑”的使用是否正确。
”、“↓”、“↑”的使用是否正确。
3.化学式拆写是否正确。这是书写离子方程式步骤中最关键的一步,拆写应注意以下几点:
①不用离子方程式表示的离子反应类型:不在溶液中进行的任何反应通常都不用离子方程式表示。
②注意“拆写”要求:
|
拆写成“离子符号”的物质 |
不能拆的物质 |
|
强酸:H2SO4、HNO3、HClO4、HCl、HBr、HI |
沉淀、气体、金属、非金属单质、氧化物、弱酸、中强酸(H3PO4、H2SO3)、弱碱、中强碱(Mg(OH)2)、水等 |
|
强碱:NaOH、KOH、Ba(OH)2、Ca(OH)2 |
|
|
易溶盐:CaCl2、NH4Cl、CH3COONa、Na2CO3、 Fe(NO3)3、CuSO4……等 |
③微溶物的写法:一般来说,微溶物的澄清溶液写成离子形式;浑浊或沉淀时写成化学式,如澄清石灰水表示为“Ca2++2OH-”,而石灰乳则表示为“Ca(OH)2”。
例:向澄清石灰水中通入少量CO2: Ca2+ + 2OH- + CO2 == CaCO3↓+ H2O
向石灰乳中通入通入少量CO2: Ca(OH)2 + CO2 == CaCO3↓+ H2O
④可溶性多元弱酸酸式盐的酸式根一律保留酸式根的形式。如NaHCO3溶液应拆成“Na++HCO3-”,而不能拆成“Na++H++CO42-”。
故:NaHCO3 溶液与KOH溶液混合:HCO3- + OH- ==H2O+ CO32-
而强酸的酸式盐——如:NaHSO4一步电离成“Na++H++SO42-”
故:NaHSO4溶液与KOH溶液混合:H+ + OH- == H2O
4.看是否漏掉离子反应。如Ba(OH)2溶液与硫酸铜溶液反应,既要写Ba2+与SO42-的离子反应,又要写Cu2+与OH-的离子反应。
5.是否遵循三大守恒,即质量守恒、电荷守恒和得失电子守恒,如:
Ag++Cu= Ag ++Cu2+(错误) 2 Ag ++Cu=2 Ag +Cu2+(正确)
6.看反应物或产物的配比是否正确。如稀H2SO4与Ba(OH)2溶液反应
H++OH-+SO42-+Ba2+==BaSO4↓+H2O, (错误)
2H++2OH-+SO42-+Ba2+==BaSO4↓+2H2O (正确)
离子共存的判断:
1.由于发生复分解反应,离子不能大量共存——参阅“必修1—P110—溶解性表:
①有气体产生——如:H+与CO32-、HCO3-、S2-、HS-、SO32-、HSO3-等不能大
量共存,主要是由于发生CO32-+2H+=CO2↑+H2O、HS-+H+=H2S↑等。
②有沉淀生成——如: Ca2+、Mg2+ 、Ba2+等与SO42-、SO32-、CO32-等不能大量共存,主要是由于Ba2++CO32-=BaCO3↓、Ca2++SO42-=CaSO4↓(微溶);
Mg2+、Al3+、Cu2+、Fe2+、Fe3+等与OH-不能大量共存是因为:
Cu2++2OH-=Cu(OH)2↓,Fe3++3OH-=Fe(OH)3↓等;
③有弱电解质生成——如:OH-、ClO-、F-、CH3COO-、PO43-、HPO42-、H2PO4-等与H+不能大量共存,主要由于OH-+H+=H2O、CH3COO-+H+=CH3COOH等;
一些弱酸的酸式根或NH4+不能与OH-大量共存是因为:
HCO3-+OH-=CO32-+H2O、HPO42-+OH-=PO43-+H2O、NH4++OH-=NH3·H2O
此类离子反应总是朝着使溶液中某些离子浓度降低的方向进行!
2.由于发生氧化还原反应,离子不能大量共存。
①一般情况下,具有较强还原性的离子不能与具有较强氧化性的离子大量共存。
如:I-、、S2-、HS-和Fe3+不能大量共存是由于:
2I-+2Fe3+=I2+2Fe2+、 2Fe3++ S2-=S↓+2Fe2+、 2Fe3++3S2-=S↓+2Fe S↓。
②在酸性或碱性的介质中由于发生氧化还原反应而不能大量共存。
如:NO3-和I-在中性或碱性溶液中可以共存,但在有大量H+存在下不能共存;
3.注意题目要求:
①看清“一定大量共存”、“可能大量共存”、还是“不能大量共存” 等要求。
②若溶液无色——则Cu2+(蓝)、Fe3+(棕黄)、Fe2+(浅绿)、MnO4-(紫)等有色离子不能存在。
③溶液中有H+——溶液呈酸性;紫色石蕊试液变红;溶液PH<7;加入铝粉后放出H2等。
溶液中有OH———溶液呈碱性;紫色石蕊试液变蓝;溶液PH>7;加入铝粉后放出H2等。
