第一章 气体
本章从理想气体的概念出发,以理想气体状态方程为基础讨论实际气体的行为,导出了对比状态定律和实际气体的普遍化压缩因子图。
一、 概念
1. 理想气体:(1) 在任何温度和任何压力下都能严格遵从理想气体状态方程的气体。
(2) 分子之间无相互作用力,分子没有体积的气体。
2. 分压:混合气体中,某一组分气体的压力,pi = yi p
3. 临界点与临界参数:在气体的p-V图中,表示气体与液体以乳浊态共存的拐点。当系统处于该点状态时,气液的界面消失,两相的性质差别消失。表示该点状态的状态参数称为临界参数,用TC,pc和Vm,C表示。
4. 对比参数:p = p/pC;b = Vm/Vm, C ;t = T/Tc
5. 压缩因子Z = V实际/ V理想
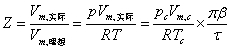
二、公式与定律
1. 理想气体状态方程:pV = nRT
2. 道尔顿分压定律: T一定且V总 = Vi 的混合理想气体,p = åpi = åni RT/V
3. 阿马格分体积定律:T、p一定的混合理想气体,V = åVi = åni RT/p
4. 实际气体的状态方程:
Van der waasl状态方程:
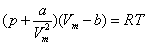
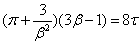
5. 对比状态定律:气体在相同的对比温度和对比体积下,具有相同的对比压力。
第二章+第三章 热力学第一、第二和第三定律
这两章的主要内容是围绕各种常见热力学过程的部分物理量(DU、DH、DS、DA、DG、W、Q、T、p和V)的计算,以及过程自发方向和限度的判断来展开的。这些计算和判断反映了热力学第一、第二和第三定律在封闭的(n一定的)理想气体系统、相变系统和化学反应系统中的运用。综合学习内容在概念、公式及计算过程与判据的运用,作如下总结。
一、 基本概念
1. 系统与环境
(1) 系统:到目前为止,学习围绕n一定的均相封闭系统和隔离系统。对于n一定的均相封闭系统,热力学状态函数与系统组成无关(组成不是变量)。所有涉及的公式对这类系统是适用的。
三类系统之间的关系及划分的方法。
(2) 环境:对于n一定的均相封闭系统而言,其与环境的关系在于能量的交换(注意W和Q的符号规定)。在DSsur的计算中,将这种能量交换过程视为可逆的(DSsur = - Qsys/Tsur)。
2. 状态函数及其性质
常见的热力学状态函数为U、H、S、A、G、T、p和V。其中,U、H、S、A、G和V是系统的广度性质,T、P和Zm( = Z/n; Z =U、H、S、A、G和V)是系统的强度性质。
性质:(1)全微分;(2)只与状态有关,与途径无关;(3)与状态有单值对应关系。
3. 热力学平衡态
热力学平衡态包含热平衡、力学平衡、相平衡和化学平衡。当系统的热力学平衡态只有:
(1) 热平衡和力学平衡时,系统经历过程变化只是简单的状态变化(可用PVT变化来描述)。
(2) 热平衡、力学平衡和相平衡时,系统经历相变化过程。
(3) 热平衡、力学平衡和化学平衡以及热平衡、力学平衡、相平衡和化学平衡,系统经历化学变化过程。
4. 热与热容
Q、Cp和CV等为与途径有关的过程量。
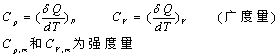
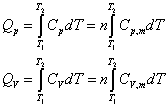
5. 功与膨胀功
dW = dWe + dWf,是与途径有关的量。
膨胀功:dWe = -pedV
一般过程: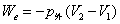
可逆过程: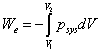
6. 可逆过程(准静态过程):系统总是与环境保持几乎接近平衡状态下发生的变化过程。
7. 焦耳实验:低压或理想气体的自由膨胀实验。
8. 节流膨胀:气体在保持恒定压差和恒定温差时的膨胀过程。
9. Carnot循环:由理想气体经历等温可逆膨胀、绝热可逆膨胀、等温可逆压缩和绝热可逆压缩构成的循环过程。
10. 自发过程:无需外力帮助,能够自动进行的过程(不可逆过程)。
二、公式与定律
n一定的封闭系统:


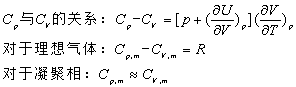
理想气体绝热可逆过程方程式:
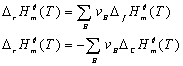
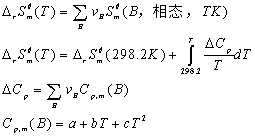
Kirchhoff定律: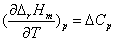
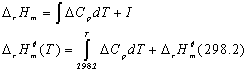
Hess 定律:不管化学反应分几步完成,该反应的热效应相同。
dT = 0,dp = 0,dWf = 0的可逆相变过程:

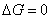
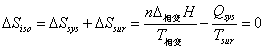
5.状态函数之间的关系
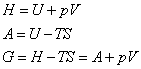
6.热力学基本方程和Maxwell关系式
n一定的封闭系统,Wf = 0,可逆过程
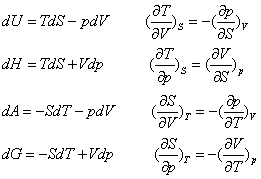
7.判别过程自发和达到限度的三个判据
熵判据: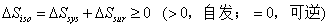
Helmholtz自由能判据:dT = 0,dV = 0,dWf = 0

Gibbs自由能判据:dT = 0,dp = 0,dWf = 0
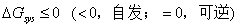
对于不可逆过程DSsys和DGsys,根据状态函数与状态有关与途径无关的性质,设计始、终态相同的可逆过程来计算。
第二篇:无机化学考研总结
转载自free kao yan
首先说明一下,我是复习考有机专业的,因为接触无机比较早,也看过一些无机的教材,对无机的知识点略有了解,同时应版主要求,把版中无机的讨论带动起来,故介绍一下个人学的无机的心得,供大家参考,仅代表个人观点.
无机的东西比较杂,并且比较松散,主要可以分为理论部分和元素化合物部分
理论部分主要分为四大结构和四大平衡,以及化学热力学,动力学初步和溶液
四大结构:原子结构,分子结构,配合物结构,晶体结构
四大平衡:酸碱平衡,沉淀溶解平衡,配位离解平衡,氧化还原平衡
如果你考物化的话化学热力学和动力学基础就不用看了,物化讲的比这个透彻得多,平衡的总纲以及溶液部分在物化里面也是讲的很详细;
如果你分析化学学得好的话,四大平衡也可以少看很多,因为分析化学就是建立在四大平衡的基础上的(仪器分析不算,呵呵);
而结构化学里面所涉及到的结构问题又比无机的四大结构深多了,同样如果你在这方面比较强,那四大结构又省了很多事.
但是如果每门掌握的都不透彻怎么办呢?不要担心,无机的理论部分仅仅是是一个大纲性质的东西,也就是总结性的概括.所以每种理论都有,但是每种理论要求都比较简单,按照四大结构-四大平衡-化学热力学初步-化学动力学初步-溶液的顺序自己仔细地过一遍也不是很难的事情,起码我感觉比自学有机容易多了,呵呵
如果你的化学基础比较扎实,也不要在旁边偷偷笑,正所谓"结构决定性质",无机尽管理论比较简单,但是其精髓在于用简单的理论解释大量的现象和物质性质,在你掌握相关理论的基础上要能够灵活地把它们运用到平时见到的单质和化合物的性质解释.这样才算真正掌握了无机的理论.
总的来说无机的理论部分重点在运用.
而无机化学的重点则元素部分,这个也是无机主要讲的东西以及无机的特点.
首先建议周期表最好是背过,认识并且会写除f区以外的元素,镧系最好能背过,一些重要的比如说La Ce也要知道的.
个人感觉主族元素里面比较重要的是B,P,S,Sn,Pb,As,Bi,
副族里Hg,Co,Cr,Mn,Ti,V,Cu等比较重要,下面分主族和副族元素分开介绍:
第一主族里面要注意过氧化物,超氧化物,臭氧化物的结构和生成条件,焰色反应的火焰颜色(包括碱土金属和少量过渡金属的都要知道),以及碱金属的不溶盐;
第二主族Mg,Ba最常见,同时也要注意焰色反应,对角线规则(主要是三对元素Li-Mg Be-Al,B-Si)首次在这里出现;
第三主族注意B和Al, 铝热反应,Al的冶炼要注意K3AlF6的作用;B绝对是基础无机的重点元素之一,要注意它的多中心缺电子桥键的结构;
第四主族里面C,Si,Ge,Sn,Pb都要比较熟悉.碳氢化合物主要是放在有机里面了,无机主要是看它的氧化物和碳酸盐,这个比较简单.
Si的考点的比较少,但是可以和元素有机结合起来,同时Si和Ge作为半导体材料应该和材料方面联系起来,并且这个地方要顺便复习一下晶体结构中的导带理论.Sn,Pb应该是重点考察的,二价Sn的还原性以及其在反应中价态变化导致颜色变化要很清楚,四价铅具有强氧化性也是要知道的.
第五主族N,P,As,Bi重点,N的氧化物结构及合成,HNO3的还原产物都是比较烦人的东西的
三种同素异形体的性质和相互转化(主要是白磷和红磷的相互转化条件)以及磷的氢化物和含氧酸的性质也要知道.As的氧化物和硫化物小心识记,马氏试砷法和古氏试砷法要熟悉,Bi要关注正五价的强氧化性
第六主族S是重点,硫化物的不溶盐及其颜色绝对可以烦死你,硫的含氧酸结构及性质也很多,带"矾"的硫酸盐要知道
卤素属于高中元素,都比较熟悉,就不多说了.但是要小心卤素互化物和拟卤素的性质
氢和稀有气体看看就好了
这些是主族的主要内容,下面是副族
第一过渡系绝对是重点中的重点,而里面又以Cr,Mn,Cu最重要,Ti,V,Co,Ni,Fe也是常考的,Sc我的印象里面貌似从来没有考过.... Cr,Mn颜色丰富多彩,价态变化多端,够看一段时间了,Fe和Cu
可以说差不多重要,要注意不同价态元素的存在条件以及转化,Co和 Ni的性质可以和铁类比,但是注意Fe,Co三价态稳定,Ni二价态稳定,
同时Fe可以有六价,Ti和V注意下反应和颜色就好了,东西比较少
第二过渡系和第三过渡系重点元素应该是Hg,Cd,Mo,W,Re,Ag,Pt,Au,Pt.Mo和W同多酸及杂多酸要知道,[Re2Cl8]2- 中存在δ键,其成键特点和对称性要知道.
其它还需要关注的是俗名和化合物的对应关系,元素及其化合物的定性鉴定(起码常见的,我上面提到的物质的定性鉴定要知道),特殊反应要记牢,顺便提醒一下,一些关于"第一","最","唯一","特殊"的东西要知道
关于教材方面我看过三个版本,个人感觉北师大版的教材的分析得很透彻,讲解比较细致,语言通俗易懂,适合初学者学;武大的无机很全面,东西比较多,每章后面有总结和专题小节,适合提高用;而大连理工的教材感觉平平,除非是指定教材,否则没有必要参考. 同时听枫版主推荐申泮文的无机也很有水平,适合提高用,感谢他的热心.
以上只是个人学习无机的几点小心得,必定存在很多疏漏之处,在这里仅起到一个抛砖引玉的作用,还请广大研友以及化学爱好者们批评指正,把它补充完整,大家共同进步,如有疑问或者好的建议,欢迎回帖或者另开主体大家共同讨论
再次感谢版主的支持和好的建议
