酵母RNA的提取及含量测定
一、实验目的与要求
1、了解并掌握稀碱法提取RNA的原理和方法;
2、了解测量核酸浓度不同方法的原理;
3、熟悉和掌握紫外吸收法测定核酸含量原理和操作方法;
4、熟悉紫外分光光度计的基本原理和使用方法。
二、实验原理
1、RNA提取原理:
由于RNA的来源和种类很多,因而提取制备方法也很各异。一般有苯酚法、去污剂法和盐酸胍法。其中苯酚法又是实验是最常用的。组织匀浆用苯酚处理并离心后,RNA即溶于上层被酚饱和的水相中,DNA和蛋白质则留在酚层中。向水层加入乙醇后,RNA即以白色絮状沉淀析出,此法能较好的除去DNA和蛋白质。上述方法提取的RNA具有生物活性。工业上常用稀碱法和浓盐法提取RNA,用这两种方法所提取的核酸均为变性的RNA,主要用作制备核苷酸的原料,其工艺比较简单。浓盐法使用10%左右氯化钠溶液,90℃提取3-4h,迅速冷却,提取液经离心后, 上清液用乙醇沉淀RNA。稀碱法使用稀碱使酵母细胞裂解,然后用酸中和,除去蛋白质和菌体后的上清液用乙醇沉淀RNA或调pH2.5利用等电点沉淀。 酵母含RNA达2.67-10.0%,而DNA含量仅为0.03-0.516%,为此,提取RNA多以酵母为原料。
2、测定RNA含量的方法:
(1)紫外吸收法原理:核酸具有吸收紫外线的性质,在波长260纳米处有最大吸收,且在一定浓度范围内光吸收值与浓度成正比(0—50微克/毫升),符合朗伯-比尔定律。优点样品用量少,不用显色,测完后样品可以继续使用。
(2)地衣酚显色法:核酸与浓盐酸共热,放生降解,生成糠醛,后者与地衣酚反应,在三价铁离子或二价铜离子作用下,生成鲜绿色的复合物,670纳米处有最大吸收,且光吸收值与浓度成正比,符合朗伯-比尔定律。缺点反应特异性差,易受干扰。
(3)定磷法:在酸性环境中,定磷试剂中的钼酸铵以钼酸形式与样品中无机磷酸生成磷钼酸,当有还原剂存在时,磷钼酸立即被还原生成蓝色的还原产物--钼蓝,其最大吸收在660纳米处,当无机磷含量在每毫升1-25微克范围内,光吸收与含磷量成正比。测量样品核酸的总磷量,需先将它用硫酸或高氯酸消化成无机磷再行测定。总磷量减去未消化样品中测得的无机磷量,即得核酸含磷量,由此可计算出核酸含量。优点测量准确,缺点操作繁琐。
3、紫外吸收法测定RNA含量:
核酸、核苷酸及其衍生物的分子结构中的嘌呤、嘧啶碱基具有共轭双健系统(-C=C一C=C-),能够强烈吸收250-280nm 波长的紫外光。核酸(DNA,RNA)的最大紫外吸收值在260nm 处。遵照Lambert-Beer 定律,可以从紫外光吸收值的变化来测定核酸物质的含量。在不同pH 溶液中嘌呤、嘧啶碱基互变异构的情况不同,紫外吸收光也随之表现出明显的差异,它们的摩尔消光系数也随之不同。所以,在测定核酸物质时均应在固定的pH溶液中进行。
核酸的摩尔消光系数(或吸收系数),通常以ε(ρ)来表示,即每升含有一摩尔核酸磷的溶液在260nm 波长处的消光值(即光密度,或称为光吸收)。核酸的摩尔消光系数不是一个常数,而是依赖于材料的前处理、溶液的pH 和离子强度发生变化。RNA 溶液(pH = 7.0)的ε(ρ)= 7 700-7 800,RNA 的含磷量为9.5%,含1μg /mL RNA 溶液的光密度为0.022-0.024。因此,测定未知浓度的DNA(RNA)溶液的光密度OD260nm,即可计算测出其中核酸的含量。该法简单、快速、灵敏度高,如核酸3μg/mL 的含量即可测出。对于含有微量蛋白质和核苷酸等吸收紫外光物质的核酸样品,测定误差较小。
蛋白质由于含有芳香族氨基酸,因此也能吸收紫外光。通常蛋白质的吸收高峰在280nm 波长处,在260nm 波长处的吸收值仅为核酸的十分之一或更低,故核酸样品中的蛋白质含量较低时对核酸的紫外测定影响不大。
三、主要仪器和试剂
干酵母粉、pH试纸、电子天平、分析天平、100ml烧杯、量筒、吸管、离心机(4000r/min)、95%乙醇、无水乙醇、酸性乙醇、0.2%NaOH溶液、紫外分光光度计、200ug/ml的标准核酸
四、实验步骤
1、称4g干酵母粉放入200ml三角瓶中加入40ml 0.2%NaOH溶液混匀;
2、三角瓶沸水浴30min后流水冷却,转入离心管,4000r/min离心15min,结束后保留上清液,加入40ml酸性乙醇,边加边搅拌;
3、加毕,静置5min,待RNA沉淀完全后,4000r/min离心5min。弃去上清液,保留沉淀,用20ml95%乙醇洗涤分两次沉淀,每次洗完后3000r/min离心5min。
4、再用20ml无水乙醇分两次洗涤沉淀,每次洗完后3000r/min离心5min,收集沉淀到滤纸上备用。
5、准确称取0.2—0.25克样品核酸,加2毫升0.2%氢氧化钠溶液和1毫升水溶解,调成糊状,再加入50毫升左右水溶解,边溶解边转移到100毫升烧杯中,用0.2%氢氧化钠调至中性,定容至100毫升,再取3毫升定容至100毫升备用(由于要做平行实验,因此是从最先定容的100ml中分别取3次3ml,再分别定容至100ml)。(开始溶液呈乳白色,完全溶解后变为澄清透明溶液)
注:本次实验一共称取了0.1765g样品。
6、制作标准曲线(标准核酸稀释至100ug/ml),测定样品。
五、实验结果
1、实验数据:
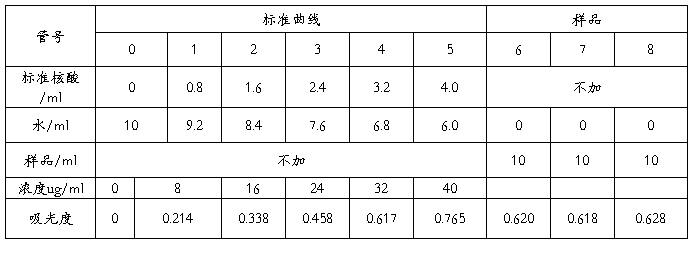
2、绘图:
通过所绘的标准曲线可知三组平行实验所对应的标准RNA的浓度分别为32.4ug/ml、32.0 ug/ml、32.8 ug/ml,平均为32.4ug/ml,则
样品中RNA质量为32.4*10000/3=1.08*10^5 ug=0.1080g
样品中RNA含量为0.1080/0.1756=0.615=61.5%。
六、实验结果分析
本次实验测得样品中RNA的含量为61.5%,总体来说还算可以,但仍有些许误差,造成误差的原因可能有以下几种:
1、因为是做了三次平行试验,所以在样品三次定容时可能有些许误差。
2、在配置标准RNA浓度时可能量取时有误差而导致RNA浓度有些许的误差。
3、样品中可能含有少量蛋白质,DNA,对紫外光也有强吸收作用会产生误差。
4、酵母RNA被溶解后调PH时由于用的是PH试纸而不是PH计这种较为准确精密的仪器,所以可能会影响测定结果,造成一定的误差。
本次实验也有许多可取之处:
1、使用紫外分光光度仪时操作规范,对每个比色杯在实验前都用待测液体进行了润洗,而且在放入仪器中时都将外表擦拭干净。
2、在提取RNA时操作规范,离心过程也比较顺利。
3、使用分析天平时做到规范准确称量。
七、注意事项
1、在使用离心机时要注意要将对角处的物体配平,否则不但不能达到离心的效果,反而会对离心机造成损害;
2、本次实验第二次洗涤沉淀时用乙醚比较好,但由于乙醚是有毒物质,故本次实验用无水乙醇代替;
3、使用紫外分光光度仪时要小心使用石英比色杯,要用手拿糙面不要碰滑面;
4、设计标准曲线梯度时要合理,不能组数太多导致实验过于复杂;
5、注意要设计平行实验,本次实验要注意平行实验是分别取3ml液体分别定容三次,而不是定容一次而取三组测量。
八、课外延伸
1.破酵母细胞时为什么要在沸水浴中进行?
答:由于酵母细胞外有一层厚厚的细胞壁,而RNA存在于细胞质中,所以必需将酵母细胞的细胞壁研磨破碎后才能提取出RNA。加入NaOH之后水浴煮沸30min的作用是促进细胞壁变性,使类脂、甘露聚糖、葡聚糖等成分部分分解,使蛋白质变性,从而使细胞破裂,RNA则从细胞中分离出来。
另外细胞中含有多种分解RNA的酶类(如RNase等),为了避免RNA在提取过程中被降解,得到较为完整的RNA分子,破碎酵母细胞时应在沸水中进行,这样可以使细胞中降解RNA的蛋白酶类活性受到抑制甚至变性失活,从而起到保护RNA分子的作用。
2.为什么用酵母作为实验原料?如何使RNA从酵母中释放出来?RNA的等电点是多少?
答:酵母繁殖快,生长周期短;其细胞质中的核酸大部分是RNA,而DNA很少;RNA提取液与菌体分离比较容易,因此酵母是提取RNA的好材料。
工业上将RNA从细胞中释放出来主要有三种方法,包括稀碱法、浓盐法和自溶法。(1)稀碱法是在一定的碱浓度下,使构成细胞壁的蛋白质、脂肪及糖的化合物得到水解,从而破坏细胞壁,使RNA从细胞中释放出来,该方法属于化学破壁法。(2)浓盐法是基于改变酵母细胞的渗透压,是细胞自身破裂而释放出RNA,即利用高浓度的盐(10% NaCl)在90~100°C条件下改变了细胞膜通透性,并将核蛋白体解离成RNA和蛋白质而使 RNA释放到盐溶液中。同时,90~100°C的高温可破坏磷酸单酯酶和磷酸二酯酶的活力,避免RNA的降解。该方法属于物理化学破壁法。(3)自溶法是利用某些酵母菌种在发酵结束后,细胞中的溶酶体膜破裂,使得溶酶体中的水解酶释放到细胞之中,利用菌体自身的酶系将细胞溶解,从而释放出RNA。通常自溶法的菌浓度为2%,PH值9.5~10,自溶温度以60~65°C为宜。
RNA的等电点为PH2.5。根据核酸在等电点溶解度最小的性质,将溶液在低温下调pH至2.0~2.5,RNA则以白色絮状沉淀形式从盐溶液中析出。再次离心,固液分离,便可获得RNA粗产品。
3 为什么用稀碱溶液可以使酵母细胞裂解?
答:酵母菌的细胞壁呈“三明治”结构——外层为甘露聚糖,内层为葡聚糖,中间层为一层蛋白质分子(包括多种酶类),此外细胞壁壁上还含有少量的类脂和几丁质。稀碱溶液能够对酵母菌细胞壁和细胞膜上的脂类起到抽提作用,脂类发生皂化反应从而被分解,使细胞穿孔。同时细胞壁的聚糖成分在碱液中会部分水解,蛋白质(包括多种酶类)也会发生变性,从而增加酵母细胞的通透性,酵母细胞原生质膜失去选择透过性,细胞就破裂使RNA流出。
4.核酸的溶解性质是什么?常用什么试剂分离沉淀核酸?
答:核酸是具有极性的高分子物质,根据相似相溶原理,DNA和RNA都是微溶于水,其钠盐在水中的溶解度较大。它们可溶于2-甲氧乙醇,也可溶于10%左右的氯化钠溶液,但不溶于乙醇、乙醚和氯仿等一般有机溶剂,尤其是在50%左右的乙醇溶液中溶解度很小。因此,常用乙醇从溶液中沉淀核酸,当乙醇浓度达50%时,DNA就沉淀出来,当乙醇浓度达75%时RNA也沉淀出来。
5.采用紫外光吸收法测定样品的核酸含量,有何优点及缺点?
答:用紫外光吸收法测定样品的核酸含量,具有简单、快速、灵敏度高的优点,并且待测核酸样品中含有的微量蛋白质和核苷酸等吸收紫外光物质,产生较小测定误差。但该法在测定样品内混杂有大量的上述吸收紫外光物质时,则会产生较大测定误差,需要设法事先除去。
6.若样品中含有核苷酸类杂质,应如何校正?
答:当样品中含有核苷酸类杂质时,需要加钼酸铵-过氯酸沉淀剂处理,沉淀除去大分子核酸,测定上清液260 nm处光密度,以此作为对照;再从未加沉淀剂测得的样品液260nm光密度中扣除。
第二篇:实验三 酵母核糖核酸的提取及测定
实验三 酵母核糖核酸的提取及测定
一.研究背景及目的
核苷酸类物质及其衍生物是遗传工程、医药、食品、农业生产和科研领域十分重要的生化试剂和原料 。其功能有:

目前我国由核酸生产的核苷酸类产品的年产量不足 100t ,不仅不能满足国内市场需要 ,而且每年还需从国外进口270t ,耗费外汇 10 亿美元左右 。我国是个农业大国 ,人 口众多 ,就核苷酸应用于农业、食品方面来说 ,核苷酸市场潜力很大 。现有可耕地面积 14 亿多亩近 2/ 3 的中低产地 , 与发达 国家相比,农作物单产还较低 。若按全国 10 亿亩耕地全部 使用核苷酸配剂 ,每亩用量 20g 计 ,这 10 亿亩耕每年使用核苷酸可达 2 万多t[2] 。 本次实验是食品医药卫生领域大工业生产RNA制剂的具体设计。
二.原理
微生物是工业上大量生产核酸的主要原料。采取酵母因为核酸的提取不需要很高活性的菌体,酵母是啤酒厂废弃的原料,从经济角度讲,用来提取核糖核酸最为理想。
提取RNA的方法很多,常见的有如下几种:(本次实验采取浓盐法10% NaCl)

核酸是由糖、碱基、磷酸以一定比例构成的,理论上定量核酸只需测定其中一种即可。定磷法准确、微量、快速,是最好的方法。紫外吸收法简单快速,但是当体系内有蛋白质及其他含共轭双键物质存在时干扰较大。
本次实验采用紫外吸收法。
基本的提取策略为:我们可以通过使用化学因素破坏细胞膜,使其中的核酸流出来,接着纯化、测定含量即可。其中影响我们纯度和定量的主要因素就是蛋白质及有共轭双键物质的干扰,所以,我们的主要目标就是排除蛋白质和有共轭双键物质对含量测定的影响。尽量保持RNA的完整性有利于提取率。
对于RNA酶的干扰,工业生产的流水化作业,使得人员参与较少,而且工业生产并不像实验室对RNA的完整性要求那么高,所以工业生产中RNA酶的存在不是主要矛盾。
三.仪器与试剂
试剂:10%NaCl;6MHCl;95%乙醇(分析纯);2%氨水;RNA沉淀剂
仪器:722-分光光度计(上海分析仪器总厂);微量可调手动移液器(大龙牌);具塞试管(15ml);漏斗(25ml一只,50ml两只);研钵;匀浆器;低速离心机(飞鸽牌,TDL-40B,上海安亭科学仪器厂);药物天平(HCTP12B1,北京宣武天平厂制);硫酸纸;烘箱()
四.实验步骤
按下表进行操作:
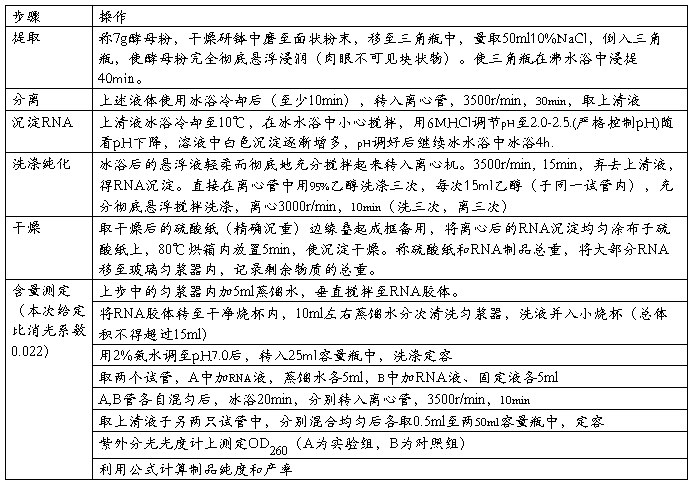
五.数据整理与结果计算
I.干燥RNA样品含量:

II. OD260记录表:

OD260/ OD280=2.25
一般RNA的OD260/ OD280>2;DNA OD260/ OD280约为1.9;样品中有蛋白质含量较高时比值下降。因此,可推断,该体系为RNA且较纯。
紫外法测定蛋白质含量校正数据OD280/ OD260的最小值为0.595.因此没有办法得到蛋白质的准确值。
根据下公式得到制品纯度和产率:
 =57.9%
=57.9%
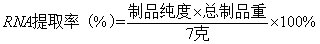 =42.9%
=42.9%
六.质疑:
1.为什么采取紫外吸收法定量核酸.由于蛋白质含量较低时,对吸光度的影响不大,因为在260nm下,蛋白质的吸收值约为核酸的1/10.本次实验经过多次乙醇的洗涤,核酸的纯度已经达到一定的浓度,紫外法操作简便,因此可使用紫外法。
2.测定W3之前需要烘干一下。这样测量的才是转入匀浆器的样品量。
3.为什么A不做多组平行管。因为没有意义,如果从稀释后的溶液中取出3只试管的待测液,相当于同一个待测测量3次;如果我们从定容那步开始做平行,也是相当于同一溶液测3次。追根溯源,如果想要做平行,就要从加热浓盐法破壁开始,实际上,如果想要测出这种方法所能达到的纯化程度,这样做是有意义的,如果作为学生实验,这么做意义并不大反而增加工作量。
4.文献《影响浓盐法提取啤酒酵母RNA的工艺参数研究》中认为浓盐法破壁的原理是高盐使得酵母自身破裂放出RNA,这点我不敢苟同。浓盐法是改变细胞膜的透性,并没有使细胞裂解。
5.有的组测量了以蒸馏水为空白对照组的OD260和OD280,结果发现管A,B之间的吸光度不是简单的加和关系,这点让我很费解。可能的原因也没有猜到,难道是狼比尔定律在浓度很低(B管)时也不适用吗?
总结:
抓主要矛盾!这是我这次实验后感受最深的一句话。举个例子在称量RNA制品重时,以下几个事件对重量的影响:
被人碰了撒地上了>称量时一碰撒天平上>速度慢样品吸水
我这回称量完成后虽然想到了人太多,小心样品!但是没有重视,就真出事了。实验时一定要避免不必要的意外。我不犯人,但也要防止人犯我。在撒了样品后,我们从新收集了较为干净的样品,那个时候,应该再次烘干称量的,但是由于手忙脚乱的收集过后,不太清醒,直接就称量了。但是,我们在称量W3时又从新回去烘干的,这就导致了RNA实际转入进匀浆器的要少,因此,导致我们算出的纯度有所下降。虽然洗了四次,而且产率开始很好,但是一次意外过后,都化作云烟了。这就告诫我,实验时要注意意外事件的发生。
参考文献
[1].中国农业大学.生物化实验室.生物化学实验指导 26-28页
[2].王定昌.核酸酵母产品的开发和应用[J].粮油食品科技 第10卷 20##年 第4期
[3]. 乔宾福. 实用微生物技术[M].上海:上海科学技术文献出版社, 1994.
思考题:
1、 本实验为何选用酵母为生产原料?在分离纯化的实验选材上有哪些主要原则?
选择酵母的原因:①微生物繁殖快、代谢旺盛、体积小、培养成本低利于工业生产 ②啤酒酵母是啤酒厂的副产品,来源广、成本低,合理的处理酵母也能防止对环境的污染③微生物中酵母的RNA含量比较高(2.7-11%)[3] ④ 酵母的生活规律为人熟知,用于生产、使用较为安全 。
分离纯化 原则: 选材:①材料中所含目标产物较多②材料中的其他杂质易于除去③ 材料易得
2、浓盐法的选择是基于怎样的考虑?
仅仅从RNA回收率和纯度上看,稀碱法略优于浓盐法,且时间短,反应温度低。但是稀碱法对酵母有选择,提取颜色较深,很难溶解,而且对设备要求较高,设备一次性投资较大,再加上管理和维护等原因,一般采用浓盐法。同时,流水线作业可以大幅度缩减时间,浓盐法慢些也是可以承受的。本次的实验就是实现工业生产核酸的过程,所以采用浓盐法。
3、本方法为何选用等电点沉淀作为最主要的纯化步骤?
RNA等电点和大多数蛋白质相差较大,因此决定我们有等电点沉淀的理论基础。实验室中为得到RNA的自然结构,会采取有机溶剂沉淀的方法,但工业生产的核苷酸多为食用、药用,有机溶剂不易除去,会造成安全隐患。同时有机溶剂较昂贵,通常可燃,也不适于工业生产中大量使用。
4、DNA的去除本方法是怎样考虑的?
本实验中,采取浓盐法改变细胞膜的透性,使得细胞质中的RNA流出来,但是并没有破坏到核膜的透性,因而大多数的DNA还留在细胞内。有可能有部分核膜被损坏,或是部分DNA夹在线粒体中流出来时,实验主要利用DNA等电点和RNA差别较大的特点除去这部分DNA(RNA等电点在2.0-2.5,而DNA由于蛋白质修饰等原因等电点在4.0-4.5)所以在我们调等电点沉淀RNA时,DNA就留在了溶液中而被除去了。同时DNA在10%的NaCl溶液中溶解度较小,大部分以沉淀形式存在于溶液中,也起到一定的去除DNA的作用。
5、大量的乙醇洗涤在工业生产上有否危险隐患?厂家是如何考虑的?
乙醇属于易燃易爆的危险品,大量使用一定是有危险隐患的。但是只有经过乙醇的洗涤才能除去RNA中掺杂的无机盐、色素、脂溶性杂质。高浓度的盐会水和大量的水分子,RNA分子之间容易形成氢键发生沉淀,乙醇与水任意比例互溶,因而可以洗去盐和与RNA结合在一起的水。同时,乙醇易挥发,易于除去。同时乙醇较为廉价,毒性低、回收容易,因此适于工业使用。
6、本实验在用紫外法测定RNA含量时,为什么要固定测定液的pH值,若pH值不固定,会影响测定结果吗?为什么?
会影响测定。因为紫外法需要在中性条件下测定吸光度。因为核酸在强酸或强碱条件下,会发生氢键断裂,紫外吸收升高,这种现象称为增色效应。因此,测定核酸含量时需要调至中性,我们所使用的比消光系数也是在中性条件下测定的。
7、在测定中,加钼酸铵-过氯酸沉淀剂的作用是什么?离心除去沉淀后,其上清液为什么要稀释100 倍?
加钼酸铵-过氯酸沉淀剂的目的是沉淀RNA,作为对照组(透光度100%)。因为A管稀释了100倍,如果B管想要作为A管的对照组,就必须相应的稀释相同的倍数才行。如果我们加入的试剂对吸光度有影响的话,我们就更有必要进行相应的稀释了。
